HERRAMIENTAS DE SOPORTE PARA EL RAZONAMIENTO CLÍNICO EN MEDICINA INTERNA BASADAS EN INTELIGENCIA ARTIFICIAL
..................
Andrés Eduardo Rico-Carrillo ¹,²
Resumen
Palabras clave: Inteligencia artificial; servicios médicos; herramientas; ética; registros clínicos electrónicos.
..............
² Departamento de Medicina Interna, Fundación Javeriana de Servicios Médicos y Odontológicos Interuniversitarios “Carlos Márquez Villegas” JaveSalud IPS, Bogotá.
SUPPORT TOOLS FOR CLINICAL REASONING IN INTERNAL MEDICINE BASED ON ARTIFICIAL INTELLIGENCE
Abstract
Artificial intelligence is a set of tools that simulate the cognitive processes of humans and based on the analysis of a large volume of data has the ability to collect and organize information, allowing processes of: decision-making, reasoning, recognition of voice, image perception and visual interpretation. In medicine, it makes its way as a strategy for the improvement in the provision of services in the different specialties. Through a clinical case, the applicability of artificial intelligence in the daily life of the outpatient field of internal medicine will be shown, where the relevance of Dr. Maskó’s phrase is highlighted: “AI is not meant to replace medical professionals, but those who do not use it will probably be replaced by those physicians who do use it”.Keywords: Artificial Intelligence; Medical Resources; Tools; Ethics; EHealth; Electronic Health Records/Electronic Medical Records.
Introducción
Esta revisión descriptiva de la literatura en torno a la aplicabilidad de herramientas de inteligencia artificial en la práctica clínica tiene por objetivo aportar en el esclarecimiento de un horizonte que hasta el momento está colmado de incertidumbre. La inteligencia artificial está cada vez más presente en la vida cotidiana, una de las formas más comunes la experimentamos con asistentes de voz, tales como, Google, Siri y Alexa y aplicaciones que permiten transcripción de voz a texto o texto a voz. En medicina, el uso de estas herramientas facilita los procesos asistenciales y administrativos, contribuye con la disminución de la carga laboral del personal asistencial y optimiza los tiempos de atención. Esta tendencia innovadora creciente en el mundo ha generado la inminencia de un cambio del paradigma en la atención de personas sanas, enfermas, convalecientes o en rehabilitación. Se expondrá un caso de vida real para ejemplificar los aspectos relevantes en la implementación de la inteligencia artificial en la práctica médica (1-6).Caso Clínico
Adriana, es una mujer de 54 años, nacida en España, vive en Bogotá hace 20 años, asiste a consulta de medicina interna remitida por medicina general ante el hallazgo de presión arterial de 142/90 mmHg y llega 7 minutos tarde a consulta. Dentro de la revisión por sistemas, como aspectos relevantes se destacan episodios ocasionales de palpitaciones y muestra un registro de ritmo cardiaco tomado por su reloj inteligente compatible con fibrilación auricular. Como antecedentes de importancia, fue fumadora de 10 cigarrillos/día por 20 años, hasta hace 10 años, sufrió fractura de Colles por caída de su propia altura, que requirió reducción abierta y fijación interna, tuvo histerectomía más salpingo-ooferectomía bilateral hace 10 años por una lesión NIC III, su padre sufrió infarto de miocardio a los 48 años y su madre presentó fractura de cadera a los 78 años, es hipertensa y se encuentra en tratamiento de cáncer de seno. Al examen físico se encuentra con pulso regular y ruidos cardiacos rítmicos, presión arterial de 138/92 mmHg, estatura de 1,62 metros, peso de 70 kg, perímetro abdominal 94 cm.Trae resultados de paraclínicos que muestran: creatinina 1,26 mg/dl, colesterol total 278 mg/dl, colesterol HDL 35 mg/dl, triglicéridos 310 mg/dl, glicemia 102 mg/dl, uroanálisis con proteinuria, electrocardiograma en ritmo sinusal, onda P duración aumentada (> 0,12 segundos), S en V3 de 8 mm, R en aVL de 12mm, S en V1 de 18 mm, R en V6 de 22 mm y relación albuminuria/creatinuria 120 mg/g. Con base en la descripción del caso, se plantean algunas preguntas para definir las estrategias de diagnóstico, tratamiento y prevención: ¿La función renal es normal?, ¿Tiene daño de órgano blanco?, ¿tiene dislipidemia familiar?, ¿Cuál sería el cálculo del riesgo cardiovascular?, ¿Cuál es FINDRISC?,¿Tiene riesgo de fractura osteoporótica?, ¿Tiene riesgo de cáncer?, ¿Cuáles son las metas de tratamiento?, ¿Son suficientes 20 minutos para contestar estas preguntas, educar y asesorar a la paciente?
Aplicando herramientas de inteligencia artificial al caso clínico
Para entender las posibles actividades en las que es susceptible la aplicación de las herramientas de inteligencia artificial se ha realizado un mapa de travesía o “journey map” asociado con un mapa de flujo de valor del proceso de atención de la paciente del caso, que corresponde a la Figura 1.A través de un Chatbot, con un algoritmo entrenado, la paciente solicita la asignación de una cita, la herramienta evalúa la disponibilidad de la agenda, propone citas, la paciente escoge la opción, posteriormente el Chatbot le solicita el consentimiento informado para acceder a datos clínicos provenientes de registros clínicos electrónicos (49). Entre el punto 1 y 4 hay un algoritmo complementario que evalúa la complejidad del caso y realiza una programación dinámica de la agenda (43), al ser primera vez y por el motivo de remisión se asigna una duración mayor de 20 minutos.
El punto 2 nos muestra una dificultad y es que a pesar de tener una limitación en el tiempo la paciente llega tarde, sin embargo, a través de la programación dinámica mediada por una herramienta de inteligencia artificial se reprograma el horario de atención y en tiempo real se avisa a los otros pacientes. En los puntos 3 y 4, se realiza la consulta médica y con base en algoritmos previamente diseñados se realiza el análisis de los datos, se construye la historia clínica sin necesidad de digitar y se entrega al clínico. En el punto 5, los algoritmos realizan la clasificación multidimensional de riesgo a través del cálculo simultáneo de Score, Framingham, PROCAMS y los ajusta según la evidencia disponible, de la tasa de filtración glomerular con varias ecuaciones, el FindRisc, el Frax y el riesgo de cáncer junto con el riesgo de sufrir de hipercolesterolemia familiar. En el punto 6, se establecen una serie de sugerencias con base en “aprendizaje automatizado”, que permiten al clínico contextualizarlas a la realidad del paciente y emitir el plan terapéutico final. A través de chatbots y dispositivos móviles conectados a internet se hace el seguimiento del proceso terapéutico (1,6,9,10-13,20-44,47-49).
Tal como se describió en el mapa de flujo de valor del caso clínico expuesto, en la Figura 2 se detallan las potenciales oportunidades de implementar la inteligencia artificial como una herramienta útil para la simplificación de tiempos y movimientos durante un proceso de atención clínico, lo cual corresponde a los puntos 4, 5 y 6 de la gráfica anterior (Figura 1).
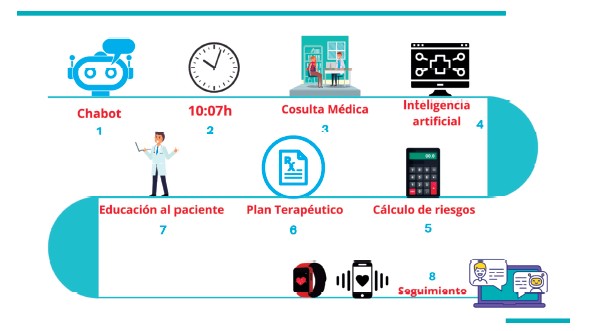
Figura 1. Flujo de atención con IA del caso: (1). Asignación de cita médica por medio de chat automatizado por IA, (2). Incumplimiento de hora de llega optimizado por IA, (3). Búsqueda de la data para alimentar IA, registros clínicos electrónicos previos y resultados de ayudas diagnósticas, (4). Uso de algoritmos de IA para realización del registro clínico electrónico, (5). Análisis de la data y cálculo multidimensional de riesgo, (6) Sugerencia de plan terapéutico individualizado con base en análisis de la evidencia científica y la data por IA y predicción de interacciones medicamentosas, (7). Contextualización psico-socio-económica del plan sugerido por IA por parte del médico y explicación al paciente, (8). Seguimiento de adherencia al plan terapéutico y desenlaces clínicos por IA.
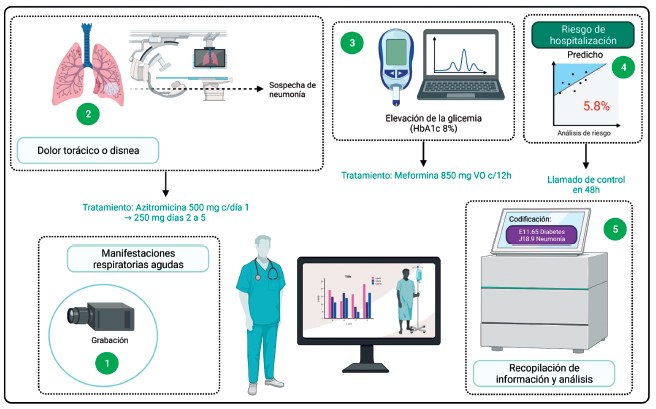
Figura 2. Ejemplo de asistente electrónico de datos (modificado con autorización de Lin S, Shanfelt T, Asch S. Reimagining Clinical Documentation With Artificial Intelligence, Mayo Clin Proc. 2018;93(5):563-565 https://doi.org/10.1016/j.mayocp.2018.02.016).
Existen diferentes herramientas basadas en inteligencia artificial que pueden ser aplicadas a la atención en salud y cuya utilidad dependerá del contexto de implementación. En la Figura 3 se describen algunas de ellas.
¿Cuáles son los potenciales beneficios del uso de la inteligencia artificial?
Cuando se pregunta a un médico qué es lo más importante para lograr el éxito en el cuidado de los pacientes, usualmente responde: conocimiento y experiencia, es decir, cuantos más pacientes trate más experiencia y conocimiento; un paradigma en el cual se confía en la concordancia de los patrones aprendidos (combinación de síntomas, signos y datos de laboratorio con los criterios diagnósticos), se configura el concepto de “paciente típico” y el tratamiento está basado en experiencias pasadas de ensayo y error, con el riesgo potencial de efectos colaterales o infectividad (35,36,37).La principal limitación para la inteligencia humana en términos de la cantidad de datos, es el tiempo. Al gran volumen de información de los registros electrónicos y dispositivos de telemonitoreo (werables), se suman los datos generados por revistas, websites y e-books en torno a la práctica clínica, que rebasan la capacidad humana de procesar y organizar la información para la toma de decisiones (34,35,36). Para manejar esta masiva cantidad de datos, se requieren herramientas que asistan en estos procesos y la inteligencia artificial brinda esa oportunidad de filtrar y priorizar información, favoreciendo un adecuado enfoque y una disminución de errores diagnósticos y terapéuticos (conciliación de medicamentos), además de eliminar la parte repetitiva del trabajo (17,23).
La inteligencia artificial utiliza algoritmos que simulan funciones cognitivas humanas a través de modelos matemáticos que son dependientes del volumen y calidad de los datos; entre más información esté disponible para el entrenamiento, mayor capacidad tendrá para ejecutar la función diseñada (1,6-9,16- 19,20,30,33,34,43,45,48).
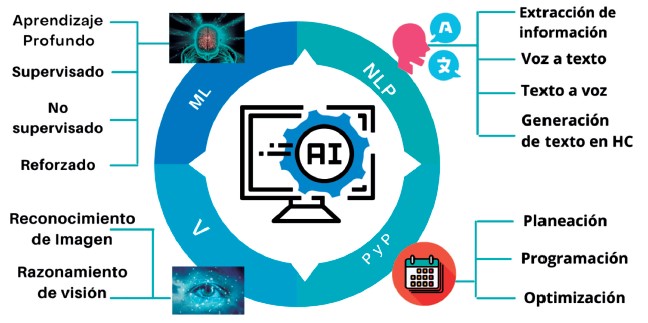
Figura 3. Tipos de herramientas de IA aplicables a la consulta externa de medicina interna (figura adaptada con autorización de The Royal College of General Practitioners, 2019 - Artificial Intelligence and Primary Care, https://www.rcgp.org.uk/-/media/Files/CIRC/artificial-intelligence-and-primary-care-jan-2019.ashx?la=en).
La obtención y análisis de “Big Data” ha sido un cuello de botella al requerir métodos estadísticos y computacionales sofisticados, pero ha generado “una taxonomía multiparamétrica de la enfermedad”, una diferenciación en la susceptibilidad, clasificación fenotípica, duración y probabilidad de respuestas positivas o negativas a determinada terapia (37). Con el desarrollo en hardware y software, el tiempo no es limitante, liberando el poder de la “Big Data”, es decir, de grandes volúmenes de información derivados de biología molecular (la genómica, trascriptómica, proteómica, epigenómica, metabolómica, anormalidades cromosómicas, polimorfismos, mutaciones, deficiencias funcionales de etiología genética, expresiones génicas alteradas y biomarcadores), que junto con los datos clínicos provenientes de registros electrónicos, respaldan la toma de decisiones basadas en la evidencia y predicen los desenlaces (7,30,34,37).
De manera simultánea a esta avalancha de información, el cuidado primario en salud se ha vuelto más complejo debido a la multimorbilidad, el gran número de opciones terapéuticas, las múltiples escalas de estratificación del riesgo y el aumento de actividades de índole asistencial y administrativo inherentes al registro clínico y al proceso de atención segura (1,7,9,44).
Los desarrollos tecnológicos alcanzados, como la historia clínica electrónica, prometían agilizar el proceso de atención y liberar al médico de tareas no clínicas, sin embargo, en la práctica, los resultados han sido contrarios, generando inconformidad entre el personal médico y sobrecarga laboral. Esta percepción, la incertidumbre y confusión en su definición, propósito y potencial, han condicionado los bajos índices de aceptación e implementación de la inteligencia artificial, retrasando la posibilidad de generar un modelo de atención en medicina automatizado, de tipo predictivo, preventivo, personalizado y participativo (3,7,9,15-17,30,37,43).
En otras disciplinas, la inteligencia artificial cada día es más tangible y se ha expresado en múltiples recursos tecnológicos consumibles como Alexa en Amazon y Siri en Apple y se ha incorporado en dispositivos que los consumidores mantienen con ellos la mayoría del tiempo, como teléfonos inteligentes, relojes, entre otros. El área de la salud se ha quedado atrás en términos de reconocer el valor de los datos y la esperanza de alcanzar mejores desenlaces en la atención clínica se ha visto entorpecida por la baja eficiencia de la tecnología actual (15, 18, 26, 30, 37, 40, 43-45, 48).
Los procesos de atención relacionados con el cuidado de la salud, que se han optimizado con tecnologías de inteligencia artificial y el uso de la “Big Data”, con el objetivo de predecir desenlaces, aplicar medicina de precisión y salud poblacional, han mostrado mejorar el diagnóstico, el tratamiento y disminución en el error médico. La sugerencia de pruebas con alto impacto diagnóstico reduce la solicitud de ayudas poco útiles, además de mejorar la experiencia del paciente y minimizan el impacto financiero al optimizar el funcionamiento de las instituciones, pero esto requiere la compatibilidad de la IA con los procesos económicos y clínicos actuales (35-37).
¿Qué se ha definido como inteligencia artificial en la práctica clínica?
Existen diversas definiciones de inteligencia artificial. Por ejemplo, el Royal College of General Practicioners, lo ha definido como cualquier software con capacidad de decisión, desde algoritmos de programación basados en el “checking” dicotómico o árboles de decisiones, hasta soluciones más elaboradas que permiten cambios y adaptaciones automatizadas del software, o como la American Medical Association (AMA), que la define como “inteligencia humana aumentada” (2,3,7,15,30,32).En otro enfoque se ha considerado la inteligencia artificial como un conjunto de algoritmos que con el poder computacional y acceso a gran volumen de información (bases de datos), a través de modelos matemáticos identifica relaciones no lineales entre variables, lo cual se denomina analítica, con capacidad de realizar modificaciones o correcciones a los algoritmos como respuesta al hallazgo de un error, esto es entrenamiento/aprendizaje y mejoría en la exactitud y precisión de la capacidad de predicción o confianza (4,6,8,9).
La inteligencia artificial tiene un gran número de arquitecturas que combinan ciencias computacionales, estadística, capacidad de análisis de grandes volúmenes de datos, evaluación de combinación de decisiones, toma de decisiones, aprendizaje, adaptación, razonamiento, solución de problemas, contextualización y entendimiento del lenguaje natural; con base en su diseño y funcionalidad, se puede clasificar en aprendizaje de máquina o “Machine Learning”, “Deep Learning” o redes neurales, entre otras (1,4,6,8,9,5,20,30,33,34, 35).
Hay algoritmos no basados en inteligencia artificial o “sistemas expertos”, confinados a un tópico específico que toman los principios generales y los aplican, sin aprendizaje; las herramientas de inteligencia artificial toman los datos, encuentra las relaciones no lineales y establecen las reglas de predicción, aprenden, predicen y se corrigen (19,30,32).
En este artículo, según su utilidad y aplicabilidad, se ha divido en tres tipos:
- Inteligencia artificial estrecha (ANI – artificial narrow intelligence), diseñada para la realización de una tarea.
- Inteligencia artificial general (AGI - artificial general intelligence), que tiene la capacidad de dar contexto a su ambiente, también conocida como Inteligencia con nivel humano.
- Superinteligencia artificial, considerada como la capacidad de entendimiento y la toma de decisiones al nivel del humano más listo en cada área de habilidades científicas, sociales y “cultura general” (1,5).
Las capacidades de la inteligencia artificial en cualquier modalidad podrían aumentar el desempeño humano en un proceso “no-lineal”, como lo es la práctica clínica en el diagnóstico, análisis de “Small Data” (síntomas y signos individuales) y “Big Data” (bases de datos, guías) para la toma de decisiones en tiempo real, facilitando la comunicación con el paciente y su seguimiento (1,5,6,9). Para la práctica clínica actual la inteligencia artificial ideal es la estrecha (ANI), diseñada en enfocarse en tareas específicas (5,15). Los datos perdidos o de mala calidad influencian el entrenamiento, ejecución y validación del algoritmo, alterando la capacidad predictiva y por ende, la confianza en los resultados. Para que los datos sean útiles, deben estar en formatos susceptibles de análisis e interpretación (9,19).
La adopción de la historia clínica electrónica (EHR Electronic Health Record – EMR Electronic Medical Record) ha promovido la recopilación de datos a gran escala. La inteligencia artificial integrada al proceso permite la automatización de sistemas de captura, procesamiento y almacenamiento de los datos (demografía, síntomas, signos, resultados de ayudas diagnósticas) y ofrece la oportunidad de análisis de datos multivariado, dando soporte al razonamiento clínico en tiempo real (6,8,9,16,18, 30-37).
Una de las dificultades en el aprovechamiento de los datos es su formato en estos repositorios de información, pues son datos “no estructurados”, además diferentes instituciones y hospitales difieren en los formatos y así, no son útiles para los análisis estadísticos convencionales. Para convertir esta información en utilizable, se requiere de una conversión manual, por ejemplo, formatos de investigación o herramientas basadas en inteligencia artificial como algoritmos de procesamiento de lenguaje natural o NLP, individual o paralelo a otros algoritmos. Por otra parte, la confidencialidad del dato se ve comprometida, ya que no existen procesos estandarizados de intercambio ni de anonimización (18,19,33,35,36).
Se plantean ejemplos como la investigación del Dr. Choi en 2017, en la que usando los registros electrónicos de salud (EHR – Electronic Health Records, Historia Clínica Electrónica) como entrenamiento/aprendizaje, una herramienta de inteligencia artificial de tipo redes neurales, predijo la aparición de falla cardiaca superando la metodología usada para ese fin (10). La aplicación de “Big Data” en la salud es inevitable, dando paso a preguntas como: ¿Fue la implementación de la historia clínica electrónica la primera revolución digital?, ¿El uso de “Big Data” a través de la inteligencia artificial es la segunda revolución digital en medicina?, ¿Podremos convertir el “Big Data” en salud en conocimiento útil para los pacientes? (18,49).
La captura automatizada de los datos provenientes de “wearables”, se abre espacio en la atención de pacientes; actualmente uno de los campos de mayor desarrollo es la detección de fibrilación auricular, con una buena sensibilidad y especificidad, surgiendo como evidencia clase I en tamizaje de fibrilación auricular silente (10,11,13). Esta práctica se encuentra limitada por las características de los dispositivos (sensores), su calibración y el uso por parte del consumidor (1,4,5,23).
La integración de los datos médicos, de salud y los “omics” promete evaluar la heterogeneidad de los pacientes, facilitar la agrupación en fenotipos, entender la conexión entres genes, características humanas y enfermedades, dando paso a la medicina personalizada, inclusive el surgimiento del concepto de “gemelos digitales”, entidades que simularán con base en predicciones de inteligencia artificial los desenlaces clínicos derivados de una intervención (9,30,32,37).
En términos de predicción de eventos, la inteligencia artificial aprende del procesamiento de un gran volumen de los datos recogidos y se adapta según la nueva data, impactando en varios niveles, desde lo administrativo hasta lo asistencial, lo cual se ve reflejado en la experiencia de cuatro hospitales en París, que tomaron la información de ingresos, clima, días festivos y patrones de ocurrencia de la gripa durante 10 años y predijeron el número de consultas con 15 días de antelación, conduciendo a la contratación de personal extra cuando se esperaban más casos, obteniendo rapidez y calidad de la atención (20). Un segundo estudio mostró los beneficios en la construcción de modelos para la identificación de enfermedades subclínicas, como la enfermedad vascular periférica, generando modelos de clasificación y predicción más exactos (21).
La validación del funcionamiento de los algoritmos en términos de exactitud no es equivalente a la demostración de la eficacia clínica; validaciones y evaluación de reproducibilidad de los resultados en cohortes prospectivas, serán el paso para demostrar utilidad clínica. Hasta el momento los estudios acerca de la implementación de la inteligencia artificial en escenarios clínicos son limitados, enfocados en el desarrollo de algoritmos y validaciones usando cohortes retrospectivas (22,30,33,35).
Los médicos requieren contextualizar las sugerencias dadas por la inteligencia artificial, pero además participar en el diseño de las interfaces, ser críticos en los análisis estadísticos (construcción e interpretación); de lo contrario, empresas como Google, Facebook o biobancos de datos, por ejemplo, Kaggle Data Science Bowl, The Cancer Genome Atlas entre otros, abrumaran al clínico (20,33).
A nivel global, en los sistemas de salud se presenta una crisis con tres factores en común: escasez y burnout del personal médico, envejecimiento de la población con mayor expectativa de vida y mayor incidencia de complicaciones por enfermedad crónica (5). La medicina ha sido una combinación entre un modelo de negocios fallido con un incremento en los gastos, una mazcla de errores de diagnóstico y tratamiento, desperdicio de recursos, ineficiencias, inequidades y tiempos de oportunidad de atención prolongados (30).
Como respuesta al aumento en los costos de salud derivados del modelo actual de prestación de servicios, hay una tendencia de las compañías de seguros y los países a cambiar su tipo de pagos por evento, a planes que prioricen los desenlaces clínicos de los pacientes para tratar de aliviar la inequidad en la distribución del recurso (20,22,23).
La inteligencia artificial requiere humanos
La inteligencia artificial requiere humanos para la programación de los algoritmos y generación de modelos computacionales; la interpretación y contextualización de los resultados bioestadísticos y clínicos generados; la identificación de modelos débiles que generan resultados espurios con sesgos (6,15,33). En el contexto de la medicina, la interpretación y juicio clínico es una responsabilidad del médico, y las herramientas basadas en inteligencia artificial lograrán su potencial solo si están acopladas al trabajo clínico como parte del equipo y están validadas o certificadas (1,5,6,15,26,33).Se requiere una supervisión en el entrenamiento (de novo o por “transfer learning”), ejecución, validación, aplicación, evaluación y recalibración de los algoritmos, además de conocer las necesidades y objetivos del sector en el cual se implementarán para escoger el software adecuado (9,16). En la industria de la manufactura la automatización total falló. Aunque los robots no se cansan y son fuertes, no tienen la destreza, agilidad, ni flexibilidad mental de los humanos, lo que abrió el cambio hacia los “cobots”, un trabajo colaborativo entre humanos y robots (15).
Aplicando el trabajo colaborativo a la relación entre la inteligencia artificial y los profesionales de la salud, habrá una mejor distribución de funciones, el médico se preocupará más por las personas (empatía) y la herramienta por la velocidad, el acceso a la información, la captura automatizada de los datos a distancia (importación de registros clínicos previos y resultados), las necesidades desconocidas de los pacientes, el establecimiento de probabilidades, los pronósticos, la predicción de interacciones medicamentosas y la calidad de la historia clínica (15).
Los médicos de hoy se sienten incómodos con la incertidumbre, pues el avance de la tecnología y la ciencia crea el sofisma de la medicina como una ciencia exacta, sin embargo, no hay que olvidar que los instrumentos electrónicos no ofrecen la absoluta y decisiva verdad, y en inteligencia artificial los resultados de los algoritmos no son por completo reproducibles, por lo tanto, deben ser supervisados por médicos, aunque inevitablemente se contaminen de la subjetividad de la cual hemos tratado de escapar (14,15).
Hay un cambio sociológico en curso ligado a la irrupción de las tecnologías en la salud de los pacientes. Estas tecnologías progresan rápidamente, pero no necesariamente mejoran per se, los desenlaces clínicos de los pacientes, si no se cuenta con la orientación y el acompañamiento del personal de salud, quien debe retroalimentarse de forma constante en el uso de los dispositivos, internet, uso de apps y cualquier tipo de innovación. El toque humano y la inteligencia emocional deben provenir del personal de salud entrenado para una adecuada aplicación de la inteligencia artificial, que entienda y contextualice las predicciones y sugerencias (23,33,48).
Limitaciones
El desarrollo de las herramientas basadas en inteligencia artificial en el campo del cuidado de la salud se ha enfocado en la tecnología y la necesidad comercial para encontrar un mercado, más que en las necesidades de los profesionales de la salud, sistemas de salud, comunidades y pacientes (15,37,48). La inteligencia artificial no es la panacea, pues cada elemento y parámetro no puede ser trasladado a un lenguaje de programación, por eso la inteligencia artificial no es la solución a todos los retos del cuidado de la salud, pero si constituye una herramienta que ayuda a mejorar diagnósticos, decisiones terapéuticas, disminuyendo de errores médicos, mejorando desenlaces en su papel como asistente cognoscitivo y facilitador de procesos. La inteligencia artificial no es “la bala de plata” y podrían presentarse efectos no anticipados que impliquen un aumento en la carga laboral del médico u obstaculizar procesos administrativos como los pagos y reembolsos (1,5,6,30).Los administradores de las instituciones de salud deben evaluar y mitigar las disrupciones en el flujo de trabajo cuando se introduce alguna herramienta basada en inteligencia artificial, superar la falta de entendimiento de la tecnología, de estrategias claras de integración, el bajo entrenamiento en el uso de las mismas, la incompatibilidad de la tecnología con la infraestructura existente y la carencia de datos de buena calidad para el entrenamiento de los algoritmos con datos locales (6,34,35).
La cantidad, calidad y fuente del dato, impactan dramáticamente en el desarrollo de los modelos de inteligencia artificial, por lo cual la capacidad para recolectar, almacenar y aprender es crucial para el desarrollo de la misma (35). Los registros médicos electrónicos o historia clínica electrónica no son interoperables, es decir, las plataformas y lenguajes de programación no permiten un intercambio de información fluido, generando una limitación en el uso de décadas de información almacenada en los servidores (4,15,17,18,20).
Los datos de baja calidad alteran el procesamiento de la información por correlaciones múltiples erradas que generan estimaciones inestables denominadas “overfit” o sobreentrenamiento. Se disminuye su impacto a través de modelos de prueba y validación independiente (9,15,18,23,26,33,35). Los algoritmos son realizados en poblaciones específicas, lo que limita la replicación en otras poblaciones (validez externa) y su replicación (validez interna), por lo cual su aplicación general se ha visto limitada, especialmente en las minorías étnicas (1,4,5,9,26).
Las predicciones de desenlaces clínicos relevantes en casos con patrones infrecuentes o en entidades atípicas, en las que no se tenga un entrenamiento robusto estarán comprometidas y requieren un entrenamiento adicional antes de la validación (17,33,35,37). La mayoría de los algoritmos no están diseñados para inferir causalidad, sino para predicción, teniendo en cuenta que los factores predictores no son causas, sin embargo, recientemente la fenotipificación profunda proveniente de la medicina molecular y analizada a través de los algoritmos, ha permitido la construcción de una red de modelos causales de enfermedad a nivel de la fisiopatología molecular y celular (19,37).
Las capacidades analíticas de la inteligencia artificial que soportan la medicina de precisión se enfrentan a enfermedades crónicas con un compromiso multiorgánico y fenotipos heterogéneos, eventos agudos o agudizaciones erráticas, diferentes comportamientos en el tiempo sin un patrón evidente en un paciente y cursos clínicos diferentes entre pacientes, dificultando la traslación del Big Data a la tecnología de inteligencia artificial y a la aplicación clínica (4,30,32,33,34,35). El desarrollo de herramientas basadas en inteligencia artificial, requirieron costosos equipos de cómputo con procesadores de múltiples núcleos o supercomputadoras, sin embargo, el avance en las capacidades de los computadores de escritorio, la optimización en la ejecución de los algoritmos y el internet han permitido que estas soluciones se puedan diseñar o ejecutar desde la nube (9,17,34). ¿Por qué la resistencia a la implementación de la inteligencia artificial? La evolución de las tecnologías médicas ha implicado rápidos cambios de concepto en el término “dispositivos médicos”, incorporando términos novedosos como algoritmos, teléfonos inteligentes o el internet de las cosas, provoca una disrupción en la práctica clínica del personal no entrenado ni preparado para estos cambios, además de la generación de grandes volúmenes de información (guías, consensos, estudios aleatorizados) (9,17,22,23).
La adopción de la historia clínica electrónica, en muchos casos ha aumentado la carga de trabajo, inclusive convirtiéndose en factor que aumenta la incidencia del síndrome de Burnout. Adicionalmente, el miedo del médico a ser reemplazado, aunque el grueso de la literatura médica muestra la inteligencia artificial como herramientas que aumentan las capacidades humanas, ha generado una evidente resistencia a su implementación (7,43,45) y miedo a las repercusiones legales y de responsabilidad por aceptar o rechazar las recomendaciones del algoritmo, pues hay una ausencia en las regulaciones en términos legales de responsabilidad (7,33,43), experiencias como Watson Oncology donde las recomendaciones eran erradas, probablemente porque la data no provenía de la vida real (30).
La “cultura digital” en salud se ha definido como la disrupción de los desarrollos tecnológicos en términos de proveer datos digitales y objetivos a personal de la salud y pacientes, llevando el paradigma de la relación médico paciente a un plano de decisiones compartidas e informadas, un cuidado de la salud basado en el valor y en las capacidades humanas aumentadas como por ejemplo el juicio clínico, un cuidado de salud inevitablemente cada vez más dependiente de la tecnología y la digitalización, el surgimiento del “epatient”, como lo menciona el Dr. Ferguson, empoderado y siendo parte en la toma de decisiones sobre su salud y su vida, en medio de un personal no entrenado (23,24,30,33). En los currículos no hay políticas que lo reflejen y en consecuencia los médicos no están preparados para afrontar los retos de la digitalización en salud (4,6,15,23).
La ética y la inteligencia artificial
La inteligencia artificial como cualquier herramienta humana tiene el potencial de ayudar o dañar, no es buena ni mala y su impacto depende de cómo se use (27,30). La inteligencia artificial implica unos riesgos de daño al paciente, generados por errores de resultados ocasionados por un entrenamiento con datos deficientes, errores de validación que desvían al sobrediagnóstico o infradiagnóstico, o la presencia de minorías étnicas que pueden no estar representadas adecuadamente en el desarrollo y validación de los algoritmos (1,6,34,35,36). ¿Qué implica las sugerencias y la toma de decisiones por parte de sistemas de inteligencia artificial? ¿Cuáles son las consecuencias morales, sociales y legales de las acciones y decisiones de la inteligencia artificial? ¿Cómo se pueden controlar estas herramientas una vez desarrollen sus capacidades de aprendizaje? (26,32).Una vez las capacidades para la toma de las decisiones crezcan, es necesario repensar y redefinir los conceptos de responsabilidad, que debe ir más allá de características adicionales de los algoritmos o el botón de apagado del sistema, debe existir una “ética por el diseño”, una ética integrada al comportamiento autónomo del algoritmo, una “ética en el diseño” o regulación en los métodos de ingeniería y una “ética para el diseño” o códigos de conducta, procesos estandarizados y certificados que aseguren la integridad del modelo para lograr que los algoritmos y sistemas que estén en nuestras vidas sean transparentes, justos y aceptables, disminuyendo el efecto de “caja negra” (26,30).
Se requiere que el razonamiento de los algoritmos tome en cuenta los valores sociales, morales y éticos del sitio donde se implementará. En las áreas, regiones o países con bajos ingresos su población tendría un acceso limitado a estas tecnologías, siendo sujeto de inequidad. La carencia de acceso puede hacer que los pacientes recurran a terapias ineficaces o “charlatanería en internet”. No obstante, en poblaciones rurales la implementación de dispositivos de telemonitoreo pueden generar una opción de acceso a los servicios de salud (5,23,26,30).
El procesamiento de la información a través de algoritmos debe cumplir los principios éticos, como lo menciona la normatividad federal para introducción de las nuevas tecnologías biomédicas, Reporte Belmont (26), que es extrapolable a la inteligencia artificial hasta el momento, basado en los principios de respeto a las personas, beneficencia y justicia y que puede incluir otros parámetros éticos como no maleficencia, libertad, autonomía, confidencialidad y transparencia, con énfasis en prevenir la formación de monopolios u oligopolios de la información a través de “compartir ético”, es decir, que los repositorios de los datos sean accesibles en el contexto de la confidencialidad de los datos personales y clínicos con estrategias para prevenir la intrusión o “hackeo” de los datos (1,15,23,27,28-30).
Las herramientas basadas en inteligencia artificial se deben focalizar en sistemas con alto rendimiento, exactos, confiables, efectivos y entendibles, conservar muestras representativas que les permitan mantener la validez al algoritmo, superando obstáculos como datos perdidos o tamaños muestrales pequeños que alteren la implementación de las herramientas de soporte para toma de decisiones, por ello, la implementación debe llevarse a cabo con precaución; el desarrollo de los algoritmos debe ser explicable y entendible, a pesar de la complejidad con las redes neurales, con el objetivo de promover la confiabilidad (26,30,33).
Nuevas promesas de la Inteligencia Artificial
Herramientas de ayuda para diligenciamiento eficiente de los registros clínicos, con requerimientos de inversión de tiempo mínimos para el diligenciamiento automatizado de la historia clínica y carga administrativa, disminuyendo la probabilidad del síndrome de burnout en el personal sanitario y el miedo a la deshumanización (7,33). El miedo a ser reemplazado y mejorar la aceptación de la inteligencia artificial puede ser minimizado si el diseño de los estudios futuros en lugar de comparar las soluciones de inteligencia artificial versus las humanas, compare los resultados de humanos que usan inteligencia artificial versus resultados de aquellos que no la usan, dando paso al concepto de la inteligencia artificial como un complemento a las habilidades humanas (7,30,33). El avance de la tecnología, la informática y la programación, permitirán una mayor disponibilidad de datos para un entrenamiento que sea acumulable y la generación de un ciclo de retroalimentación positiva, consistente en más datos, más precisión y exactitud, mejor producto, más usuarios, (15,30,32,33).El cambio de una medicina jerárquica a un nuevo estatus quo, con pacientes empoderados, con acceso a la información a través de la tecnología y un seguimiento de su condición clínica a través del telemonitoreo, promoverá un cuidado integral y no una fragmentación del paciente en especialidades, la creación de una verdadera red de trabajo basada en la ética y el uso consensuado de los registros clínicos, telemedicina e inclusive las redes sociales, dando paso al surgimiento de la “e-health” y la “m-health” (23,34,35).
Una historia clínica interoperable, con la generación de datos estructurados, ágil y eficiente, que permita el uso eficaz, efectivo y eficiente de los datos (10- 20,30,32-36). La sinergia entre inteligencia humana y algoritmos de inteligencia artificial serán la clave del desarrollo y sincronización de los diferentes sistemas de registro médico electrónico, mejorando la eficiencia, la seguridad y el acceso a los servicios de salud (33-35). Se ha identificado que la historia clínica electrónica es uno de los desencadenantes más importantes de burnout en el personal médico y se estima que generó pérdidas entre 90 y 140 billones de dólares para 2015 en tiempo perdido por año (equivalente a 532.000.000.000.000 pesos colombianos con una cambio de $3.800 pesos por dólar). Los médicos utilizan entre el 34 y el 55% de su día laboral creando notas, el 78% del tiempo de la realización de las historias clínicas electrónicas corresponde a escribirlas y revisarlas, además interfieren en el contacto con el paciente, la calidad de la atención y la mala calidad de la documentación clínica (43,44). El estudio del Dr. Young y colaboradores en 2018, muestra como el clínico emplea más tiempo diligenciando la historia, que en el contacto visual con el paciente (45); por lo anterior, empresas como Google, Microsoft, Nuance y Epic trabajan en soluciones basadas en inteligencia artificial para el reconocimiento de voz, algunas de ellas generando la nota clínica de manera automatizada, mientras la herramienta captura la información en tiempo real provee recomendaciones basadas en la evidencia usando la información actual y el entrenamiento previo, transforma unos datos no estructurados (historia clínica no lineal, fragmentada, multicapas) y genera un documento con una narrativa lógica, susceptible de ser manejado, además, logra integrar información de otras fuentes al registro, como los laboratorios y las radiografías (40-44).
La inteligencia artificial generará modelos predictivos basados en “Big Data” provenientes de los registros clínicos electrónicos: Kaiser Permanente asociado a KenSci da los primeros pasos para estratificar pacientes con falla cardiaca y predecir hospitalización, readmisión y mortalidad; Ochsner Health System asociado con Epic predice el deterioro clínico o Banner Health y Base Health’s AI predicen y previenen en 100.000 miembros las visitas a urgencias (43). El registro clínico electrónico dejará de ser un repositorio pasivo de información y se convertirá en un asistente digital inteligente. ¿La inteligencia artificial convertirá la relación médico paciente en una relación más humana? (44).
Algunas empresas han desarrollado “AI doctors”, que son herramientas basadas en inteligencia artificial que asesoran sobre síntomas comunes y leves; más que reemplazar médicos, al hacer parte del equipo de salud, logran optimizar los servicios, dejando espacio para las consultas de casos más complejos y mejoran el manejo de las agendas. “Digital Coach” es una oportunidad en las enfermedades crónicas, pues a través de aplicaciones, ofrece asesoría y seguimiento, para el logro de las metas terapéuticas (43).
La inteligencia artificial ofrece las herramientas para evitar distracciones (como labores administrativas) que puedan poner en riesgo la seguridad del paciente, disminuir la carga de teclear, redactar el registro clínico, la sobrecarga de información proveniente del paciente; brindar acceso a la mejor evidencia en tiempo real y realizar tamizajes “en segundo plano” a través de la exploración consensuada de los registros electrónicos previos (43).
Conclusiones
La inteligencia artificial es una herramienta tecnológica creada por los humanos, que ofrece gran diversidad de alternativas y utilidades para la optimización de los procesos de atención en salud. La incertidumbre siempre existirá en el campo de la salud, pues la medicina no solo es una ciencia, sino un arte. A pesar de una implementación lenta de la inteligencia artificial en el campo de la salud, aparentemente se ha llegado a un punto de no retorno y será una herramienta para aumentar las capacidades humanas, no para reemplazarlas. La experiencia previa con la historia clínica electrónica mostró, que, si no participamos en el diseño y planeación de herramientas de inteligencia artificial, seremos víctimas de un Frankenstein electrónico, construido de retazos y sin una utilidad clara.En la práctica clínica, el papel del médico en el “ritual de la atención” y en la relación médico paciente, en la que se establece la confianza, la empatía y la humanidad, es irremplazable. La inteligencia artificial está presente para soporte, optimización y priorización del paciente. La humanidad depende del médico, no de las máquinas. La ética médica aplica para cualquier tipo de proceso involucrado en la relación con el paciente, incluyendo la inteligencia artificial, que no puede desconocer la normatividad actual.
La práctica de la medicina interna y la atención primaria con la ayuda de la inteligencia artificial migrarán a una tendencia más preventiva, de diagnóstico temprano y optimización terapéutica, minimizando el error diagnóstico y terapéutico y mejorando la calidad de vida, el bienestar personal, social, económico y laboral. La inteligencia artificial depende de la calidad de los datos con que se alimenten las bases de datos y esta depende de la calidad de la historia clínica electrónica. Hay preguntas por responder ¿Los costos de atención aumentarán? ¿Los médicos serán más eficientes? ¿El hardware requerido será costoso? ¿Será una inversión viable? ¿La conexión a internet en zonas apartadas funcionará? ¿Qué pasará con el efecto “black box”?
Este caso es ficticio pero basado en la experiencia clínica del autor, es reflejo de los retos diarios en el consultorio, en el contexto de un sistema de salud con problemas de oportunidad en la atención especializada; el abordaje inadecuado implica un riesgo de eventos cardiovasculares, progresión a diálisis, u otras complicaciones que generan discapacidad, muerte y aumento de costos para el sistema de salud, siendo la aplicación de la inteligencia artificial, como se describió, una fuente de transformación y mejoramiento.
Referencias
1.
Artificial Intelligence and Primary Care [Internet] The Royal College
of General Practitioners;2019 [consultado 20 septiembre de 2021].
Disponible en: https://www.rcgp.org.uk/-/media/Files/CIRC/artificial-intelligence-and-primary-care-jan-2019.ashx?la=en
2. Augmented intelligence in health care [Internet]. American Medical Association; 2021 [consultado 20 septiembre 2021]. Disponible en:
https://www.ama-assn.org/system/files/2019-08/ai-2018-board-policy-summary.pdf
3. Augmented intelligence in health care [Internet]. American Medical Association; 2021 [consultado 20 septiembre 2021]. Disponible en:
https://www.fsmb.org/siteassets/artificial-intelligence/pdfs/ama-ai-advocacy.pdf
4. Miller D., Brown E. Artificial Intelligence in Medical Practice: The Question to Answer? Am J Med 2018;131(2):129-133.
5. Meskó B, Hetényi G., Gyorffy Z., Will artificial intelligence solve the human resource crisis in healthcare? BMC Health Serv Res. 2018;18(1):545
6. Yu H., Beam A., Kohane I. Artificial intelligence in healthcare. Nat Biomed Eng. 2018;2(2):719–731.
7. Briganti G., Le Moine O., Artificial Intelligence in Medicine: Today and Tomorrow. Front Med (Lausanne). 2020;7:27.
8. Jiang F., Jiang Y., Zhi H., Dong Y., Li H., Ma S, et al. Artificial intelligence in healthcare: past, present and future. Stroke Vasc Neurol. 2017;2(4):230-243.
9. Krittanawong C., Johnson K., Rosenson R., Wang Z., Aydar M., Baber U, et al. Deep learning for cardiovascular medicine: a practical primer. Eur Heart J. 2019;40(25):2058–2073.
10. Choi E, Schuetz A, Stewart WF, Sun J. Using recurrent neural network models for early detection of heart failure onset. J Am Med Inform Assoc 2017;24(2):361–370.
11. Tison GH, Sanchez JM, Ballinger B, Singh A, Olgin JE, Pletcher MJ, Vittinghoff E, et al. Passive detection of atrial fibrillation using a commercially available smartwatch. JAMA Cardiol. 2018;3(5):409–416.
12. Nagaran V., Lee SL., Robertus JL., Nienaber CA., Trayanova NA., Ernst S,. Artificial Intelligence in the Diagnosis an Management and Arrythmias, Eur Heart J. 2021;42(38):3904-3916.
13. Hindricks G., Potpara T., Dagres N., Arbelo E., Bax J., Blomström-Lundqvist C, et al. 2020 ESC Guidelines for the Diagnosis and Mangement of Atrial Fibrillation Developed in Collaboration with The European Association for Cardio-Thoracic Surgery (EACTS): The Task Force for The Diagnosis and Management of Atrial Fibrillation of the European Society of Cardiology (ESC) Developed with the Special Contribution of The European Heart Rhythm Association (EHRA) of the ESC.- Eur Heart J. 2021;42(5):373-498.
14. Jauhar S., The Demise of the Physical Exam. N Engl J Med. 2006;354(6):548-551.
15. Mistry P., Artificial intelligence in primary care. Br J Gen Pract. 2019;69(686):422-423.
16. Beam A., Kohan I. Translating Artificial Intelligence Into Clinical Care. JAMA. 2016;316(22):2368-9.
17. Dwivedi A.,Deivedi SS., Tariq MR., Qiu X., Hong S., Xin Y. Scope of Artificial Intelligence in Medicine. J Res Med Dent Sc. 2020;8(3):137-140.
18. Murdoch T., Detsky A. The Inevitable Application of Big Data to Health Care. JAMA. 2013;309(13):1351-2.
19. Obermeyer Z., Emanuel E. Predicting the Future — Big Data, Machine Learning and Clinical Medicine. N Engl J Med. 2016;375(13):1216-9.
20. Ricco J., Guetarni F., Holh P. Learning from Artificial Intelligence and Big Data in Health Care. Eur J Vasc Endovasc Surg. 2020;59(6):868-869.
21. Ross EG, Shah NH, Dalman RL, Nead KT, Cooke JP, Leeper NJ. The use of machine learning for the identification of peripheral artery disease and future mortality risk. J Vasc Surg. 2016;64(5):1515-22.
22. Yin J., Ngiam K., Teo H. Role of Artificial Intelligence Applications in Real-Life Clinical Practice: Systematic Review. J Med Internet Res. 2021;23(4):e25759).
23. Meskó B., Drobni Z., Bényei É., Gergely B., Györffy Z. Digital health is a cultural transformation of traditional healthcare. MHealth. 2017;3:38.
24. Ferguson T. (doctom.com) [Internet]. Doctom.com. 2021. [consultado 20 septiembre de 2021]. Disponible en: http://www.doctom.com/
25. Eysenbach G. What is e-health? J Med Internet Res. 2001;3(2):E20.
26. Dignum V. Ethics in artificial intelligence: introduction to the special issue. Ethics and Information Technology.2018;20(1):1–3.
27. Read the Belmont Report. [Internet]. HHS.gov. 2021 [consultado 20 septiembre de 2021]. Disponible en:
https://www.hhs.gov/ohrp/regulations-and-policy/belmont-report/read-the-belmont-report/index.html
28. The Good Clinical Practice [Internet]Gco.nidatraining.org. 2021 [consultado 14 octubre de 2021] . Disponible en: https://gcp.nidatraining.org
29. Protecting Human Research Participants | PHRP Training [Internet]. Phrptraining.com 2021 [consultado 20 septiembre de 2021]. Disponible en: https://phrptraining.com
30. Topol E., High-performance medicine: the convergence of human and artificial intelligence. Nat Med. 2019;25(1):44–56
31. Garcia-Vidal C., Sanjuan G., Puerta-Alcalde P., Moreno-García E., Soriano A. Artificial intelligence to support clinical decision-making processes. EBioMedicine. 2019;46:27–29.
32. Noorbakhsh-Sabet N., Zand R., Zhang Y., Abedi V. Artificial Intelligence Transforms the Future Artificial Intelligence Transforms the Future of Health Care. Am J Med. 2019;132(7):795−801.
33. Dzobo k., Adotey S., Thomford N., Dzobo W. Integrating Artificial and Human Intelligence: A Partnership for Responsible Innovation in Biomedical Engineering and Medicine. OMICS.2020;24(5):247-263.
34. Yoav M.,Ronit B. Introduction to artificial intelligence in medicine. Minim Invasive Ther Allied Technol. 28:(2):73-81.
35. Chen, M., Decary M.,Artificial intelligence in healthcare: An essential guide for health leaders. Healthc Manage Forum. 2020;33(1):10-18.
36. Mehta N., Devarakonda M. Machine learning, natural language programming, and electronic health records: The next step in the artificial intelligence journey? J Allergy Clin Immunol. 2018;141(6):2019-21.
37. Seyhan A., Carini C. Are innovation and new technologies in precision medicine paving a new era in patients centric care? J Transl Med. 2019;17(1):114.
38. Chi E.,Chi G., Tsui C., Jiang., Jarr K., Kulkarni C, et al. Development and Validation of an Artificial Intelligence System to Optimize Clinical Review of Patient Records. JAMA Netw Open. 2021;4(7):e2117391.
39. Beveridge M., Fox J., Automatic generation of spoken dialogue from medical plans and ontologies. J Biomed Inform.2006 39(5):482-499.
40. Migneault J., Farzanfar R., Wright JA., Friedman R. How to write health dialog for a talking computer. J Biomed Inform. 2006;39(5):468–481.
41. Fox J., Cognitive systems at the point of care: The CREDO program. J Biomed Inform. 2017;68:83–95.
42. Smith T. 10 Ways Health Care Could Transform Primary Care. [Internet]. American Medical Association. 2021. [consultado 14 octubre de 2021]. Disponible en:
https://www.ama-assn.org/practice-management/digital/10-ways-health-care-ai-could-transform-primary-care
43. Lin S., Mahoney M., Sinsky C., Ten Ways Artificial Intelligence Will Transform Primary Care. J Gen Intern Med. 2019;34(8):1626–30.
44. Lin S., Shanfelt T., Asch S. Reimagining Clinical Documentation With Artificial Intelligence. Mayo Clin Proc. 2018;93(5):563-565.
45. Young R.,Burge S., Kumar K., Wilson J., Ortiz D. A TimeMotion Study of Primary Care Physicians’ Work in the Electronic Health Record Era. Fam Med. 2018;50(2):91-9.
46. Wong J., Murray M., Zhou L., ToH, Using machine learning to identify health outcomes from electronic health record data. Curr Epidemiol Rep. 2018;5(4):331–342.
47. Xiao C., Choi E., Sun J., Opportunities and challenges in developing deep learning models using electronic health records data: a systematic review. J Am Med Inform Assoc. 2018;25(10):1419–1428.
48. Fogel A., Kvedar J. Artificial intelligence powers digital medicine. NPJ Digital Med. 20181:5.
49. Garg S., Williams N., Ip A., Dicker A. Clinical Integration of Digital Solutions inHealth Care: An Overview of the Current Landscape of Digital Technologies in Cancer Care. JCO Clin Cancer Inform. 2018;2:1-9.
Recibido: 12 de Noviembre, 2021
Aceptado: 22 de Noviembre, 2021
Correspondencia:
Andrés Eduardo Rico-Carrillo