Resúmen
El nuevo coronavirus SARS-CoV-2 también conocido como 2019-nCoV ocasiona la COVID-19, continúa siendo desconocido para el mundo de la salud por los cambios genómicos, fenotípicos del virus y los cambios fisiopatológicos relacionados con la respuesta proinflamatoria y procoagulante que genera en el huésped y su alta mortalidad. En la literatura médica, el aumento de las especies reactivas del oxígeno o radicales libres de oxígeno se asocia con la respuesta inflamatoria secundaria a la infección por virus y bacterias con el consecuente daño celular, tisular y sistémico en el huésped. La acción prooxidativa celular del virus SARS-CoV-2 hace que se pierda la hemostasia redox, que aumenten las especies reactivas del oxígeno y se genere estrés oxidativo con pérdida de la función del sistema antioxidante. Conocer la relación que tienen las especies reactivas del oxígeno y el sistema de defensa antioxidante con la respuesta inflamatoria del SARS-CoV-2, ayudará a entender e interpretar mejor la COVID-19.Se realizó una revisión sistemática de la literatura médica a través de las bases de datos de PubMed y Medline con los términos: Infección por SARS-CoV-2, especies reactivas del oxígeno en la COVID-19, respuesta inflamatoria en la COVID-19.
Esta revisión mostró relación de la infección, inflamación, coagulación con el aumento de las especies reactivas del oxígeno y la pérdida del sistema de defensa antioxidante en la respuesta inflamatoria al SARS-CoV-2.
Palabras clave: Especies reactivas del oxígeno; estrés oxidativo; SARS-Cov-2; citoquinas
..............
1 Médico especialista en Medicina Interna; subespecialista en Cuidado Intensivo. Maestría en Gestión de Trasplantes. Maestría en Bioética. Miembro correspondiente Academia Nacional de Medicina, Capítulo Atlántico. Coordinador sección de Bioética y gestión de trasplantes AMCI 2020.
¿Are reactive oxygen species and the antioxidant defense system related to the inflammatory response of SARS-CoV-2?
Abstract
The new coronavirus SARS-CoV-2 also known as 2019-nCoV causes COVID-19. Which continues to be unknown to the health world due to the genomic and phenotypic changes of the virus and the pathophysiological changes related to the proinflammatory and procoagulant response that it generates in the host and its high mortality. The increase in reactive oxygen species or oxygen free radicals is reported in the medical literature, associated with the inflammatory response secondary to infection by viruses and bacteria with the consequent cellular, tissue and systemic damage in the host. The cellular pro-oxidative action of the SARS-CoV-2 virus causes the loss of redox hemostasis, the increase in reactive oxygen species and the generation of oxidative stress with loss of the function of the antioxidant system. Knowing the relationship that reactive oxygen species and the antioxidant defense system have with the inflammatory response of SARSCoV-2 will help us better understand and interpret COVID-19.A systematic review of the medical literature was carried out through the PubMed and Midline databases with the terms: SARS-CoV-2 infection. Reactive oxygen species in COVID-19. Inflammatory response in COVID-19.
This review showed a relationship of infection, inflation, coagulation with the increase in reactive oxygen species and the loss of the antioxidant defense system with the inflammatory response of SARS-CoV-2.
Keywords: : Reactive oxygen species; oxidative stress; SARS-Cov-2; Cytokines.
Introducción
Los seres humanos poseen un sistema de oxidación/ reducción (homeostasia redox) necesario para mantener el equilibrio interno entre el nivel de especies reactivas del oxígeno y el sistema antioxidante. Cuando la capacidad de defensa antioxidante del organismo disminuye por la acción prooxidante de un virus o bacteria, aumentan las especies reactivas del oxígeno ocasionando daño celular y sistémico, lo que se conoce como estrés oxidativo, que ocasiona el daño a lípidos, ADN, proteínas y otras macromoléculas de la membrana celular. Para reducir las especies reactivas del oxígeno y sus respectivos radicales libres de oxígeno, en condiciones normales el organismo utiliza antioxidantes enzimáticos y no enzimáticos endógenos como el glutatión peroxidasa (GPX. enzimático) y el glutatión reducido (GSH- no enzimático), para neutralizar las sustancias reactivas del oxígeno y transformarlas en productos no tóxicos para el organismo.El nuevo coronavirus SARS-CoV-2 también conocido como 2019-nCoV es el virus que causa la COVID-19. Se detectó en diciembre de 2019 en la ciudad china de Wuhan, en la provincia de Hubei. Como todos los virus de RNA, el SARS-CoV-2 tiene acción prooxidativa celular que activa por esta vía la respuesta inflamatoria secundaria a la infección, generando especies reactivas del oxígeno que ayudan a perpetuar el daño por el estrés oxidativo y la pérdida del sistema regulador antioxidante.
La justificación de este trabajo se orienta a conocer si existe relación entre las especies reactivas del oxígeno, el estrés oxidativo y la respuesta inflamatoria ocasionada por el SARS-CoV-2, y si la respuesta inflamatoria sistémica leve a severa causada por este virus es perpetuada directamente por el virus o por la pérdida de la función del sistema antioxidante en el paciente. El conocimiento y comprensión de las bases celulares, moleculares y biológicas del SARS-CoV-2 permitirá plantear la disminución de los efectos patogénicos de la COVID-19 (1).
El objetivo es revisar de forma sistemática la literatura médica y determinar si las especies reactivas del oxígeno y el sistema de defensa antioxidante influyen en la respuesta inflamatoria que ocasiona el SARS- CoV-2. El orden metodológico que se empleará para esta revisión descriptiva será:
Introducción y objetivo. Planteamiento del problema. Marco teórico. Localización, selección y evaluación de estudios primarios. Revisión de las preguntas planteadas. Desarrollo, comentario y Conclusiones.
Planteamiento del problema
El SARS-CoV-2 es un virus prooxidante que ocasiona
una serie de cambios fisiopatológicos, asociados con
la edad, comorbilidades (diabetes, obesidad, hipertensión) y el estado
inmunológico del huésped. Genera
una sobreexpresión de citocinas proinflamatorias que
ocasiona la llamada tormenta de citocinas y alteraciones sistémicas
graves como el síndrome de dificultad
respiratoria aguda (SDRA) y cambios en la microcirculación, endotelio
capilar, coagulación y muerte.
Estudios relacionados con el SARS-CoV-2 comienzan
a aparecer en la literatura médica, y mencionan la relación de la
COVID-19 con la pérdida de la homeostasia redox, presencia de especies
reactivas del oxígeno,
estrés oxidativo, e insuficiencia del sistema antioxidante. Con estos
datos se plantea si existe asociación
entre el nuevo coronavirus SARS-CoV-2 y su estímulo
prooxidativo celular con la respuesta inflamatoria del
huésped. Para dar respuesta a este planteamiento, se
estructuraron tres preguntas de investigación y búsqueda bibliográfica
elaboradas con la estrategia PICO (Paciente, Intervención, Comparación,
Resultado).
Pregunta No.1
¿En el SARS-COV-2 es importante conocer el mecanismo de ingreso a la célula para comprender la patogenia de la COVID-19?
Pregunta No.2
¿El SARS-CoV-2 genera una acción prooxidante que
perpetúa el daño celular por la producción excesiva de
especies reactivas del oxígeno y el estrés oxidativo en
la COVID-19?
Pregunta No.3
¿En la COVID-19 la tormenta de citocinas es determinante en la respuesta inflamatoria ocasionada por el
virus SARS-CoV-2?
Hipótesis
Desde que el SARS-CoV-2 ingresa al organismo genera una acción
prooxidativa en la célula. El sistema de
defensa antioxidante es insuficiente para contrarrestar
la producción de especies reactivas del oxígeno, iniciándose una
reacción en cadena, con generación de estrés oxidativo y apoptosis celular, contribuyendo a
la respuesta inflamatoria y procoagulante de la COVID-19.
Fundamento de la hipótesis
La acción fisiológica del sistema antioxidante esta conservada y
presente en toda persona antes de ser invadida por un virus o una
bacteria y es mantenida por la
hemostasia Redox. Al ser invadido por el virus SARSCoV-2 se genera una
respuesta sistémica con pérdida
del equilibrio de oxidación/reducción del huésped,
generándose sustancias reactivas del oxígeno, estrés
oxidativo, daño y muerte celular. Si todo esto es lo que
está sucediendo con el SARS-CoV-2 se hace necesario
una intervención relacionada a minimizar el daño.
Marco teórico
Conocer los mecanismos de generación de las especies
reactivas del oxígeno o radicales libres del oxígeno, las
especies reactivas del nitrógeno o radicales libres del
nitrógeno, el estrés oxidativo y la pérdida de la función
del sistema de defensa antioxidante, ayudará a una
mejor comprensión de la COVID-19 y sus variaciones
fisiopatológicas, y de la cascada de eventos sistémicos
que se generan.
En 1954 los investigadores Rebeca Gerschman y Daniel L. Gilbert propusieron por primera vez que “los radicales libres” (RL) son moléculas que se producen en condiciones normales cuando nuestras células crean energía a partir de los alimentos y el oxígeno (2-3). Pero eran agentes tóxicos generadores de enfermedades cuando estaban expuestos a infecciones microbianas, virales, ejercicio intenso o contaminantes ambientales o toxinas o radiación (4). Los radicales libres son átomos o moléculas que tienen electrones no apareados, generalmente inestables y altamente reactivos (5). El término “radical libre” a mediados de siglo XX se fue identificando gradualmente con los términos Especies Reactivas del Oxígeno (ROS) que se refiere a los radicales libres generados por el oxígeno y Especies Reactivas del Nitrógeno (RNS) que se refiere a los radicales libres generados por el nitrógeno (siglas en inglés para “reactive oxygen species (ROS) y para “reactive nitrogen species” (RNS)). En el organismo encontramos dos tipos de radicales libres: de oxígeno y de nitrógeno (6).Se usarán las siglas en español ERO para Especies Reactivas del Oxígeno, y ERN para las Especies Reactivas del Nitrógeno.
Las ERO la conforman los radicales libres Anión superóxido (O2-), Hidroxilo (OH), radicales peroxilo (ROO) y peróxido de hidrógeno (H2O2). Las ERN la conforman los radicales libres Dióxido de nitrógeno, óxido nítrico (NO), peroxinitrito (OONO) y el superóxido (7). El óxido nítrico (NO) es un radical libre gaseoso que ha resultado ser un importante mediador en la reactividad del músculo liso y los vasos sanguíneos en el endotelio capilar. Una sustancia mucho más tóxica que el propio NO es el peroxinitrito (OONO) que se descompone en el radical libre de oxígeno hidroxilo (OH). (8-9)
Las ERO y ERN pueden iniciar la peroxidación de lípidos, causar roturas de la cadena de ADN y oxidar de forma indiscriminada prácticamente todas las moléculas en las membranas biológicas y los tejidos, lo que resulta en daño. Sin embargo, debido a que el cuerpo es capaz de eliminar ERO y ERN hasta cierto punto de inflexión, estas especies reactivas no son necesariamente una amenaza para el cuerpo en condiciones fisiológicas. Pero son perjudiciales cuando originan un “estrés oxidativo” o un “estrés nitrosativo (10). El estrés oxidativo/ nitrosativo representa el desequilibrio en la producción y eliminación de especies reactivas de oxígeno y nitrógeno (radicales libres de oxígeno y nitrógeno), así como una disminución de la producción de antioxidantes endógenos enzimáticos y no enzimáticos(11)
Las fuentes generadoras de ERO o radicales libres del oxígeno en condiciones de normalidad son la respiración mitocondrial o celular. Se conoce que el 90% del total del oxígeno inhalado se consume en la mitocondria y alrededor del 2 % del oxígeno reducido se transforma en radicales libres del oxigeno. El oxígeno (O2) utilizado por el organismo humano es reducido a agua por acción del complejo citocromo-oxidasa (citocromo A+a3) de la cadena respiratoria mitocondrial. Al elevarse la concentración fisiológica de radicales libres del oxígeno como el anión superóxido (O2-), peróxido de hidrogeno (H2O2), Hidroxilo (OH), se pueden generar importantes alteraciones fisiológicas y funcionales (12). Los leucocitos polimorfonucleares son otra fuente de ERO o radicales libres de oxígeno. Estos constituyen una fuente importante cuando se activan por diversas proteínas que actúan específicamente sobre ellos (complemento, interleucinas); esta situación se da particularmente en los procesos infecciosos (13). Los leucocitos poseen en sus membranas la enzima NADPH (Nicotiamida-Adenina Dinucleótido fosfato) que cataliza la transferencia de un electrón de O2 con la formación del radical libre de oxígeno el superóxido (O2-), el cual es rápidamente convertido en otro radical libre de oxígeno, el peróxido de hidrógeno (H2O2). Esta situación se da particularmente en los procesos inflamatorios e infecciosos virales o bacterianos (14). El metabolismo del ácido araquidónico, por la vía de la ciclooxigenasa y de la lipooxigenasa dan lugar a la formación de prostaglandinas, tromboxanos, leucotrienos y otros derivados, todos los cuales son promotores de la formación de ERO o radicales libres de oxígeno. Otras fuentes generadoras de ERO son la catálisis por liberación de hierro y cobre y las acciones enzimáticas (15). Cualquier desequilibrio entre las fuentes generadoras de radicales libres de oxígeno o nitrógeno con la pérdida de la capacidad del sistema antioxidante ocasiona el estrés oxidativo, que es la incapacidad de reparar el daño resultante (16-17).
El sistema antioxidante está constituido por un grupo de sustancias antioxidantes, enzimáticas y no enzimáticas. Las sustancias antioxidantes enzimáticas, endógenas son la superóxido dismutasa (SOD), la cual pertenece a una familia de metaloenzimas que cataliza la dismutación del radical libre de oxígeno el anión superóxido (O2-) originando peróxido de hidrógeno y oxígeno (O2- a H2O2 y O2). (18). La catalasa (CAT) que es una enzima tetramérica que cataliza la dismutación del radical libre de oxígeno el peróxido de hidrógeno (H2O2) en agua y oxígeno (H2O2 a H2O y O2) y el glutatión peroxidasa (GPx) que cataliza la dismutación del radical libre de oxígeno el peróxido de hidrogeno (H2O2) o de otros peróxidos orgánicos a agua (H2O) (19) . Estas acciones fisiológicas de las sustancias antioxidantes enzimáticas endógenas pueden controlar el estrés oxidativo mientras la producción de las radicales libres de oxígeno no supere a esta barrera antioxidante endógena y natural (20). Dentro de las sustancias antioxidantes no enzimáticas se encuentran el glutatión (GSH), un tripéptido proteínico compuesto por tres aminoácidos: cisteína, glicina y glutamato; se trata del principal antioxidante de las células, es ubicuo y ayuda a protegerlas de las especies reactivas del oxígeno y de los peróxidos. En las células, el glutatión se encuentra principalmente en su estado reducido (GSH) y, en mucha menor proporción, en su estado oxidado (GSSG). El ácido ascórbico, una vitamina hidrosoluble que el humano no puede sintetizar por lo que debe adquirirla a través de la dieta. El α-tocoferol, una vitamina liposoluble que debe ser ingerida a través de la dieta, ya que no se sintetiza endógenamente (21). Los antioxidantes no enzimáticos están presentes en la dieta ingerida por los seres vivos, sobre todo en las frutas y verduras (22-23). Las defensas del sistema antioxidante, incluidos los componentes enzimáticos y no enzimáticos, protegen contra las especies reactivas del oxígeno (ERO) en forma natural y fisiológica (24).
Localización, selección y evaluación
de estudios primarios
Se realizó una revisión sistemática en ask MEDLINE
herramienta de búsqueda para encontrar evidencia
actual en MEDLINE / PubMed. http://askmedline.nlm.nih.gov/ask/pico.php.
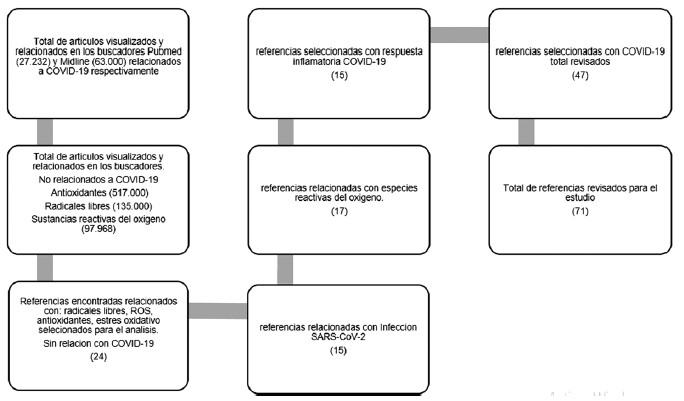
Se visualizaron un total de 27.232 artículos en Pubmed relacionados al COVID-19. En Medline (Medical Literature Analysis and Retrieval System Online) se visualizaron 63.000 artículos relacionados con COVID-19. Los artículos no COVID-19 visualizados relacionados con la búsqueda Radicales libres fueron 135.000, con especies reactivas del oxígeno 97.968, y con antioxidantes 517.000.
Al utilizar la estrategia y proceso de búsqueda PICO para los artículos COVID-19, los términos y criterios de búsqueda utilizados, fueron: Infección por SARSCoV-2. Especies reactivas de oxígeno y COVID-19. Respuesta inflamatoria COVID-19.
Los artículos seleccionados para la revisión que llenaron los criterios de búsqueda (artículos de revisión, estudios observacionales, estudios retrospectivos, metaanálisis) fueron: para infección por SARS-CoV-2 15 artículos; Especies reactivas del Oxígeno y COVID-19, 17 artículos; Respuesta inflamatoria COVID-19, 15 artículos. En total entraron a la revisión 47 artículos COVID-19 y 24 artículos de los considerados no COVID-19 pero sí relacionados con las búsquedas: Radicales libres, sustancias reactivas del oxígeno, considerados como fuente primaria relacionada al objetivo del estudio. En total se revisaron 71 referencias.
Los títulos, autores, comentarios y referencias están relacionados en las tablas respectivas, a las preguntas (PICO) planteadas. Con los numerales Tabla No. 2,3,4, se dan respuestas a cada pregunta de la revisión hecha.
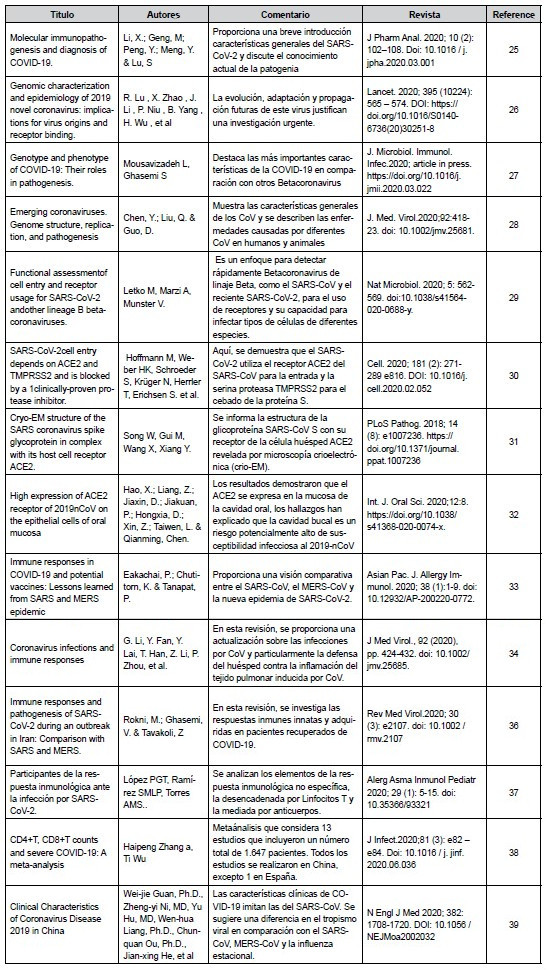
Tabla 1. Selección de artículos relacionados al Sars-Cov-2 e infección, especies reactivas del oxígeno, inflamación en la enfermedad Covid-19.
Infección por el SARS-CoV-2.
Pregunta No.1
¿En el SARS-COV-2 es importante conocer el mecanismo de ingreso a la célula para comprender la patogenia de la COVID-19?
La secuenciación del genoma del virus de cinco pacientes con neumonía hospitalizados del 18 al 29 de diciembre de 2019 en Wuhan, China, reveló la presencia de una cepa de β-CoV, previamente desconocida en todos ellos. Este nuevo β-CoV aislado mostró un 88 % de identidad con la secuencia de dos coronavirus; el síndrome respiratorio agudo (SARS-CoV) derivado de murciélagos, bat-SL-CoVZC45 y bat-SL-CoVZXC21. Y aproximadamente un 50 % de identidad con la secuencia del síndrome respiratorio agudo de oriente medio (MERS-CoV). El nuevo β-CoV fue denominado entonces “SARS-CoV-2” por la Comisión Internacional de Clasificación de Virus(25).
Los primeros informes reportados sobre la vigilancia genómica de las muestras clínicas de nueve pacientes con neumonía viral en Wuhan, China, mostraron al análisis filogenético secuenciado que el virus pertenece al subgénero Sarbecovirus 2019-nCoV. Fue más similar a las dos cepas de coronavirus derivadas de murciélagos que a las cepas de los humanos infectados por otros coronavirus, y a la cepa del virus SARS-CoV que causó el brote en 2003. Epidemiológicamente ocho de los nueve pacientes del estudio tenían un historial de exposición al mercado de mariscos de Huanan en Wuhan, lo que sugiere que podrían haber estado en contacto con la fuente de infección en el mercado. Sin embargo, un paciente nunca había visitado el mercado, aunque se había alojado en un hotel cercano antes del inicio de su enfermedad (26).
Los Betacoronavirus humanos (SARS-CoV-2, SARSCoV y MERS-CoV) tienen muchas similitudes, pero también tienen diferencias en su estructura genómica y fenotípica que pueden influir en su patogenia. Se ha reportado en la literatura que genéticamente, SARSCoV-2 es menos similar al SARS-CoV en alrededor del 79 % y al MERS-CoV en alrededor del 50 %. Además, que la disposición de las proteínas entre los Betacoronavirus, la nucleocápside (N), la proteína de la envoltura (E) y la proteína de la membrana (M) son diferentes, lo que explica los comportamientos y manifestaciones clínicas entre estos virus (27).
En la disposición de las cuatro proteínas estructurales esenciales para el ensamblaje del virión y la infección de CoV, la proteína S (superficie) forma “los picos” en la superficie viral, que son responsables de la unión a los receptores del huésped a través de la Enzima Convertidora de Angiotensina-2 (ACE-2). La proteína M (de membrana) tiene tres dominios transmembrana y da forma a los viriones, promueve la curvatura de la membrana y se une a la nucleocápside. La proteína E (de envoltura o pericapside) juega un papel en el ensamblaje y la liberación del virus, y participa en la patogénesis viral. La proteína N (nucleocápside) contiene dos dominios, los cuales pueden unirse al genoma del ARN del virus a través de diferentes mecanismos (28).
El receptor del huésped conocido para los Betacoronavirus es la ACE-2. Todos los CoV codifican una glicoproteína de superficie (S) pico, que se une a este receptor del huésped para mediar la entrada viral. Para los Betacoronavirus, una sola región de la proteína de pico llamada dominio de unión al receptor (RBD), media la interacción con el receptor de la célula huésped. Después de unirse al receptor, una proteína endotelial, serina-tipo 2 de la proteasa de la transmembrana proteína (TMPRSS2) del huésped, libera un péptido de fusión a la glicoproteína de superficie (S) pico, lo que facilita la entrada del virus (29).
El SARS-CoV-2 utiliza el receptor ACE-2 al igual que el SARS-CoV para la entrada a la célula y la serina proteasa TMPRSS2 para el cebado de la proteína S (glicoproteína de superficie) (30). Un estudio realizado con microscopia electrónica (crio-EM) con el SARSCoV mostró cómo la estructura de la glicoproteína de superficie (S) de este virus establece un complejo con el receptor ACE-2 de la célula huésped, observándose que sólo un dominio de unión al receptor (RBD) de la glicoproteína S trimérica se une. Este resultado proporcionó conocimiento para entender el mecanismo de la entrada del virus SARS-CoV a la célula (31). En cuanto al receptor ACE-2 se ha publicado que la mucosa de la cavidad oral podía expresar el ACE-2, siendo más alta la expresión en lengua que en otros sitios orales. Otras células humanas que expresan ACE-2 en general, se encuentran en pulmón, intestino, corazón y riñón. La expresión de ACE-2 en el pulmón se concentra en una pequeña población de células alveolares de tipo II (AT2) (32-33). Una vez ingresa el virus al organismo inicia su respuesta inmunológica con los macrófagos, los cuales presentan antígenos CoV a las células T. Este proceso conduce a la activación y diferenciación de las células T, y a la producción de citocinas asociadas con los diferentes subconjuntos de células T. La producción continua de estos mediadores debido a la persistencia viral tiene un efecto negativo sobre la activación de las células T, natural Killer (NK) y T CD8. Sin embargo, las células T CD8 producen mediadores muy eficaces para eliminar CoV (34).
La inmunidad humoral es esencial para el control de la fase persistente de la infección por CoV, a través del sistema del complemento, debido a que proporciona un mecanismo de detección y respuesta al sistema inmunológico para que responda a antígenos extraños. El complemento C3a y C5a tienen potentes propiedades proinflamatorias y puede desencadenar el reclutamiento de células inflamatorias y la activación de neutrófilos (35).
En un estudio que evaluó la inmunidad innata, se observó que la linfopenia causada por la infección viral del SARS - CoV -2 puede ocurrir por tres mecanismos: 1) por reducción de la producción de linfocitos o la linfopoyesis alterada, 2) por apoptosis y destrucción de linfocitos, y 3) por redistribución de los linfocitos con unión al endotelio vascular (fenómeno similar a la marginación de los neutrófilos). Estos mecanismos pueden conducir a una disminución de los linfocitos circulantes y explican la linfopenia en los pacientes con la COVID-19 (36).
Los anticuerpos IgM y IgG y su respuesta fueron evaluados a través de un estudio en 173 pacientes con infección por SARS-CoV-2. Se observó que la tasa de seroconversión y los niveles de anticuerpos aumentaron rápidamente durante las primeras dos semanas. La tasa de seropositividad acumulada alcanzó 50 % en el día 11 y 100 % en el día 39 de los anticuerpos totales, IgM e IgG respectivamente (p < 0,05). Se concluyó que algunos pacientes con ARN indetectable por prueba de RT- PCR en la primera semana, podrían ser examinados a través de la prueba de anticuerpos (37).
En cuanto a los linfocitos CD4 +T y los CD8 + T (inmunidad adaptativa) que juegan un papel antiviral significativo, en un metaanálisis en el que se consideraron 13 estudios que incluyeron un número total de 1.647 pacientes con la COVID-19, se distinguieron grupos graves y no graves, grupos de UCI y no UCI, grupos de fallecidos y supervivientes. Los datos de los recuentos de CD4 + T, CD8 + T se redujeron significativamente en el grupo de COVID-19 grave en comparación con el grupo no grave. Los T CD4 + y los T CD8 + muestran que juegan un papel vital en el mantenimiento de la función inmunológica y la eliminación viral (38-39) (Tabla 2).
Tabla 2. Infecciónpor el Sars-CoV-2.
Pregunta No.1. ¿En el SARS-COV-2 es importante conocer el mecanismo de
ingreso a la célula para comprender la patogenia
de la COVID-19?
Especies reactivas del oxígeno
(ero) y el SARS-CoV-2
Pregunta No. 2
¿El SARS-CoV-2 genera una acción prooxidante que perpetúa el daño celular por la producción de especies reactivas del oxígeno y estrés oxidativo en la COVID-19?
Las especies reactivas del oxígeno (ERO) o radicales libres del oxígeno son “mediadores de la respuesta inflamatoria que activan la señalización celular, aumentando la producción y liberación de citocinas proinflamatorias, manteniendo así la respuesta inflamatoria” (40). El estrés oxidativo es el resultado de la disminución de los niveles de antioxidantes enzimáticos y no enzimáticos que perpetúan el daño celular a nivel del ADN, lípidos y proteínas de la membrana celular (41).
En la COVID-19 parece que el estrés oxidativo ocasionado por el aumento de los radicales libres de oxígeno, es decir, de las especies reactivas del oxígeno (ERO) juega un papel en la patogénesis de la tormenta de citocinas, en el mecanismo de coagulación y la exacerbación de la hipoxia. Esta evidencia indica una importante participación del estrés oxidativo en la patogénesis de la infección viral SARS-CoV-2 y la lesión tisular, incluida la disfunción mitocondrial (42). Las mitocondrias son el centro de la homeostasis oxidativa celular; al perder su equilibrio son generadoras de ERO. El estado inflamatorio y oxidativo elevado puede llevar a la disfunción y el estrés oxidativo mitocondrial, que puede contribuir a la disbiosis o desbalance del equilibrio de la microbiota intestinal, alimentando la respuesta inflamatoria y oxidativa. (43). El papel de las especies reactivas del oxígeno (ERO) en la patogénesis de las infecciones virales, ha sido un área de investigación que ha cobrado importancia desde los años 90s con la infección por el virus de la inmunodeficiencia humana (VIH) (44). La atención de los estudios se ha centrado en tres clases de virus: Los virus de ARN, los virus de ADN y los retrovirus, con especial atención a los virus de la influenza, el virus de la hepatitis B y el VIH como ejemplos representativos de estas tres clases de virus (45). En el virus VIH se ha estudiado el efecto sobre la activación de células fagocíticas en la liberación de las ERO y citocinas proinflamatorias y el factor de necrosis tumoral. También se ha estudiado el efecto en la inhibición de antioxidantes enzimáticos como superóxido dismutasa (SOD) y aumento de prooxidantes tales como óxido nítrico (NO) y el estado redox de la célula (46). Los virus respiratorios, entre ellos el SARS-CoV-2, inducen una formación de ERO o radicales libres de oxígeno de forma desregulada como resultado del aumento del reclutamiento de células inflamatorias en el sitio de infección. Además, las infecciones virales alteran los mecanismos antioxidantes generando una acción prooxidante, lo que conduce a un estado oxidativo-antioxidante desequilibrado y el consiguiente daño celular oxidativo (47).
El SARS-Cov-2, al desencadenar la infección viral hace que el sistema inmune innato (macrófagos, dendritas, monocitos) detecte la infección mediante receptores de reconocimiento de patrones (PRRs), receptores que identifican moléculas intrínsecas presentes en los patógenos. Entre los PRRs conocidos en la actualidad se incluyen principalmente los receptores tipo toll (TLR), que activan una respuesta prooxidante de los macrófagos, que da lugar a la activación del TNF-α y del NADPH- oxidasa en los leucocitos, y que a su vez median la producción de especies reactivas del oxígeno (ERO) (48).
En los pacientes con la COVID-19 el estado hiperinflamatorio denominado “tormenta de citocinas”, que implica importantes perturbaciones sistémicas en el huésped, tales como la desregulación del hierro que se manifiesta como hiperferritinemia asociada con la gravedad de la enfermedad, induce la producción de especies reactivas de oxígeno (ERO) y promueve el estrés oxidativo (49).
La óxido nítrico-sintasa es una enzima inducible en los neutrófilos, que al ser activada produce radicales libres de oxígeno capaces de combinarse con el óxido nítrico (NO) para dar sustancias mucho más tóxicas que el propio NO, tales como el peroxinitrito (OONO), aumentando así el estrés nitrosativo. La neutrofilia genera un exceso de especies reactivas del oxígeno (ERO) que exacerba la respuesta inmunopatológica del huésped, resultando en una enfermedad más severa. La alta proporción de neutrófilos observada en pacientes críticamente enfermos con la COVID-19, promueve una cascada de eventos biológicos que impulsa la respuesta patológica e induce daño tisular, trombosis y disfunción de los glóbulos rojos, lo que contribuye a la gravedad de la COVID-19. La acción deletérea de las ERO sobre las funciones de las células pulmonares como de los glóbulos rojos (RBC) puede verse como un contribuyente importante a la insuficiencia respiratoria hipóxica, observada en los casos más graves de la COVID-19, siendo su efecto dañino sobre las células endoteliales y epiteliales alveolares, con endotelitis procoagulativa, y exceso de ERO (50).
La producción abrumadora de especies reactivas del oxígeno o radicales libres de oxígeno en las células pulmonares resulta en estrés oxidativo y conduce a la COVID-19 severa, aumentando la formación de trampas extracelulares de neutrófilos (NET) dentro de los microvasos (51). La agregación intravascular de NET conduce a una rápida oclusión de los vasos afectados, alterando la microcirculación y generando daño orgánico. Los granulocitos neutrófilos están fuertemente activados y adoptan el llamado fenotipo de baja densidad, propenso a formar NET espontáneamente. La histopatología de los pulmones y otros órganos de pacientes con la COVID-19 ha mostrado congestión de numerosos microvasos por NET agregados y asociados con daño endotelial por radicales libres del nitrógeno como el óxido nítrico (NO) y el estrés nitrosativo (52).
Recientemente se ha propuesto que la COVID-19 es una enfermedad endotelial. De hecho, el virus SARSCoV-2 se une a la enzima convertidora de angiotensina tipo 2 (ACE-2) que se expresa en las células endoteliales. La ACE-2 podría estar implicada también en la producción de especies reactivas de oxígeno y de nitrógeno, causado por la disfunción endotelial debida al daño viral y asociada al estrés nitrosativo. En consecuencia, el estrés oxidativo/nitrosativo podría preparar estas células para adquirir un fenotipo protrombótico y proinflamatorio, lo que predispondría a los pacientes a eventos tromboembólicos y vasculíticos y a la coagulopatía intravascular diseminada (CID) (53).
El retículo endoplásmico (RE) liso o rugoso (contiene los ribosomas) es otro generador de especies reactivas del oxígeno (ERO). El estrés oxidativo del retículo endoplásmico activa señales proinflamatorias y formación de inflamasomas, lo que sugiere que el estrés del RE ejerce efectos inmunogénicos y puede ser activado por exceso de lípidos o citocinas proinflamatorias (54- 55). Las especies reactivas del oxígeno (ERO) o radicales libres de oxígeno son perjudiciales para las células; conducen a la muerte celular programada (PCD) a altas concentraciones. No obstante, a bajas concentraciones las ERO o radicales libres de oxígeno pueden actuar como moléculas de señalización en una variedad de procesos celulares fisiológicos (56) (Tabla 3).
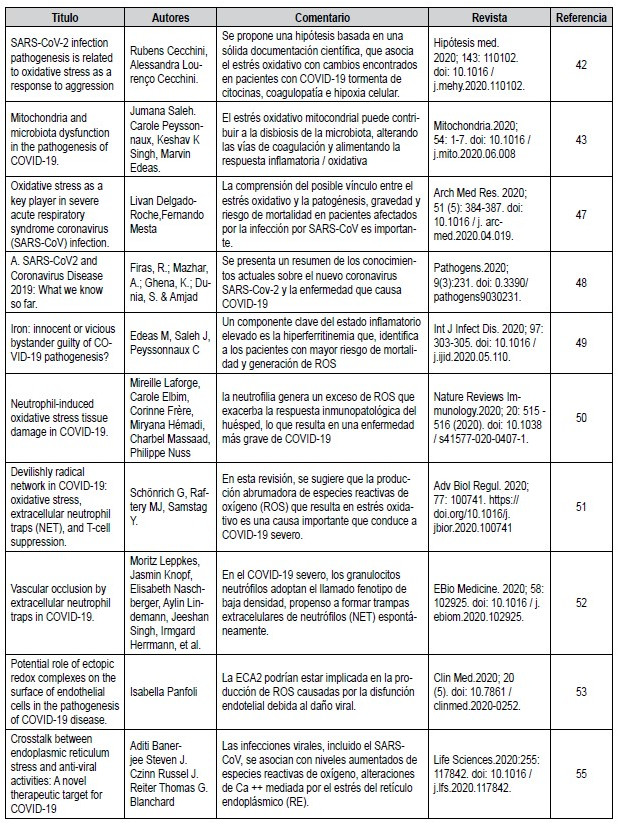
Tabla 3. Especies reactivas del oxigeno (ero) y el sars-cov2
Pregunta No. 2 ¿El SARS-CoV-2 genera una acción prooxidante que
perpetúan el daño celular por la producción de especies
reactivas del oxígeno y el estrés oxidativo en el enfermo COVID-19?
Respuesta inflamatoria en
sars-cov-2.
Pregunta No. 3
¿En la enfermedad COVI-19, la tormenta de citoquinas es determinante en la respuesta inflamatoria ocasionada por el virus SARS-CoV-2?
La infección-inflamación es la parte esencial de una respuesta inmunitaria eficaz. Es difícil eliminar las infecciones con éxito, sin inflamación. La respuesta inflamatoria comienza con un reconocimiento inicial del patógeno. Luego, los patógenos median en el reclutamiento de células inmunes, lo cual elimina los patógenos y finalmente conduce a la reparación del tejido y la restauración de la homeostasia. El SARS-CoV-2 induce infección e inflamación generando respuestas de citocinas excesivas y prolongadas en algunos individuos infectados, lo que se conoce como tormenta de citocinas, causa del SDRA y disfunción multiorgánica, que conduce al deterioro fisiológico y la muerte. (57).
Existe una amplia comunicación cruzada entre la coagulación y la inflamación, por lo que la activación de un sistema puede amplificar la activación del otro, y ambos generar daño tisular o incluso fallo multiorgánico. El Factor tisular (TF) es el nexo entre la coagulación y la inflamación, lo que proporciona un desencadenante para el inicio de la respuesta del huésped a la lesión por invasión del patógeno (58). Una relación de coagulación y la inflamación lo muestra un estudio retrospectivo con 183 pacientes con neumonía por el nuevo coronavirus (NCP). Los pacientes que no sobrevivieron revelaron niveles significativamente más altos de dímero D y producto de degradación de fibrina (FDP), con mayor tiempo de protrombina y tiempo de tromboplastina parcial activada, en comparación con los que sobrevivieron (p <0,05). El 71,4 % de los no sobrevivientes y el 0,6 % de los sobrevivientes cumplieron los criterios de coagulación intravascular diseminada durante su estancia hospitalaria, lo cual muestra que el dímero D y la FDP estuvieron marcadamente elevados y asociados en las muertes con NCP (59). Otro estudio de cohorte retrospectiva encontró que la edad avanzada, niveles de dímero D mayores de 1 μg / ml y una puntuación SOFA más alta al ingreso se asociaron con mayores probabilidades de muerte intrahospitalaria. Además, los niveles elevados de IL-6 en sangre, troponina I cardíaca de alta sensibilidad y lactato deshidrogenasa y linfopenia, se observaron con mayor frecuencia en la enfermedad grave por la COVID-19 (60). En los casos severos de la COVID-19 los niveles del dímero D están elevados y otros indicadores de coagulación como el tiempo de protombina y fibrinógeno se ven afectados. Se ha sugerido que el aumento de los niveles séricos de estos marcadores refleja un estado de hipercoagulabilidad que indican un mal pronóstico en la COVID-19. Estos biomarcadores inflamatorios y de coagulación muestran la relación estrecha entre infección-inflamación e infección-coagulación. La respuesta inflamatoria sobreactivada se asocia con la hipercoagulabilidad e infiltración excesiva de células inflamatorias del tejido pulmonar, llevando a lesión pulmonar que agrava la COVID-19 (61).
Las citocinas proinflamatorias, incluidas IL-2, IFN-γ, IL-6, pueden promover un estado de hipercoagulabilidad a favor de la formación de trombos, mientras que las citocinas antiinflamatorias, IL-10, realizan actividades anticoagulantes que previenen eventos trombóticos vasculares. En el caso de la COVID-19 grave, la liberación excesiva de citocinas proinflamatorias puede contribuir a la activación de la cascada de coagulación. La trombina, esencial en la cascada de la coagulación, no solo media la formación del coágulo de sangre al convertir el fibrinógeno en fibrina, sino que también puede actuar sobre los receptores activados para amplificar la inflamación (62). Las respuestas inmunitarias desreguladas en la COVID-19 podrían conducir al virus a provocar una respuesta inflamatoria sobreactivada y una liberación excesiva de citocinas, favoreciendo la relación infeccióninflamación-coagulación (63). Durante la infección por SARS-CoV y MERS-CoV la respuesta inmune del huésped y la producción sobreexpresada de citocinas inflamatorias, conocida como tormenta de citocinas, se correlaciona con la gravedad de la enfermedad y el mal pronóstico (64). En pacientes con SARS-CoV-2 se ha logrado demostrar, a través de un estudio de análisis transcriptómicos (expresión de genes transcritos en una célula) que la expresión de un gran número de citocinas, incluidas las citocinas proinflamatorias, están significativamente elevadas en muestras de BALF (lavado broncoalveolar) en pacientes con la COVID-19, en comparación con sus controles. También se observó un aumento de la transcripción de los respectivos receptores de quimocinas (65). Se cree que con el SARS-Cov la infección viral suele causar alteraciones masivas en el transcriptoma del huésped, que conducen a un metabolismo aberrante de la célula del huésped y a una respuesta inmune no modulada, ideal para la replicación viral (66). Los pacientes que sobreviven a esta respuesta inmune aberrante y excesiva, presentan daño pulmonar y fibrosis a largo plazo, que provoca discapacidad funcional con una reducción de la calidad de vida (67).
El diagnóstico y manejo de la tormenta de citocinas son clínicamente desafiantes y controvertidas debido a la falta de un tratamiento probado. Se han utilizado como estrategias terapéuticas inmunomoduladoras el trasplante intravenoso de células madre mesenquimales (CMM), que poseen una potente función inmunomoduladora (68); fármacos como el Inhibidor del receptor de IL-6 (anti-IL6R) tocilizumab, que reduce la respuesta inflamatoria y reactantes de fase aguda de la inflamación (69-70); ensayos in vitro que han mostrado que el SARS-CoV-2 tiene mayor sensibilidad a interferón de Tipo I (IFN-I); se ha observado que pacientes con infección leve/moderada por SARS-CoV-2 se asocian con una potente respuesta de IFN-I (71) (Tabla 4).
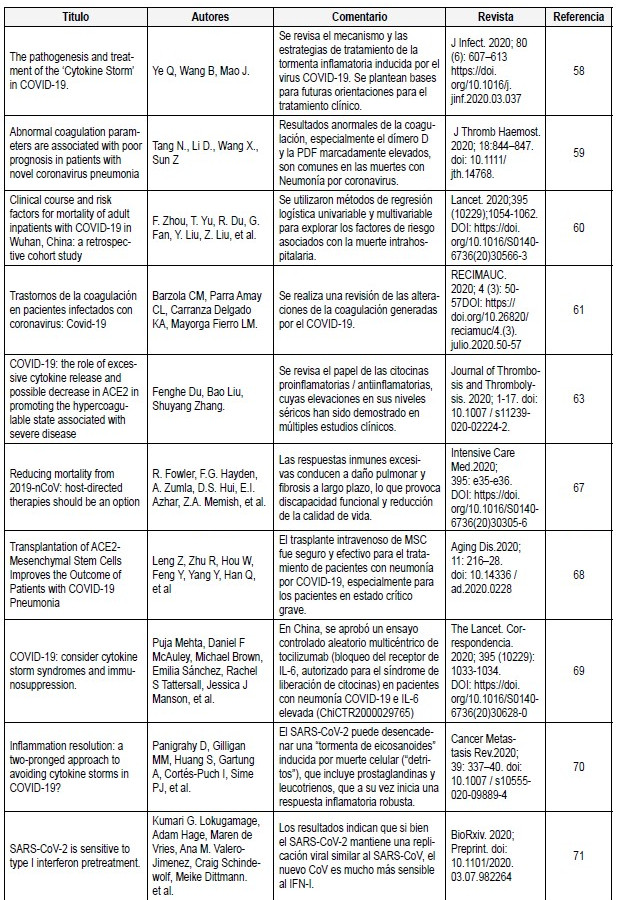
Tabla 4. Respuesta inflamatoria en SARS-CoV-2.
Pregunta No. 3
¿En la enfermedad COVID-19 la tormenta de citoquinas es determinante en
la respuesta inflamatoria ocasionada por el virus
SARS-CoV-2?
Comentario
La enfermedad COVID-19 generada por el nuevo coronavirus el SARS-CoV-2
de la familia de los Betacoronavirus, tiene algunas similitudes con el
SARS-CoV
y el MERS-CoV; son virus zoonóticos (se transmiten
de animales a humanos), periodo de incubación y mecanismo de
trasmisión.
De acuerdo con el comportamiento del genoma del virus, el comportamiento inmunológico del huésped, el ingreso del virus a la célula y la carga viral, se puede empezar a entender las variaciones en la respuesta clínica de cada paciente.
Las características clínicas de la COVID-19 que imitan las del SARS-CoV, en lo reportado muestra que la fiebre y la tos son los síntomas dominantes y los síntomas gastrointestinales son poco comunes, lo que sugiere una diferencia en el tropismo viral en comparación con el SARS-CoV, MERS-CoV y la influenza estacional.
El SARS.CoV-2 tiene similitud con SARS-CoV, MERS-CoV en la forma como se expresa en las células humanas con receptores ACE2 (Enzima Convertidora de Angiotensina-2) a través del dominio de unión del receptor de la proteína “S”.
Las investigaciones de la respuesta inmunológica de los coronavirus SARS-CoV y MERS-CoV han aportado -para el entendimiento de la respuesta inmune en la infección por el SARS-CoV-2- que los tres virus tienen respuesta inflamatoria con expresión de citocinas, siendo más explosiva y sobreactiva en el SARS-CoV-2, generando una tormenta de citoquinas desregulada y asociada al daño pulmonar. En el SARS-CoV, el MERS-CoV y el SARS-CoV-2, el órgano blanco de afectación principal es el pulmón, generando el síndrome de dificultad respiratoria aguda (SDRA).
El SARS-CoV-2 genera la COVID-19 grave con sepsis, disfunción multiorgánica, choque y muerte. Ha mostrado ser más agresiva y letal que el SARS-CoV y el MERS-CoV.
Los Betacoronavirus SARS-CoV, MERS-CoV y otros virus de RNA y el SARS-CoV-2 tienen un efecto prooxidativo celular con la consecuente producción de especies reactivas del oxígeno o radicales libres del oxígeno, estrés oxidativo, pérdida del sistema de regulación antioxidante, y acción proinflamatoria y procoagulante.
Conclusión
Los procesos inmunológicos, infecciosos, de inflamación y de
coagulación en la COVID-19 asociados con
la producción de ERO o radicales libres de oxígeno,
ayudan a comprender y entender el nivel de gravedad,
la asociación con la respuesta proinflamatoria y procoagulante, el
estrés oxidativo y la perpetuación del
daño ocasionado por SARS-CoV-2. Actualmente se
asocia con la tormenta de citoquinas y con la presencia
de especies reactivas del oxígeno y el estrés oxidativo
en pacientes críticos con la COVID-19.
La actual pandemia provocada por la COVID-19 representa un buen ejemplo de infección vírica asociada con una acción prooxidativa celular, infección, inflamación, coagulación con aumento de especies reactivas del oxígeno, estrés oxidativo y pérdida del sistema antioxidante, como coadyuvante de la enfermedad. Aún no se puede determinar si la acumulación y aumento de radicales libres o de especies reactivas del oxígeno son la causa o la consecuencia de la perpetuación del daño ocasionado con el SARS CoV-2. Debido a que no se cuenta con una cuantificación cualitativa de radicales libres de oxígeno ni de nitrógeno, de niveles de antioxidantes enzimático o no enzimáticos que permitan hacer hipótesis y generar conclusiones, esta revisión descriptiva muestra que, las especies reactivas del oxígeno, el estrés oxidativo y la defensa antioxidante son relevantes para tener en cuenta en la respuesta inflamatoria generada por el SARS-Cov-2.
Conflicto de interés
Declaro no tener ningún tipo de conflicto de interés en
esta presentación.
Financiación
Declaro no haber tenido ningún tipo de financiación
para este escrito.Referencias
1. Dae-Gyun A., Hye-Jin S., Mi-Hwa K., Sunhee L., Hae-Soo K., Jinjong M., et al.. Current Status of Epidemiology, Diagnosis, Therapeutics, and Vaccines for Novel Coronavirus Disease 2019 (COVID-19). J. Microbiol. Biotechnol. 2020;30(3):313-24.
2. Gerschman R., Gilbert D., Nye
S., Dwyer P., Fenn W., Oxigen poisoning
and X-Irradiation. A
mechanism in common. Science. 1954;119(3097):623-6.
3. Moran JF, James EK, Rubio MC,
Sarath G, Klucas RV, Becana M.
Functional Characterization and Expression of
a Cytosolic Iron-Superoxide Dismutase from Cow- pea (Vigna unguiculata) Root Nodules. Plant
Physiol. 2003;(133):773-782.
4.Piña-Garza E., Radicales Libres Beneficios y problemas (simposios). Gaceta Médica de México. [Internet].1996 [consultado 08 de mayo de 2021];132(2):183-203. Disponible en:
https://www.anmm.org.mx/bgmm/1864_2007/1996- 132-2-183-203.pdf
5. Finkel T, Holbrook N.J.
Oxidants, oxidative stress and the biology
of ageing. Nature. 2000; 408(6809):239–247.
6. FJ. Hurtado Breddaa, N. Nin Vaezab, H. Rubbo Amoninic. Estrés oxidativo y nitrosativo en la sepsis. Med Inten- siva.2005;29(3):159-65.
7. Apel K., Hirt H. Reactive
oxygen species: Metabolism, oxidative
stress, and signal transduction. Annu. Rev. Plant Biol. 2004;55:373–399.
8. McCord, J.M. The evolution of
free radicals and oxidative stress.
Am. J. Med. 2000;108(8): 652–659.
9. Lowenstein CJ, Dinerman JL, Snyder SH. Nitric Oxide:APhysiologic Messenger. Ann lntern Med. 1994;120(3):227- 237.
10. Mittler, R. Oxidative
stress, antioxidants and stress toler
ance. Trends Plant Sci.2002;7(9):405–410.
11. Pedraza-Chaverri
J., Cárdenas-Rodríguez N., Chirino YI. El óxido nítrico
y las especies reactivas de nitrógeno. Aspectos básicos e importancia
biológica. Educación Química. 2006;17(4):443-451.
12. Expósito
LA, Kokoszka JE, Waymire KG. Mitochondrial oxidative stress in mice lacking the glutatione peroxidase-1 gene.
Free Radic Biol Med. 2000;28(5):754-66.
13. Armone-Caruso A., Del Prete A., Lazzarino AI., Expósito LA, Kokoszka JE, Waymire KG. Mitochondrial oxidative stress
in mice lacking the glutatione peroxidase-1 gene. Free Radic Biol Med. 2000;28(5):754-66.
14. Market M, Andrew PC, Babior BM. Measurement of O2-
production by human neutrophils. The preparation and assay of NADPH oxidase-containing particles from human neutrophils. Methods Enzimol
1984;105:358-65.
15. Coronado
M., Vega S., Rey L., Vázquez M., Radilla C. Antioxidantes: Perspectiva actual para la salud humana.
Rev. Chil. Nutr. 2015;42(2):206-212.
16. Borut P., Dušan Š.Milisav I. Achieving the balance be- tween ROS and antioxidants: when to use
the synthetic antioxidants. Oxid Med Cell Longev. 2013;2013: 956792.
17. Mayor-Oxilia, R. Estrés Oxidativo
y Sistema de Defensa Antioxidante. Rev. Inst. Med. Trop. 2010;5(2):23-29.
18. Fridovich I.
Superóxido dismutasas. Annu Rev Biocem. 1975;44:147-159.
19. Arch. Bioechem
Biophyns. 1984;228(2):617-620.
20. Rodríguez-Perón JM., Menéndez-Lopez JR., Trujillo-Lopez Y. Radicales libres en la
biomedicine y estrés oxidativo. Rev Cub Med
Mil. 2001;30(1):15-20.
21. Mittler, R. Oxidative
stress, antioxidants and stress tolerance. Trends Plant
Sci. 2002;7(8): 405–410.
22. Eiserich, J.P., van der Vliet, A., Handeltman, GJ., Halliwell. B. Cross, C.E.
Antioxidantes dietéticos y daño biomole- cular
inducido por el humo del cigarrillo: una interacción compleja. Am. J. Clin. Nutr.1995;62(6):1490S-1500S.
23. Montero
M. Los radicales libres y las defensas antioxidantes. Revisión. AnalFacMed Univ Nal Mayor de San Marcos.1996;57(4); 278-281.
24. Segurola-Gurrutxaga H., Cárdenas-Lagranja G., Bur- gos-Peláez R. Nutrientes e inmunidad.
Nutr Clin Med 2016;X(1):1-19.
25. Li, X., Geng, M., Peng Y., Meng Y. Lu S. Molecular im- mune pathogenesis and diagnosis of COVID-19. X. Li et al., Molecular immune pathogenesis and
diagnosis of COVID-19. J Pharm Anal. 2020;10(2):102–108.
26. Lu R., Zhao X., Li J., Ni P., Yang B., Wu H., et al. Genomic caracterisation and epidemiology of 2019 novel corona-
virus: implications for virus origins and receptor binding. Lancet. 2020;395(10224):565 – 574.
27. Mousavizadeh, L., Ghasemi S. Genotype
and phenotype of COVID-19: Their roles in
pathogenesis. J. Microbiol. Immunol. Infec.
202154(2):159-163.
28. Chen Y., Liu Q., Guo D. Emerging coronaviruses: Genome structure, replication, and
pathogenesis. J. Med. Virol.2020;92:418- 23.
29. Letko M, Marzi A, Munster V. Functional assessment of cell entry and receptor usage for SARS-CoV-2 and other lineage B betacoronaviruses. Nat Microbiol. 2020;5:562-569.
30. Hoffmann M, Weber
HK, Schroeder S, Krüger Herrler
T, Erichsen S. et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a 1clinically-proven protease inhibitor. Cell. 2020;181(2):271-289.
31. Song W, Gui M, Wang X, Xiang Y. Cryo-EM
structure of the SARS coronavirus spike glycoprotein in complex with its host cell receptor ACE2. PLoS
Pathog. 2018;14(8):e1007236.
32. Hao, X.; Liang, Z.; Jiaxin, D.; Jiakuan, P.; Hongxia, D.; Xin, Z. et al. High expression of ACE2
receptor of 2019 nCoV on the
epithelial cells of oral mucosa. Int. J. Oral Sci. 2020;12(1):8.
33. Eakachai, P., Chutitorn K., Tanapat P. Immune responses in COVID-19
and potential vaccines: Lessons learned from
SARS and MERS epidemic. Asian Pac. J. Allergy
Immunol. 2020;38(1):1-9.
34. Li
G., Fan Y., Lai Y, Han T., Li Z., Zhou P., et al. Coronavirus infections and
immune responses. J Med Virol. 2020;92(4):424-432.
35. Gralinski LE, Sheahan TP, Morrison TE, et al. Complement activation contributes to severe acute respiratory syndrome coronavirus pathogenesis. mBio. 2018;9(5):e01753‐18.
36. Rokni, M.; Ghasemi, V. & Tavakoli, Z. Immune responses and pathogenesis of SARS-CoV-2 during an outbreak in Iran: Comparison with SARS and MERS. Rev Med Virol. 2020;30(3):e2107.
37. Lopez
PGT, Ramírez SMLP, Torres AMS. Participantes
de la respuesta inmunológica ante la infección por SARS- CoV-2. Alerg Asma
Inmunol Pediatr. 2020;29(1):5-15.
38. Haipeng Z., Ti W. CD4+T, CD8+T counts and severe COVID-19: A meta-analysis J Infect.2020;81 (3):e82–e84.
39. Guan W, Ni Z.,Hu Y., Liang W.,Ou C., He J., et al. Clinical Characteristics of Coronavirus Disease 2019 in China.
N Engl J Med. 2020;382(18):1708-1720.
40. Li YR., Jia Z., Trush MA. Defining
ROS in Biology and Medicine. React Oxyg Species
(Apex). 2016;1(1):9-21.
41. Kalyanaraman B. Teaching the basics of redox biology to medical and graduate students: Oxidants,
antioxidants and disease
mechanisms. Redox Biol. 2013;1(1):244-57.
42. Cecchini B., Lourenço-Cecchini A. SARS-CoV-2 infection pathogenesis is related to oxidative stress
as a response to aggression. Med Hypotheses. 2020;143:110102.
43. Saleh J., Peyssonnaux C.,, Singh KK., Edeas M. Mito- chondria
and microbiota dysfunction in the pathogenesis of COVID-19. Mitochondrion. 2020;54:1-7.
44. Peterhans E. Oxidants and antioxidants in viral diseases: disease mechanisms and metabolic
regulation. J Nutr. 1997;127(5 Suppl):962S-965S.
45. Schwartz KB. Oxidative stress during viral infection: a review.
.Free Radic Biol Med. 1996;21(5):641-9.46
46. Suresh DR, Annam V, Pratibha K, Prasad BV. Total antioxidant capacity--a novel early bio-chemical marker of oxidative stress in HIV infected
individuals. J Biomed Sci. 2009;16(1):61.
47. Delgado-Roche
L., Mesta F.. Oxidative stress as a key player in severe
acute respiratory syndrome
coronavirus (SARS-CoV)
infection. Arch Med Res. 2020;51(5):384-387.
48. Firas R.,. Mazhar, A., Ghena K.,; Dunia, S. Amjad A. SARS-CoV2 and Coronavirus Disease 2019:
What we know so far. Pathogens. 2020;9(3):231.
49. Edeas M, Saleh J, Peyssonnaux C. Iron: innocent or vi- cious bystander guilty of COVID-19
pathogenesis? Int J Infect Dis. 2020;97:303-305..
50. Laforge M., Elbim C., Frère C., Hémadi M., Massaad C et al. Tissue damage from
neutrophil-induced oxidative stress
in COVID-19. Nat RevImmunol.2020;20(9):515 –516.
51. Schönrich G, Raftery MJ, Samstag Y. Devilishly radical network
in COVID-19: oxidative
stress, extracellular neutrophil traps (NET), and T-cell
suppression. Adv Biol Regul. 2020;77:100741.52
52. Leppkes M., Knopf J., Naschberger E, Lindemann A., Singh J., Herrmann I. et al. Vascular
occlusion by extracellular
neutrophil traps in COVID-19. EBioMedicine. 2020; 58:102925.
53. Panfoli I. Potential role of ectopic redox complexes on the surface of endothelial cells in the
pathogenesis of COVID-19 disease.
Clin Med. 2020;20(5):e146-e147.
54. Lin J.H., Walter P., Yen T.S.B. Endoplasmic reticulum stress in disease pathogenesis. Ann. Rev. Pathol. 2008;3:399–425.
55. Banerjee A, Czinn SJ., Reiter RJ., Blanchard TG. Cross- talk between endoplasmic reticulum stress and anti-viral activities: A novel therapeutic target
for COVID-19. Life Sci.2020:255:117842.
56. Li Z., Xu X., Leng X., He M., Wang J., Cheng S et al. Roles of reactive oxygen species in cell
signaling path- ways and immune
responses to viral infections . Arch Virol.2017;162(3):603-610. 57
57. Ye Q, Wang B, Mao J. The pathogenesis and treatment of the ‘Cytokine Storm’ in COVID-19. J Infect. 2020;80(6):607–613.
58. Foley J.H., Conway E.M. Cross talk pathways between coagulation and inflammation. Circ Res. 2016;118(9):1392–408.
59. Tang N., Li D., Wang X., Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients
with novel coronavirus pneumonia. J Thromb Haemost. 2020;18:844–847.
60. Zhou
F, Yu T, Du R, Fan G, Liu Y, Liu Z et al. Clinical course and risk factors for mortality of
adult inpatients with COVID-19 in
Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054-1062.
61. Barzola
CM, Parra-Amay CL, Carranza-Delgado KA, Mayorga-Fierro
LM. Trastornos de la coagulación en pacientes
infectados con coronavirus: Covid-19. RECI- MAUC. 2020;4(3):50-57.
62. José RJ, Williams AE, Chambers RC. Proteinase-activated receptors in fibroproliferative lung
disease. Tórax. 2014;69(2):190-192.
63. Fenghe Du, Bao Liu, Shuyang Zhang. COVID-19: the
role of excessive cytokine
release and possible decrease in ACE2 in promoting
the hypercoagulable state associated with severe disease.
J Thrombolysis. 202051(2): 1-17.
64. Fehr AR, Channappanavar R , Perlman S. Middle East Respiratory Syndrome: Emergence of a Pathogenic Human Coronavirus. Annu Rev Med.2017;68:387-399.
65. Xiong Y., Liu Y, Cao L., Wang D., Guo M., Jiang A. et al. Transcriptomic characteristics of bronchoalveolar lavage
fluid and peripheral blood mononuclear cells in COVID-19 patients. Emerg Microbes Infect.
2020;9(1):761-770.
66. Thaker SK, Ch’ng J, Christofk HR. Viral hijacking of cellular
metabolism.. BMC Biol.2019;17(1):59.67 Fowler
R., Hayden FG., Zumla A., Hui DS., Azhar EI., Memish, et al. Reducing mortality from
2019-nCoV: host-directed therapies should be an option. Intensive Care Med. 2020;395:e35-e36.
67. Fowler
R., Hayden FG., Zumla A., Hui DS., Azhar EI.,
Memish, et al. Reducing mortality from 2019-nCoV: host-
directed therapies should be an option. Intensive
Care Med. 2020;395:e35-e36.
68. Leng Z, Zhu R, Hou W, Feng Y, Yang Y, Han Q, et al. Trans- plantation of ACE2- Mesenchymal Stem
Cells Improves the Outcome
of Patients with COVID-19 Pneumonia. Aging Dis. 2020;11:216–28.
69. Mehta P, McAuley DF., Brown M., Sánchez E., Tatter- sall RS., Manson JJ. et al. COVID-19:
consider cytokine storm
syndromes and immunosuppression. Lancet. 2020;395(10229):1033-1034.
70. Panigrahy D, Gilligan MM, Huang S, Gartung A, Cor- tés-Puch I, Sime PJ, et al. Inflammation
resolution: a two-pronged approach to
avoiding cytokine storms in COVID-19?
Cancer Metastasis Rev.2020; 39(2):337–40.
71. Lokugamage KG.,Hage A., de Vries M., Valero-Jiménez AM., Schindewolf C., Dittmann M., et al. Type I interferon susceptibility distinguishes SARS-CoV-2 from SARS-CoV. BioRxiv. 2020.
Recibido: Mayo 10, 2021
Aceptado: Agosto 02, 2021
Correspondencia: Rubén Darío Camargo Rubio rcamargorubio@gmail.com