Resúmen
En los últimos años, el ámbito de la inmunoterapia contra el cáncer ha
experimentado un progreso
sobresaliente debido a la mejor comprensión sobre la biología de los
linfocitos y su rápida traducción a
ensayos clínicos. Los inhibidores de puntos de control inmunológico
(ICI, por sus siglas en inglés) han
demostrado un impacto significativo en el tratamiento de pacientes con
cáncer de pulmón de células
no pequeñas (CPCNP) surgiendo como una opción eficaz de tratamiento,
incluso en el entorno de la
primera línea. Los ICI pueden bloquear las vías inhibidoras que
restringen la respuesta inmunitaria
contra el cáncer, restaurando y manteniendo la inmunidad antitumoral.
Actualmente hay 5 agentes
disponibles para bloquear PD-1/PD-L1, y los regímenes que incluyen
inmunoterapia sola o en combinación con quimioterapia u otro ICI, son
ahora la opción preferida. Hay esfuerzos continuos para
encontrar biomarcadores predictivos que permitan perfilar el patrón de
respuesta a los ICIs. Las expresiones de PD-L1 cuantificada por
inmunohistoquímica y la carga mutacional han emergido como
los marcadores mejor validados en múltiples ensayos clínicos. Sin
embargo, todavía existe la necesidad
de mejorar la selección de los pacientes, y establecer cuáles de las
terapias en son más efectivas en los
diferentes entornos clínicos del CPCNP. Esta revisión presentará la
utilidad de los ICIs en el CPCNP
analizando los estudios clínicos más recientes, para discutir quienes
tendrán el mayor beneficio para
proporcionar una vía óptima que permita modificar los desenlaces de la
enfermedad.
Palabras clave: Cáncer de pulmón; inmunoterapia;
linfocitos; punto de control inmunológico; biomarcador.

¹ Departmento de Oncología Médica, Centro Integral Oncológico Clara
Campal (HM-CIOCC), Hospital HM Delfos, HM Hospitales,
Barcelona, España
THE IMMUNOTHERAPY REVOLUTION:
IMMUNE CHECKPOINT INHIBITORS FOR NON-SMALL
CELL LUNG CANCER
Abstract
In recent years, the field of cancer immunotherapy has seen outstanding
progress due to
our improved understanding of lymphocyte biology and its rapid
translation into clinical trials.
Immune checkpoint inhibitors (ICIs) have shown significant impact in
treating patients with
Non-small-cell lung cancer (NSCLC) and have emerged as an effective
treatment option even
in the first-line setting. ICIs can block inhibitory pathways that
restrain the immune response
against cancer, restoring, and sustaining antitumor immunity. There are
currently 5 PD-1/PDL1 blocking agents available, and
immunotherapy-based regimens alone or in combination
with chemotherapy or another ICI is now the preferred option. There are
continuous efforts
to find predictive biomarkers to find those who respond better to ICIs.
PD-L1 expressions by
immunohistochemistry and tumor mutational burden have emerged as the
most well-validated
biomarkers in multiple clinical trials. However, there is still a need
to improve patient selection
and establish the most effective concurrent or sequential combination
therapies in different
NSCLC clinical settings. This review will introduce currently used ICIs
and analyze the most
recent trials, and finally discuss how, when, and for whom ICIs can be
used to provide promising avenues for lung cancer treatment.
Keywords: Lung cancer; immunotherapy; lymphocytes;
immune checkpoint; biomarker
Introducción
“En el curso enormemente complicado del
desarrollo fetal
y posfetal, las células aberrantes se
vuelven inusualmente
comunes. Afortunadamente, en la
mayoría de las personas
quedan completamente latentes gracias
a los mecanismos
positivos que defienden el organismo”
Paul Erlich
La introducción de los inhibidores de puntos de control inmunitarios
(ICI, por sus siglas en inglés) ha
transformado rápidamente el paradigma de tratamiento para múltiples
tipos de cáncer, incluidas las neoplasias torácicas. En el cáncer de
pulmón de células no
pequeñas (CPCNP) avanzado, este cambio se debe en
parte al notable beneficio sobre la supervivencia global
(SG) a largo plazo, ya que la administración de estos
medicamentos favorece una tasa de supervivencia a 5
años que oscila entre el 15% y el 30%, entre los pacientes previamente
tratados y sin ninguna intervención
previa, respectivamente (1). Se han probado diferentes
ICIs en pacientes con CPCNP avanzado; entre otros,
los inhibidores del antígeno 4 del linfocito T citotóxico
(CTLA-4), y del receptor y ligando de muerte programada (PD-[L]1),
ambos forman parte activa de la estrategia de tratamiento en
combinación (con inmunoterapia, quimioterapia o agentes
antiangiogénicos) o
en monoterapia como parte del entorno terapéutico de
la primera línea. Asimismo, el tratamiento de consolidación con
Durvalumab (un anticuerpo monoclonal
anti-PD-L1) constituye un nuevo estándar de manejo
para el CPCNP localmente avanzado después de la
quimiorradiación, intervención que generó una prolongación en la SG sin
precedentes (2). Es probable
que, en un futuro próximo, la inmunoterapia también
modifique diversos axiomas sobre el manejo del CPCNP en estados
tempranos (3,4). Esta revisión tiene
como objetivo resumir la evidencia actual respecto de
la eficacia de los ICIs en monoterapia o combinación
para el CPCNP, utilizando diversos biomarcadores
predictivos, y las aprobaciones de las agencias regulatorias para la
evaluación de medicamentos de los
Estados Unidos (
Federal Drug
Administration, FDA) y
de la Comunidad Europea (
European
Medicines Agency, EMA). El uso de la inmunoterapia en cáncer de
pulmón representa uno de los mejores ejemplos de la
transformación de la historia natural y evolución del
diagnóstico y tratamiento del cáncer. La
Figura 1 ilustra la línea de tiempo
desde el desarrollo de la inmunoterapia inespecífica hasta los
antagonistas y agonistas
disponibles en la actualidad.
Monoterapia con ICI como estrategia
de tratamiento de primera línea
en pacientes con CPCNP y PD-L1
positivo
La búsqueda e implementación de biomarcadores para
predecir la respuesta a la inmunoterapia es un tópico
crítico para el ámbito oncológico. Los dos que han
sido explorados con mayor avidez son la expresión de
PD-L1 y la carga mutacional (TMB,
por
sus siglas en
inglés). La TMB representa el número total mutaciones
somáticas (Mut) no sinónimas que se identifican en
cada megabase (Mb) del área que codifica el genoma
tumoral. Por el momento, la TMB no se ha visto relacionada con la
supervivencia global (OS) en pacientes
con CPCNP. De hecho, existen varias inquietudes respecto de cuál es la
mejor técnica para evaluar la TMB
[(secuenciación completa del exoma - WES,
por sus
siglas en inglés) vs. secuenciación de nueva generación
(NGS, por sus siglas en inglés)], evento que desencadenó limitaciones
para la estandarización de la prueba a
partir de diversos paneles genéticos. De igual forma,
no existe un punto de corte estandarizado entre diferentes neoplasias.
Estas dificultades han limitado la introducción de la TMB como
biomarcador útil para
seleccionar y estratificar a los pacientes candidatos a
recibir ICIs como monoterapia o en combinación para
la primera línea (5).
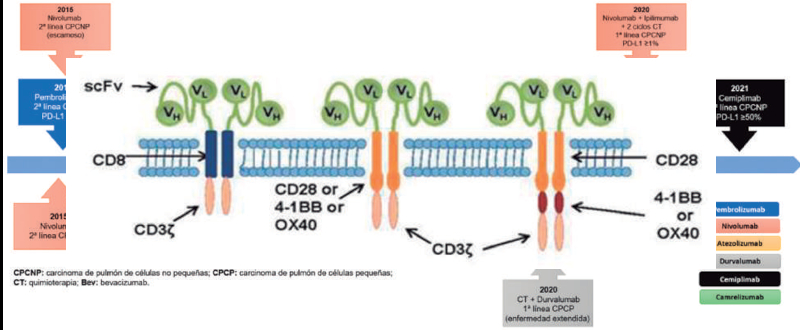
Figura 1. Línea de tiempo que ilustra el desarrollo de la
inmunoterapia específica en cáncer de pulmón
Por otro lado, la evaluación del nivel de expresión de PD-L1 en el
tejido tumoral puede
realizarse usando diferentes anticuerpos monoclonales
desarrollados sobre plataformas automatizadas de inmunohistoquímica
(IHC, por sus siglas en inglés). Las
diferencias entre estos pueden explicar, al menos en
parte, los resultados divergentes al comparar el desempeño de cada una
de las pruebas (SP142, 28,8, 22C3,
SP263, y 73-10). De acuerdo con lo anterior, la fase 2
del estudio “Blueprint” (estudio comparativo de IHC
para PD-L1) se diseñó para armonizar los resultados
proporcionando información sobre la comparabilidad
clínica y analítica de los cuatro monoclonales descritos. El estudio
reveló que tres de las cinco pruebas
para evaluar la expresión de PD-L1 tenían una elevada
concordancia (22C3, 28-8, y SP263), mientras que el
anticuerpo SP142 tuvo menor marcación en las células tumorales y el
73-10 demostró una alta sensibilidad
con baja especificidad (6). La
Figura
2 muestra algunos de los biomarcadores más representativos para
la
estratificación de los pacientes candidatos a recibir inmunoterapia.
Desafortunadamente, un subgrupo de pacientes no se
beneficia de los ICIs a pesar de tener una expresión
positiva de PD-L1, y en oposición, otros sin ella responden. A pesar de
las limitaciones vinculadas con el
uso regular de la expresión de PD-L1, este biomarcador continúa siendo
el estándar para seleccionar los
candidatos a recibir monoterapia con pembrolizumab,
atezolizumab o cemiplimab. De hecho, existe una relación directa y
proporcional entre la expresión de PDL1 y la supervivencia global (7).
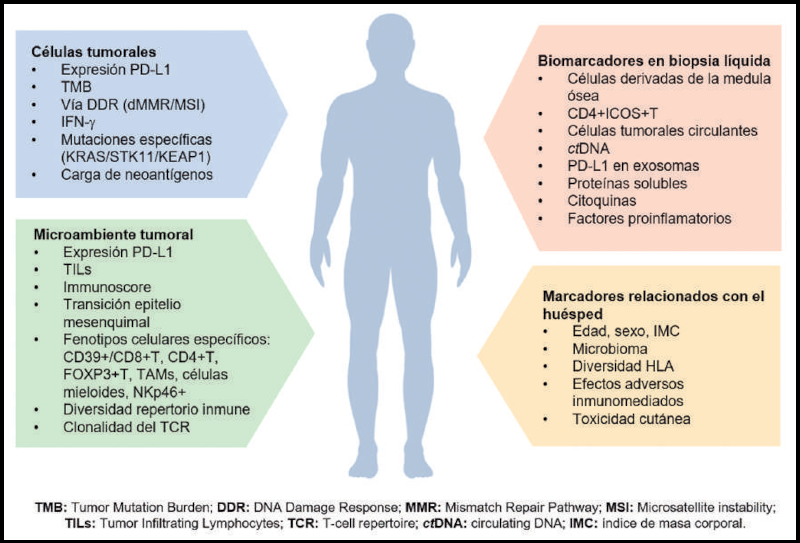
Figura 2. Potenciales biomarcadores para predecir la utilidad de la
inmunoterapia divididos según su relación con las
características del huésped, las células tumorales, el microambiente
tumoral, y en biopsia líquida.
De acuerdo con varios
experimentos clínicos fase 3 que incluyeron pacientes
con CPCNP avanzado sin alteraciones genómicas
potencialmente modulables (mutaciones en EGFR
y traslocaciones de ALK), el tratamiento inicial con
ICI en monoterapia constituye el estándar terapéutico
para aquellos pacientes con alta expresión de PD-L1.
Para los pacientes con tumores (≥ 50% oTC3/IC3). El
pembrolizumab, evaluado en los estudios KEYNOTE-024 (8,9) y KEYNOTE-042
(10,11), el atezolizumab en el IMpower 110 (12), y el cemiplimab en el
estudio EMPOWER-Lung01 (13), reportaron mejoría
en la OS al ser comparados con la quimioterapia basada en platino. En
el estudio KEYNOTE-024 se evaluaron 1.934 pacientes, de los cuales 500
(30%) tuvieron
una expresión de PD-L1 ≥50%; de estos, se aleatorizaron 305 para
recibir pembrolizumab (200 mg IV c/3
semanas) hasta intolerancia, progresión o 2 años de
intervención vs. 4 a 6 ciclos de un doblete de platino
estándar (8). Todas las medidas de eficacia favorecieron al
pembrolizumab, incluyendo la tasa de respuesta
global (RR, por sus siglas en inglés) (46% vs. 31%), la
supervivencia libre de progresión (PFS, por sus siglas
en inglés) (7,7 meses vs. 5,5 meses; HR 0,50, IC 95%
0,39-0,65, P<0,001) y la OS (26,3 meses vs. 14,3 meses; HR 0,62, IC
95% 0,48-0,81), incluso a pesar de
un 66% de entrecruzamiento. Cabe señalar que la OS
a 5 años fue de 32% con pembrolizumab vs. 16% para
la quimioterapia (9), lo que reafirma una estrategia de
manejo inicial basada en ICIs. De hecho, también se
documentó que el pembrolizumab mejoró o mantuvo
la calidad de vida (14). Aunque los resultados son limitados, 39
pacientes completaron 2 años de tratamiento
con pembrolizumab, alcanzando una OS a 3 años del
81%. La reinducción con el anti-PD-1 se llevó a cabo
en 12 pacientes que presentaron progresión después de
2 años o 35 ciclos de tratamiento; la segunda secuencia
del monoclonal se asoció a una RR del 33% y a una
tasa de control de enfermedad (DCR, por su sigla en
inglés) del 83%. Sin embargo, no hay biomarcadores
predictivos que permitan reconocer cuales casos son
elegibles para la estrategia de reinducción (9).
En el estudio KEYNOTE-042 se aleatorizaron 1.274
pacientes con CPCNP y PD-L1 de ≥1% para recibir
tratamiento con pembrolizumab o con quimioterapia
sin permitir el entrecruzamiento. Los pacientes que
recibieron pembrolizumab tuvieron un beneficio significativo en la OS,
en particular gracias al segmento
de sujetos con una expresión de PD-L1 ≥50% (20,0
meses vs. 12,2 meses, HR 0,70, IC95% 0,58-0,86), en
aquellos con niveles ≥20% (18,0 meses vs. 13 meses,
HR 0,77, IC 95% 0,65-0,91), y en el subgrupo con expresión ≥1% (16,4
meses vs. 12,1 meses, HR 0,82, IC
95% 0,71-0,93). No obstante, un análisis exploratorio
no reportó un beneficio significativo en tumores con
expresión de PD-L1 entre 1-49% (13,4 meses vs. 12,1
meses, HR 0,91, IC 95% 0,77-1,09) (10,11).
El estudio IMpower 110 valoró el manejo inicial con
atezolizumab (1.200 mg c/3 semanas) comparado con
quimioterapia estándar 572 pacientes con CPCNP
avanzado y un nivel de expresión de PD-L1 ≥1% en
las células tumorales, o al menos 1% de reactividad
en los linfocitos infiltrantes del tumor usando el anticuerpo
monoclonal SP142. El IMpower 110 permitió
el entrecruzamiento, favoreciendo que el 29,6% de los
pacientes en el grupo control recibieran ICIs al momento de la
progresión. El análisis de la OS fue jerarquizado según los estratos de
expresión del PD-L1. En
el subgrupo TC3/IC3 el atezolizumab demostró superioridad en la OS en
comparación con la quimioterapia (20,2 meses vs. 13,1 meses, HR 0,59,
IC 95% 0,40-
0,89; P=0,01). De forma similar, la mediana de la PFS
(8,1 meses vs. 5,0 meses, HR 0,63; IC 95% 0,45-0,88;
P=0,007) y la RR (38,3% vs. 28,6%, respectivamente)
favorecieron el uso del anti-PD-L1. Sin embargo, el
análisis de la OS no consideró la superposición de las
poblaciones con niveles de expresión TC2/3 e IC2/3
(12). De los 554 pacientes, 389 fueron evaluados según la TMB valorada
en sangre (bTMB, por sus siglas en inglés); el 22,4% tenía una bTMB ≥16
mutaciones
por Mb (Mut/Mb). En este subgrupo, el atezolizumab
mostró una mejoría no significativa en la OS comparado con la
quimioterapia (13,9 meses vs. 8,5 meses, HR
0,75; IC95% 0,41-1,35), lo que desestimó la utilidad
de la bTMB como marcador potencial para definir el
beneficio de la monoterapia con ICIs (12).
Finalmente, en el estudio EMPOWER-Lung 01, 563
pacientes con CPCNP avanzado y PD-L1 ≥50% se
aleatorizaron para recibir cemiplimab (350 mg c/3 semanas hasta la
intolerancia, progresión o al completar
108 semanas de intervención) o un doblete de platino.
La terapia con cemiplimab impactó los desenlaces primarios,
favoreciendo al anti-PD-1 respecto de la PFS
(8,2 meses vs. 5,7 meses, HR 0,54, IC 95% 0,43-0,68;
P< 0,0001) y de la OS (no alcanzada vs. 14,2 meses, HR
0,57, IC 95% 0,42-0,77; P=0,0002) en comparación con
la quimioterapia, incluso a pesar de tener un entrecruzamiento del 74%.
La RR también fue superior con el
cemiplimab (39,2% vs. 20,4%) (13).
Con base en estos resultados, algunos de los ICIs ya
fueron aprobados por las autoridades sanitarias europea (EMA) y
americana (FDA). Sin embargo, como
monoterapia, el pembrolizumab solo está aprobado en
Europa para el tratamiento de aquellos tumores con alta
expresión de PD-L1, mientras que en Estados Unidos
la etiqueta incluyó aquellos con un nivel superior al 1%.
A pesar de que los ICIs presentan un perfil de toxicidad
favorable, la tasa de eventos adversos grado ≥3 parece
ser similar entre los tumores con baja y alta expresión
de PD-L1, oscilando entre el 17% y 37%, y con una tasa
de interrupción de la intervención del ~10%.
Sin embargo, aún en pacientes seleccionados, los ICI
como monoterapia o en combinación han tenido resultados negativos en la
primera línea, como se evidenció
en los estudios fase tres CheckMate 026 (15) MYSTIC
(16). En el estudio CheckMate 026, el nivolumab no
mejoró la PFS ni la OS, en comparación con la quimioterapia estándar
usada en pacientes con CPCNP
avanzado con expresión de PD-L1 de ≥5% (15). Un
análisis exploratorio del estudio CheckMate 026 en tumores con alta TMB
(>243 Mut por WES) demostró
que el nivolumab tuvo una mejor tasa de respuesta vs.
la quimioterapia (47% vs. 28%), y una PFS más prolongada (9,7 meses vs.
5,8 meses; HR 0,62, IC95% 0,38-
1,00); no obstante, no se evidenció diferencia para la
OS. De hecho, el mayor beneficio para los desenlaces
de supervivencia fue para el subgrupo de aquellos con
una elevada TMB más alta expresión de PD-L1 (15).
De forma similar, en el estudio MYSTIC no se logró
un impacto positivo en los desenlaces clave incluyendo la OS y la PFS
al comparar el durvalumab con la
quimioterapia estándar, o la combinación de durvalumab/tremelimumab vs.
el manejo habitual de los
pacientes con enfermedad avanzada y una expresión
de PD-L1 ≥25% (16). El análisis exploratorio de los
pacientes con una bTMB ≥20 Mut/Mb demostró una
diferencia significativa a favor de la inmunoterapia
dual respecto de la OS (21,9 meses vs. 10,0 meses para
la quimioterapia; HR 0,49, IC 95% 0,32-0,74). Asimismo, la TMB
determinada en tejido tumoral (≥10 mut/
Mb) se asoció con una OS más prolongada para el durvalumab solo o en
combinación con tremelimumab al
ser comparados con la quimioterapia (16).
En contraposición, la combinación de nivolumab/ipilimumab utilizada
como primera línea demostró una
mejoría significativa en la OS al ser comparada con la
quimioterapia. En la primera parte del estudio CheckMate 227
(17,18)29,3 mo, la combinación de nivolumab
(3 mg/kg c/2 semanas) más ipilimumab (1 mg/kg c/6
semanas) impactó el desenlace primario demostrando un
beneficio significativo sobre la OS en tumores con PDL1 positivo (17,1
meses vs. 14,9 meses; HR 0,79, IC
95% 0,67-0,93). Sin embargo, el 71% de los pacientes
en el brazo control recibieron algún ICI al momento
de la progresión. Es importante resaltar que la OS a 3
años fue del 33% con la combinación de nivolumab/
ipilimumab y 22% con la quimioterapia. Un análisis exploratorio,
también demostró una mejoría en la
OS con la combinación de ICIs en tumores con PDL1 <1% (17,2 meses
vs. 12,2 meses; HR 0,64, IC 95%
0,51-0,81) (17). Por otra parte, en la población con PDL1 positivo el
beneficio sobre la supervivencia estuvo
limitado al segmento de sujetos con alta expresión de
PD-L1 (PD-L1 ≥50% HR 0.70, IC 95% 0,55-0,90 vs.
PD-L1 1-49% HR 0,94 IC 95% 0,73-1,12) (18). A pesar de estas
limitaciones, la FDA aprobó en mayo de
2020 la combinación de nivolumab/ipilimumab en pacientes con CPCNP con
PD-L1 ≥1%.
En el estudio CheckMate 227, el análisis realizado en
un punto designado durante el seguimiento demostró
que la tasa de respuesta global se relaciona de forma
independiente con los niveles de expresión de PD-L1.
La valoración realizada a los 3 años encontró que el
70% y 82% de los pacientes estaban vivos si tenían un
PD-L1 positivo y negativo, respectivamente (17); esta
información resultó similar a lo encontrado en otras
patologías como el melanoma. En la parte 1 del estudio CheckMate 227
también se encontró un desenlace
positivo a favor de la combinación en aquellos pacientes con tumores
que tuvieron una elevada TMB (≥ 10
Mut/Mb). Este punto de corte se estableció siguiendo los resultados
reportados en la fase dos del estudio
CheckMate 568 (19). En el CheckMate 227, el 17% de
la población tuvo una TMB alta, usando este parámetro para asignar de
forma aleatoria a los pacientes para
recibir nivolumab/ipilimumab (N=169) o quimioterapia (N=130). La
combinación de ICIs mejoró la PFS
(HR 0,58, IC 75% 0,41-0,81), sin embargo, los resultados para la OS
fueron independientes de la TMB (alta
≥10 Mut/Mb HR 0,68, IC 95% 0,51-0,91 vs. o baja
<10 Mut/Mb HR 0,75, IC 95% 0,59-0,94) (20).
El estudio NEPTUNE (NCT02542293) evaluó la eficacia de la combinación
de durvalumab más tremelimumab frente a la quimioterapia basada en
platino
como tratamiento de primera línea en pacientes con
CPCNP avanzado. El 6 de junio de 2019, se dieron
a conocer los resultados para la OS según la bTMB
usando como punto de corte la presencia de 20 Mut/
Mb. Posteriormente, se confirmó que la combinación
de ICIs no alcanzó la significancia para la OS vs. la
quimioterapia. Esta información permitió cuestionar el valor predictivo
de la TMB como biomarcador
para definir el tratamiento con ICIs en los pacientes
con CPCNP avanzado. Actualmente se encuentra en
curso el estudio BFAST (NCT03178552), un experimento clínico fase 3 que
esta evaluando el papel del
atezolizumab vs. la quimioterapia con base en platino
en primera línea en pacientes con CPCNP avanzado y
una elevada bTMB (≥16 mut/Mb). Los resultados de
este estudio podrían ayudar a definir o no el papel de
la TMB para refinar la toma de decisiones en la primera línea. A pesar
de la controversia, recientemente
la FDA aprobó el uso del pembrolizumab en tumores
con una elevada TMB (≥10 Mut/Mb) de acuerdo al
análisis retrospectivo del estudio KEYNOTE-158 (21).
Sin embargo, esta evaluación no incluyó pacientes con
CPCNP, lo que mantiene en duda el valor real de la
TMB en los pacientes con cáncer de pulmón.
Combinación de ICIs con quimioterapia
en la primera línea de tratamiento del
CPCNP (independiente del nivel de
expresión de PD-L1)
En los estudios clínicos que valoraron el papel de los
ICIs como monoterapia o en combinación (inhibidores de PD-1/L1 más
CTLA-4) en pacientes con expresión de PD-L1 ≥1% (11,16,20,22) se ha
documentado
un fenómeno donde las curvas de supervivencia se entrecruzan
tempranamente. Este hallazgo ha sugerido
que una proporción de pacientes sin beneficio con la
inmunoterapia podrían no exponerse a la intervención
con base en el uso de biomarcadores con un alto valor
predictivo negativo. Con la finalidad de superar esta
situación y tomar ventaja de la actividad sinérgica de
los agentes citotóxicos y de la inmunoterapia, diferentes estudios
clínicos evaluaron el papel de la combinación de ICIs con
quimioterapia. Hay que resaltar, la existencia de la hiperprogresión,
un modelo negativo
de respuesta encontrado en aproximadamente 14-26%
de los pacientes con CPCNP pretratados que recibieron monoterapia con
algún ICI en segunda línea.
Hace poco, el análisis exhaustivo de una cohorte de
pacientes tratados con ICIs permitió confirmar que la
hiperprogresión se presenta hasta en el 16% de los pacientes con
elevada expresión de PD-L1, posiblemente por la presencia de
resistencia innata mediada por
comutaciones en genes como STK11 y KEAP1. No
obstante, la hiperprogresión es inusual (6%) entre los
sujetos expuestos a quimioterapia más inmunoterapia
(23), evento que respalda el uso de este tipo de combinaciones en
primera línea.
Los resultados de múltiples estudios fase 3 incluyendo
el KEYNOTE-189 (24,25), IMpower150 (26,27), IMpower132 (28), IMpower130
(29), ORIENT-12 (30)
y RATIONALE 304 (31) soportan el uso de nuevas
combinaciones con ICIs como primera línea estándar
para pacientes con carcinomas no escamosos de pulmón. De igual forma,
los estudios KEYNOTE-407
(32,33), IMpower131 (34) y RATIONALE 307 (35)
demostraron el papel de la quimioinmunoterapia para
el tratamiento de los carcinomas escamosos, y CheckMate 227 parte 2
(36) y CheckMate 9LA (37) para
ambos subgrupos histológicos.
En el estudio KEYNOTE-189, se incluyeron pacientes
con CPCNP no escamoso avanzado, sin mutaciones
en EGFR o ALK, siendo asignados de forma aleatoria en un formato 2:1
para recibir pemetrexed más
cisplation o carboplatin y pembrolizumab o placebo
cada 3 semans por 4 ciclos; posteriormente, pembrolizumab y pemetrexed
o pemetrexed más placebo hasta
completar 2 años o 35 ciclos (24). El uso del pembrolizumab en
combinación con quimioterapia mejoró
significativamente la mediana de la OS (22,0 meses
vs. 10,6 meses, HR 0,56 IC 95% 0,46-0,96), a pesar de
que hubo un entrecruzamiento del 55%. Hay que resaltar que beneficio
sobre la OS se observó en todos
los subgrupos de expresión de PD-L1 [PD-L1 ≥50%
27,7 meses vs. 10,1 meses (HR 0,59, IC 95% 0,40-
0,86); PD-L1 1-49% 21,8 meses vs. 12,1 meses (HR
0,66, IC 95% 0,46-0,96); y PD-L1 <1% 17,2 meses vs.
10,2 meses (HR 0,51, IC 95% 0,36-0,71)]. La PFS también favoreció la
combinación de pembrolizumab más
quimioterapia (9,0 meses vs. 4,9 meses, HR 0,49, IC
95% 0,41-0,59) (25). En el estudio KEYNOTE-189, la
TMB medida en sangre o en tejido no fue útil como
biomarcador predictivo (38,39).
En el estudio IMpower150, la adición de atezolizumab
a bevacizumab más quimioterapia (brazo B) mejoró
significativamente la PFS (8,3 meses vs. 6,8 meses, HR
0,62, IC 95% 0,52-0,74; P<0,001) y la OS (19,2 meses
vs. 14,7 meses, HR 0,78 IC 95% 0,64-0,96; P=0,02) en
comparación con el uso de bevacizumab más quimioterapia (brazo C) en
pacientes con CPCNP no escamoso metastásico independeinte de la
expresión de
PD-L1 (26). El análisis final del IMpower150 también
mostró una mejoría numérica en la OS sin modificaciones
estadísticamente significativas en el brazo A
(atezolizumab más quimioterapia) vs. el brazo C (40).
En el subgrupo de sujetos con mutaciones del EGFR
el esquema del brazo B vs. el brazo C mejoró la PFS
(10,2 meses vs. 7,1 meses, HR 0,56 IC 95% 0,34-0,91)
y la OS (26,1 meses vs. 20,3 meses, HR 0,91 IC 95%
0,43-1,39) (27,41). En contraposición, el brazo A no
mejoró la PFS (HR 0,93 IC 95% 0,60-1,44) o la OS
(HR 1,16 IC 95% 0,71-1,89) en el grupo de pacientes
portadores de mutaciones en el EGFR (41). El estudio Impower130 (29)
fue un experimento multicéntrico abierto y con asignación aleatoria que
incluyó
pacientes con un formato 2:1 a recibir atezolizumab
(1.200 mg c/3 semanas) más carboplatino y paclitaxel unido a
nanoparticulas de albumina (nab-P) (4–6
ciclos) seguido de mantenimiento con atezolizumab
hasta la intolerancia o progresión. El IMpower130
(29) reportó un beneficio en la OS con la introducción
del monoclonal anti-PD-L1 cuando se comparó con
la quimioterapia (18,6 meses vs. 13,9 meses, HR 0,79 IC 95% 0,64-0,98;
P=0,033), pese a que se documentó
un 59% de entrecruzamiento con la inmunoterapia al
momento de la progresión. No obstante, el beneficio
real de esta combinación fue circunscrito a los sujetos
sin mutaciones en EGFR/ALK y entre aquellos sin
extensión hepática de la enfermedad, sugiriendo un
papel aditivo con el uso concomitante del bevacizumab. Por otra parte,
el uso del atezolizumab en combinación también mejoró la PFS (7,0 meses
en el brazo
de atezolizumab más quimioterapia vs. 5,5 meses en el
brazo de quimioterapia, HR 0,64 IC 95% 0,54 -0,77;
P<0,0001) y la RR (49,2% vs 39,2%, respectivamente).
Finalmente, dos estudios solo reclutaron pacientes
asiáticos; el ORIENT, que aleatorizó (2:1) 397 pacientes con CPCNP no
escamoso avanzado sin alteraciones en EGFR o ALK a recibir sintilimab
200 mg más
quimioterapia con base en platino vs. cisplatino/pemetrexed/placebo c/3
semanas por 4 ciclos seguidos,
en ambos casos, de mantenimiento con sintilimab/
pemetrexed o pemetrexed/placebo. La adición del
sintilimab mejoró significativamente la PFS en comparación con el
control (8,9 meses vs. 5,0 meses, HR
0,48 IC 95% 0,362-0,643; P<0,00001), al igual que incrementó la RR
(51,9% vs. 29,8%). El beneficio para la
PFS fue evidente en todos los subgrupos, siento superior para los
pacientes con expresión positiva de PDL1 (1-49% HR 0,50 IC 95%
0,28-0,92 y ≥50% HR 0,31
IC 95% 0,19-0,49) vs. aquellos con tumores con PD-L1
negativo (HR 0,66 IC 95% 0,41-1,091) (30).
El otro estudio dirigido a la población asiática exclusiva fue el
RATIONALE 307, un experimento clínico
fase 3 que incluyó 334 pacientes con CPCNO de patrón no escamoso sin
alteraciones en EGFR o ALK.
El estudio asignó de forma aleatoria (2:1) el uso de
tislelizumab (200 mg) más la combinación de platino
y pemetrexed por 4 ciclos seguido de tislelizumab más
pemetrexed vs. el modelo de tratamiento estándar solo
con quimioterapia. El uso del tislelizumab mejoró la
mediana de la PFS (9,7 meses vs. 7,6 meses, HR 0,56
IC 95%CI 0,46-0,90; P<0,0044) y la RR (57,4% vs.
37%). Sin embargo, el análisis por subgrupos demostró ineficacia sobre
la PFS para aquellos con PD-L1
negativo (HR 0,76 IC 95% 0,46-1,22), mientras el mayor beneficio se vio
para la población de altos expresores (PD-L1 ≥50% HR 0,31 IC 0,17-0,57)
(31).
En los pacientes con CPCNP de patrón escamoso avanzado el estudio
KEYNOTE-407 aleatorizó pacientes
(1:1) a recibir carboplatino/paclitaxel o paclitaxel unido a
nanopartículas de albumina +/- pembrolizumab
hasta completar 35 ciclos o 2 años de tratamiento. La
combinación de quimioterapia más el anti-PD-1 se
asoció con una mejora significativa de la RR (58,4%
vs. 35,0%; P=0,0004) y de la OS (HR 0,64, 15,9 vs.
11,3 meses; P=0,0008). El beneficio sobre la OS fue
homogéneo entre todos los subgrupos de expresión del
PD-L1 (TPS <1% HR 0,61, TPS 1%–49% HR 0,57, y
TPS ≥50% HR 0,64) (32,33). De hecho, la adición de
pembrolizumab a la quimioterapia mantuvo o mejoró
la calidad de vida (HRQoL) valorada a las 9 y 18 semanas de seguimiento
(42). En el experimento clínico
fase 3 RATIONALE 307, 360 pacientes asiáticos con
CPCNP de patrón escamoso avanzado (all comers) fueron aleatorizados a
recibir tislelizumab más nab-P o
quimioterapia sola. El brazo de la combinación con
el monoclonal alcanzó una PFS más prolongada (7,6
meses vs. 5,5 meses) y una mayor RR (74% vs. 50%).
El beneficio sobre la PFS fue evidente en todos los subgrupos de
expresión de PD-L1 (35).
Finalmente, el estudio CheckMate 9LA (37) valoró la
combinación de nivolumab más ipilimumab y 2 ciclos
de quimioterapia vs. quimioterapia en primera línea
para pacientes con CPCNP avanzado indistintamente de su variante
histológica. En el análisis intermedio
se encontró que la mediana para la S se prologó significativamente con
el uso de la inmunoterapia dual
más la quimioterapia comparada con la quimioterapia
sola (14,1 meses vs. 10,7 meses, HR 0,69 IC 96,71%
0,55–0,87; P=0,0006); el beneficio ocurrió de manera independiente al
subtipo histológico (histología escamosa 14,5 vs. 9,1 meses, HR 0,62 e
histología no escamosa 17,0 vs. 11,9 meses, HR 0,69), y para los
tumores
PD-L1-positivos (≥1% HR0,64) y PD-L1-negativos
(<1% HR 0,62). La FDA aprobó este modelo de tratamiento como parte
de la primera línea en mayo de
2020 y la EMA en septiembre del mismo año.
El estudio POSEIDON (NCT03164616) actualmente
en curso, está evaluando la efectividad del durvalumab
en combinación con quimioterapia con y sin tremelimumab vs. la
quimioterapia sola en pacientes con
CPCNP usando como desenlaces primarios la PFS y
OS de acuerdo a una revisión independiente. Se estima
que sus resultados estarán disponibles en abril de 2021.
Independientemente de estos resultados clínicamente relevantes, otros
estudios no reportaron beneficios
en la OS cuando se valoró el uso de la quimioterapia
en combinación con ICIs, incluyendo el IMpower132
(28), la parte 2 del CheckMate 22736 y el IMpower131
(34). En el estudio Impower132, la adición del atezolizumab a la
quimioterapia con platino más pemetrexed
impactó la PFS vs. la quimioterapia sola (7,6 meses
vs. 5,2 meses, HR 0,60 IC 95% 0,49-0,72; P<0,0001)
sin modificar significativamente la OS (18.1 meses vs.
13,6 meses, HR 0,81 IC 95% 0,64-1,03; P=0,0797) al
término del seguimiento (la OS final aún se encuentra
pendiente) (28). Así mismo, la parte 2 del CheckMate
227 no encontró un impacto positivo con la combinación de nivolumab más
quimioterapia vs. la quimioterapia sola en los pacientes con histología
no escamosa
(18,8 meses vs. 15,6 meses, HR 0,86 IC 95% 0,69-1,08;
P=0,1859), aunque un análisis exploratorio demostró impacto con la
combinación en los pacientes con
PD-L1 ≥50% (HR 0,56) (36). Por otra parte, el estudio
IMpower131, probó la combinación de atezolizumab
más quimioterapia en 1.021 pacientes con CPCNP de
patrón escamoso sin modificar la OS al comparar con
la quimioterapia sola (14,2 meses vs. 13,5 meses, HR
0,88 IC 95% 0,73-1,05; P= 0,16). Como excepción,
el IMpower131 demostró superioridad para el brazo
experimental respecto de la OS en el subgrupo de pacientes con alta
expresión de PD-L1 (HR 0,48 IC 95%
0,29-0,81) (34). La Figura 3 ilustra las opciones de tratamiento para
los pacientes con CPCNP sin blancos
moleculares potencialmente modulables.
Interrogantes abiertos
Globalmente, los datos apoyan el hecho de que los
ICIs son el nuevo tratamiento estándar en los pacientes con CPCNP
avanzado, independiente del subtipo histológico y de la expresión de
PD-L1, siendo la
estrategia en combinación la más adecuada para los
tumores con PD-L1 negativo (43). Sin embargo, aún
existe controversia alrededor del mejor manejo para
aquellos con un PD-L1 ≥50%, ya que ninguno de los
experimentos comparó de forma directa el uso de un
ICI más quimioterapia vs. la monoterapia con un ICI.
La comparación indirecta entre los estudios mostró
desenlaces similares respecto de la OS entre los pacientes con PD-L1 ≥
50%, con perfiles de toxicidad
diferentes, sugiriendo por el momento que la monoterapia con
pembrolizumab puede ser la opción más
razonable para esta población. El estudio EA5163/
S1709 está valorando si la inducción con pembrolizumab es superior a la
combinación de pemetrexed más
platino y pembrolizumab en pacientes con tumores no
escamosos avanzados. Dicho experimento se estratificará de acuerdo al
nivel de expresión del PD-L1 (≥50%
vs. 1-49%) para poder elucidar la mejor estrategia. El
uso de otros biomarcadores y su utilidad para subseleccionar a los
pacientes con base en la genómica sigue
siendo un área plena de incertidumbre, en especial, si
se consideran algunas alteraciones que favorecen la resistencia
intrínseca (STK11 y KEAP1) o una mayor
sensibilidad a la inmunoterapia (ARID1A). Por el momento, los
resultados han sido variables y continúan
sin confirmación prospectiva.
Finalmente, la duración óptima del tratamiento permanece indefinida.
Basándose en los datos del estudio CheckMate 153, el tratamiento con
ICI debería continuar por más de un año (44). No obstante, para
aquellos pacientes que completaron el número de ciclos por
protocolo y progresaron, la reinducción con los ICIs
puede brindar un beneficio clínico en cerca del 80% de
los casos (9). Actualmente, no hay parámetros definidos
para definir cuales sujetos podrían ser candidatos para
continuar una estrategia de supresión y reinducción.
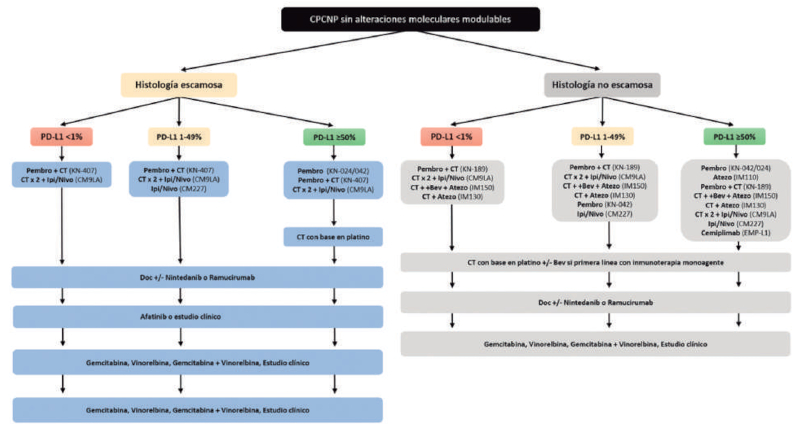
Figura 3. Opciones de tratamiento para los pacientes con CPCNP sin
blancos moleculares potencialmente
modulables según la información obtenida de los experimentos clínicos
fase 3 descritos.
Referencias
1. Garon EB. Hellmann MD. Rizvi NA.
Carcereny E. Leighl
NB. Ahn MJ et al. Five-Year Overall Survival for Patients
With Advanced Non‒Small-Cell Lung Cancer Treated
With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study. J Clin
Onccol, 2019;37(28):2518-
25234
2. Faivre-Finn C, Vicente D. Kurata
T. Planchard D. PazAres L, Vansteenkiste J et al. LBA49 Durvalumab
after
chemoradiotherapy in stage III NSCLC: 4-year survival
update from the phase III PACIFIC trial. Ann Oncol,
2020;31:S1178-S11781
3. Provencio M. Nadal E. Insa A.
García-Campelo M. Casal-Rubio J. Dómine M et al. Neoadjuvant
chemotherapy
and nivolumab in resectable non-small-cell lung cancer
(NADIM): an open-label. Multicentre, single-arm. Phase
2 trial. Lancet Onco24, 2020;21(11):1413-14-8
4. Benitez JC. Remon J. Besse B.
Current Panorama and
Challenges for Neoadjuvant Cancer Immunotherapy.
Clin Cancer Res, 2020;26(19):5068-50755
5. Teixido C. Reguart N, Using
biomarkers to determine optimal combinations with immunotherapy
(biomarker discovery perspective). Future OnEngl, 2020;16(23):1677-
1671
6. Tsao MS. Kerr KM. Kockx M. Beasley
MB. Borczuk AC.
Botling J et al. PD-L1 Immunohistochemistry Comparability Study in
Real-Life Clinical Samples: Results of Blueprint Phase 2 Project. J
Thorac Oncer, 2018;13(9):1302-
13113
7. Aguilar EJ. Ricciuti B. Gainor JF.
Kehl KL. Kravets S.
Dahlberg S et al. Outcomes to first-line pembrolizumab
in patients with non-small-cell lung cancer and very high
PD-L1 expression. Ann Oncol, 2019;30(10):1653-1688.
8. Reck M. Rodríguez-Abreu D.
Robinson AG. Hui R.
Csőszi T. Fülöp A et al. Pembrolizumab vs. Chemotherapy for
PD-L1-Positive Non-Small-Cell Lung Cancer. N
Engl J Med, 2016;375(19):1823-1874
9. Brahmer JR. Rodriguez-Abreu D.
Robinson AG. Hui
R. Csőszi T. Fülöp A et al. KEYNOTE-024 5-year OS
update: First-line (1L) pembrolizumab (pembro) vs platinum-based
chemotherapy (chemo) in patients (pts) with
metastatic NSCLC and PD-L1 tumour proportion score
(TPS) ≥50%. Ann Oncol, 2020;31:S1181-S11884
10. Mok TSK, Wu Y-L. Kudaba I.
Kowalski D. Cho B, Turna
H et al. Pembrolizumab vs. chemotherapy for previously
untreated. PD-L1-expressing. Locally advanced or metastatic
non-small-cell lung cancer (KEYNOTE-042): a
randomised. Open-label. Controlled. Phase 3 trial. LancEngl,
2019;393(10183):1819-183-7
11. Mok TSK, Wu Y-L. Kudaba I.
Kowalski D. Cho B, Turna
H et al. Final analysis of the phase III KEYNOTE-042
study: Pembrolizumab (Pembro) vs. platinum-based
chemotherapy (Chemo) as first-line therapy for patients
(Pts) with PD-L1–positive locally advanced/metastatic
NSCLC. Ann Oncol, 2019;30:i363
12. Herbst RS. Giaccone G. De Marinis
F. Reinmuth N,
Vergnenegre A. Barrios CH et al. Atezolizumab for FirstLine Treatment
of PD-L1-Selected Patients with NSCLC.
N Engl J Med, 2020;383(14):1328-13346
13. Sezer A. Kilickap S. Gümüş M.
Bondarenko I, Özgüroglu
M. Gogishvili M et al. LBA52 EMPOWER-Lung 1: Phase
III first-line (1L) cemiplimab monotherapy vs platinumdoublet
chemotherapy (chemo) in advanced non-small
cell lung cancer (NSCLC) with programmed cell deathligand 1 (PD-L1)
≥50%. Ann Oncol, 2020;31:S1182-
S11885
14. Brahmer JR. Rodríguez-Abreu D.
Robinson AG. Hui R.
Csőszi T. Fülöp A et al. Health-related quality-of-life results for
pembrolizumab vs. chemotherapy in advanced.
PD-L1-positive NSCLC (KEYNOTE-024): a multicentre.
International. Randomised. Open-label phase 3 trial.
Lancet Oncol, 2017;18(12):1600-160-3
15. Carbone DP. Reck M. Paz-Ares L.
Creelan B. Horn L,
Steins M et al. First-Line Nivolumab in Stage IV or Recurrent
Non-Small-Cell Lung Cancer. N Engl J Med,
2017;376(25):2415-2493
16. Rizvi NA. Cho BC. Reinmuth N. Lee
KH. Luft A. Ahn
MJ et al. Durvalumab With or Without Tremelimumab
vs Standard Chemotherapy in First-line Treatment of
Metastatic Non-Small Cell Lung Cancer: The MYSTIC Phase 3 Randomized
Clinical Trial. JAMA Oncol,
2020;6(5):661-6737
17. Ramalingam SS. Ciuleanu TE.
Pluzanski A. Lee J,
Schenker M. Bernabe-Caro R et al. Nivolumab + ipilimumab vs.
platinum-doublet chemotherapy as firstline treatment for advanced
non-small cell lung cancer:
Three-year update from CheckMate 227 Part 1. J Clin
Oncol, 2020;38(15_suppl):9500-9500
18. Hellmann MD. Paz-Ares L. Bernabe
Caro R, Zurawski B.
Kim S. Carcereny-Costa E et al. Nivolumab plus Ipilimumab in Advanced
Non-Small-Cell Lung Cancer. N Engl J
Med, 2019;381(21):2020-20331
19. Ready N. Hellmann MD. Awad MM.
Otterson GA. Gutierrez M. Gainor JF et al. First-Line Nivolumab Plus
Ipilimumab in Advanced Non-Small-Cell Lung Cancer
(CheckMate 568): Outcomes by Programmed Death Ligand 1 and Tumor
Mutational Burden as Biomarkers. J
Clin Onccol, 2019;37(12):992-1042
20. Hellmann MD. Ciuleanu T-E.
Pluzanski A. Lee JS. Otterson GA. Audigier-Valette C et al. Nivolumab
plus Ipilimumab in Lung Cancer with a High Tumor Mutational
Burden. N Engl J Med, 2018;378(22):2093-2146
21. Marabelle A. Fakih M. Lopez J,
Shah M, Shapira-Frommer
R. Nakagawa K et al. Association of tumour mutational burden with
outcomes in patients with advanced solid tumours
treated with pembrolizumab: prospective biomarker analysis of the
multicohort. Open-label. Phase 2 KEYNOTE-158
study. Lancet Oncol, 2020;21(10):1353-13-9
22. Ramalingam SS. Ciuleanu TE.
Pluzanski A. Lee J,
Schenker M. Bernabe-Caro R et al. Nivolumab + ipilimumab vs.
platinum-doublet chemotherapy as firstline treatment for advanced
non-small cell lung cancer:
Three-year update from CheckMate 227 Part 1. J Clin
Oncol, 2020;38(15_suppl):9500-9500
23. Ferrara R. Facchinetti F.
Calareso G. Kasraoui I, Signorelli D. Proto C et al. Hyperprogressive
disease (HPD)
upon first-line PD-1/PD-L1 inhibitors (ICI) as single agent
or in combination with platinum-based chemotherapy in
non-small cell lung cancer (NSCLC) patients (pts). Ann
Oncol, 2020;31:S892
24. Gandhi L. Rodríguez-Abreu D.
Gadgeel S. Esteban E.
Felip E. De Angelis F et al. Pembrolizumab plus Chemotherapy in
Metastatic Non-Small-Cell Lung Cancer. N
Engl J Med, 2018;378(22):2078-2005
25. Rodriguez-Abreu D. Powell SF.
Hochmair M. Gadgeed
SM. Esteban E. Felip E. Et al. Final analysis of KEYNOTE-189:
Pemetrexed-platinum chemotherapy (chemo) with or without pembrolizumab
(pembro) in patients
(pts) with previously untreated metastatic nonsquamous
non-small cell lung cancer (NSCLC). J Clin Oncol,
2020;38(15_suppl):9582-9582
26. Socinski MA. Jotte RM. Cappuzzo
F. Orlandi F, Stroyakovskiy D. Nogasmi N et al. Atezolizumab for
FirstLine Treatment of Metastatic Nonsquamous NSCLC. N
Engl J Med, 2018;378(24):2288-2348
27. Reck M. Mok TSK. Nishio M. Jotte
R. Cappuzzo F. Orlandi F et al. Atezolizumab plus bevacizumab and
chemotherapy in non-small-cell lung cancer (IMpower150):
key subgroup analyses of patients with EGFR mutations or baseline liver
metastases in a randomised. Open-label phase 3 trial. Lancet Respir
Med, 2019;7(5):387-4-0
28. Papadimitrakopoulou V. Cobo M.
Bordoni R. Bordoni
R. Dubray-Longeras P Szalai Z et al. IMpower132: PFS
and Safety Results with 1L Atezolizumab + Carboplatin/
Cisplatin + Pemetrexed in Stage IV Non-Squamous NSCLC. J Thorac Oncol,
2018;13(10):S332-S362
29. West H. McCleod M. Hussein M.
Morabito A. Rittmeyer
A. Conter HJ et al. Atezolizumab in combination with
carboplatin plus nab-paclitaxel chemotherapy compared with chemotherapy
alone as first-line treatment for
metastatic non-squamous non-small-cell lung cancer
(IMpower130): a multicentre. Randomised. Open-label.
Phase 3 trial. Lancet Oncol, 2019;20(7):924-9-6
30. Yang Y, Wang Z. Fang J, Yu Q. Han
B. Cang S et al. Efficacy and Safety of Sintilimab Plus Pemetrexed and
Platinum
as First-Line Treatment for Locally Advanced or Metastatic Nonsquamous
NSCLC: a Randomized. Double-Blind.
Phase 3 Study (Oncology pRogram by InnovENT antiPD-1-11). J Thorac
Oncer, 2020;15(10):1636-1614
31. Lu S, Yu Y, Yu X. Hu Y. Ma Z. Li
X et al, Tislelizumab + chemotherapy vs chemotherapy alone as
first-line treatment
for locally advanced/metastatic nonsquamous NSCLC.
Ann Oncol, 2020;31:S816-S877
32. Paz-Ares L. Luft A, Vicente D,
Tafreshi A. Gümüs M.
Mazières J et al. Pembrolizumab plus Chemotherapy for
Squamous Non-Small-Cell Lung Cancer. N Engl J Med,
2018;379(21):2040-2065
33. Paz-Ares L, Vicente D, Tafreshi
A. Robinson A, Soto
Parra H. Mazières J et al. Pembrolizumab (pembro) +
chemotherapy (chemo) in metastatic squamous NSCLC: Final analysis and
progression after the next
line of therapy (PFS2) in KEYNOTE-407. Ann Oncol,
2019;30:v918-v980
34. Jotte R. Cappuzzo F, Vynnychenko
I, Stroyakovskiy D.
Rodríguez-Abreu D. Hussein M et al. Atezolizumab in
Combination With Carboplatin and Nab-Paclitaxel in
Advanced Squamous NSCLC (IMpower131): Results
From a Randomized Phase III Trial. J Thorac Oncer,
2020;15(8):1351-1328
35. Wang J. Lu S. Hu C, Sun Y, Yang
K. Chen M et al, Updated analysis of tislelizumab plus chemotherapy vs
chemotherapy alone as first-line treatment of advanced
squamous non-small cell lung cancer (SQ NSCLC). Ann
Oncol, 2020;31:S878
36. Paz-Ares L. Ciuleanu TE, Yu X,
Salman P. Pluzanski
A. Nagrial A et al. Nivolumab (NIVO) + platinum-doublet chemotherapy
(chemo) vs chemo as first-line (1L)
treatment (tx) for advanced non-small cell lung cancer
(aNSCLC): CheckMate 227 - part 2 final analysis. Ann
Oncol, 2019;30:xi67-xi04
37. Reck M. Ciuleanu T-E. Dols MC,
Schenker M, Zurawski
B. Menezes J et al. Nivolumab (NIVO) + ipilimumab (IPI)
+ 2 cycles of platinum-doublet chemotherapy (chemo) vs
4 cycles chemo as first-line (1L) treatment (tx) for stage
IV/recurrent non-small cell lung cancer (NSCLC): CheckMate 9LA. J Clin
Oncol, 2020;38(15_suppl):9501-9501
38. Garassino M. Rodriguez-Abreu D.
Gadgeel S. Esteban
E. Felip E, Speranza G et al. Evaluation of TMB in KEYNOTE-189:
Pembrolizumab Plus Chemotherapy vs Placebo Plus Chemotherapy for
Nonsquamous NSCLC. J
Thorac Oncol, 2019;14(10):S216-S227
39. Garassino MC. Gadgeel SM.
Rodriguez-Abreu D. Felip E. Esteban E, Speranza G et al. Evaluation of
blood
TMB (bTMB) in KEYNOTE-189: Pembrolizumab (pembro) plus chemotherapy
(chemo) with pemetrexed and
platinum vs. placebo plus chemo as first-line therapy
for metastatic nonsquamous NSCLC. J Clin Oncol,
2020;38(15_suppl):9521-9521
40. Socinski MA. Mok TS. Nishio M.
Jotte RM. Cappuzzo F.
Orlandi F et al. IMpower150 final analysis: Efficacy of atezolizumab
(atezo) + bevacizumab (bev) and chemotherapy in first-line (1L)
metastatic nonsquamous (nsq) nonsmall cell lung cancer (NSCLC) across
key subgroups.
Cancer Res, 2020;80(16 Supplement):CT216
41. Reck M. Mok T, Socinski MA. Jotte
R. Lim D. Cappuzzo F
et al. IMpower150: Updated efficacy analysis in patients
with EGFR mutations. Ann Oncol, 2020;31:S837-S807
42. Mazieres J. Kowalski D. Luft A,
Vicente D, Tafreshi A.
Gümüs M et al. Health-Related Quality of Life With
Carboplatin-Paclitaxel or nab-Paclitaxel With or Without Pembrolizumab
in Patients With Metastatic Squamous Non-SmallCell Lung Cancer. J Clin
Onccol, 2020;38(3):271-248
43. Borghaei H. Langer CJ. Paz-Ares
L. Rodríguez-Abreu
D. Halmos B. Garassino MC et al. Pembrolizumab plus
chemotherapy vs. chemotherapy alone in patients with
advanced non-small cell lung cancer without tumor PDL1 expression: A
pooled analysis of 3 randomized controlled trials. Cancer,
2020;126(22):4867-4842
44. Waterhouse DM. Garon EB. Chandler
J. McCleod M.
Hussein M. Jotte R et al. Continuous Vs. 1-Year FixedDuration Nivolumab
in Previously Treated Advanced
Non-Small-Cell Lung Cancer: CheckMate 153. J Clin
Onc10, 2020;38(33):3863-3831.
Recibido:
Marzo 09, 2021
Aprobado: Marzo 10, 2021
Correspondencia:
Jordi Remon
jremon@hmhospitales.com





