Resúmen
El cáncer de mama es la neoplasia más común entre las
mujeres y representa un problema global para
la salud pública. De acuerdo con estimaciones realizadas por la
Organización Mundial de la Salud ,
en el año 2018 hubo a nivel mundial 2.1 millones casos nuevos y 627.000
muertes causadas por cáncer
de mama. Historicamente el primer tratamiento considerado para cáncer
de mama era quirúrgico. Si
bien la estratificación histológica sigue siendo una práctica común,
los avances tecnológicos han desentrañado más complejidades con la
aparición de al menos cinco subtipos moleculares distintos. Sobre
esta base, los análisis combinados genómico/transcriptómico de cánceres
de mama han dado como
resultado la identificación de diez subtipos distintos de cáncer de
mama basados en grupos integrados.
En línea con estos avances, también se han realizado esfuerzos para
segregar aún más algunos de los
subtipos histológicos establecidos para los cánceres de mama
ER-negativos y triple negativos. En este
artículo se presenta la evolución del manejo del cáncer de mama a la
luz de los nuevos avances en el
diagnóstico de la enfermedad.
Palabras clave: Cáncer de mama; tratamiento médico;
terapia hormonal; receptor; terapia dirigida.

¹ Grupo Oncología Clínica y Traslacional, Instituto de Oncología,
Colsánitas, Bogotá, Colombia. Investigador Asociado ONCOLGroup.
Fundación para la Investigacion Clínica y Molecular Asociada al Cáncer
FICMAC.
BREAST CANCER: FROM SURGERY AND TAMOXIFEN
TO TARGETED THERAPY IN PATIENTS WITH HER2
POSITIVE AND LUMINAL TUMORS
Abstract
Breast cancer is the most common neoplasm among women
and represents a global problem
for public health. According to estimates made by the World Health
Organization, in 2018,
there were 2.1 million new cases worldwide and 627,000 deaths caused by
breast cancer,
Historically the first treatment considered for breast cancer was
surgical. Although histological
stratification remains a common practice, technological advances have
unraveled more complexities with the emergence of at least five
different molecular subtypes. This combined genomic/transcriptomic
analysis of breast cancers has identified ten distinct subtypes of
breast
cancer based on integrated clusters. In accord with these advances,
efforts have also been
made to further segregate some of the established histologic subtypes
for ER-negative and
triple-negative breast cancers. This article presents the evolution of
breast cancer management in the light of new advances in diagnosing the
disease.
Keywords: Breast cancer; medical treatment; hormonal
therapy; receptor; targeted therapy.
Epidemiología
El cáncer de mama (CM) es la neoplasia más común
entre las mujeres y representa un problema global para
la salud pública (1). De acuerdo con estimaciones
realizadas por la Organización Mundial de la Salud
(OMS), en el año 2018 hubo a nivel mundial 2.1 millones casos nuevos y
627.000 muertes causadas por
CM, mientras la prevalencia alcanzó los 4.4 millones
de casos (1). Más de la mitad de los casos de cáncer de
mama los casos ahora se diagnostican en países de bajos y medianos
ingresos, donde una mayor proporción
de casos (y a veces una marcada mayor proporción)
son diagnosticados en etapas avanzadas, que están
vinculadas a peor supervivencia (2). El riesgo de desarrollar CM
durante la vida es del 5% (1 de cada 5-7
mujeres) y la posibilidad de morir por la enfermedad
después del diagnóstico es cercana al 30% (2,3).
En Colombia la tasa de incidencia anual estimada para
el CM es de 36/100.000 mujeres, cifra inferior a la documentada en los
países del primer mundo (3). En relación con la mortalidad, el CM ocupa
el tercer lugar
en el país, valor precedido únicamente por el cáncer de
cérvix y las neoplasias gástricas (4). En nuestro entorno
la distribución geográfica de la mortalidad muestra un
mayor riesgo para las mujeres que viven en las capitales
departamentales, hallazgo que se puede asociar al nivel
de urbanización, por la disminución en la fecundidad y
con el sedentarismo. La tendencia de la mortalidad por
CM en el país es creciente durante los últimos años (5,6)
a pesar de que en algunas ciudades, y específicamente
en Bogotá se observa un descenso (7).
Evolución del tratamiento quirúrgico
de CM
Historicamente el primer tratamiento considerado
para CM era quirúrgico, La medicina greco-latina se
apunta a la cirugía de mama, a través de todo su recorrido, desde el
Corpus Hippocraticum hasta el siglo
I
d.C., en el que Celso hace una mención de este tema
en su obra y Leónidas describe concisamente la técnica de la
mastectomía asociada a la cauterización (11)
y es la radicalidad el eje fundamental del tratamiento quirúrgico hasta
mediados del siglo XX. Halsted,
fue quien primero realizó una mastectomía radical en
1882, publicó sus resultados en 1894 (12). El enfoque
halstediano siguió siendo el estándar de oro para el
tratamiento quirúrgico de CM durante casi 80 años.
Durante los últimos 30 años, la gestión quirúrgica del
CM ha pasado de enfoques radicales a procedimientos menos extremos para
conservar la mama, aunque
recientemente ha sido una tendencia de aumento de
las tasas de mastectomía para casos inciertos (13). La
evolución hacia procedimientos menos radicales ha
sido evaluado con toda la rigurosidad necesaria. Un
ensayo aleatorio, NSABP B-04, que comenzó en 1971,
comparó la mastectomía radical sin radiación vs. mastectomia simple con
radiación vs. mastectomía simple
sin radiación, reclutaron a 1.765 pacientes durante 126
meses, y la aleatorización se basó en parte en el estado
ganglionar, con pacientes con enfermedad con ganglios linfáticos
“clínicamente” positivos asignados al
azar a mastectomía radical o mastectomía simple con
radiación. Los pacientes con ganglios “clínicamente”
negativos fueron asignados aleatoriamente a cualquiera de los 3 grupos.
No se observaron diferencias de
supervivencia, sobrevida libre de enfermedad o sobrevida libre de
enfermedad a distancia, y este estudio
marcó el fin de la la mastectomía radical como base
para el tratamiento quirúrgico del CM(14).
Otro ensayo, NSABP B-06, incluyó una comparación
aleatoria de mastectomía frente a tumorectomía sola
frente a tumorectomía con radiación para pacientes
que tenían enfermedad en estadio I o II con tumores
de menos de 4 cm. En total, se incluyeron 2.163 mujeres desde 1976
hasta 1984, con disección axilar que
se realizó en todos los grupos. El seguimiento de 20
años de 1.851 pacientes se publicó en 2002. No hubo
diferencias en la supervivencia general, pero si diferencias
significativas en la recurrencia, con los grupos
de tumorectomía sola con una tasa del 39,2% de recurrencia a los 20
años (15). Por lo tanto, el estándar del
cuidado de la cirugía conservativa de la mama se ha
convertido en cuadrantectomía más radioterapia. Las
contraindicaciones absolutas para la tumorectomía
incluyen radioterapia previa, embarazo, tumor multicéntrico,
incapacidad para obtener márgenes claras
(tumor grande o invasión a estructuras adyacentes), e
incapacidad física para tolerar la radioterapia. Las contraindicaciones
relativas incluyen tumor multifocal,
enfermedad del tejido conectivo (16) y una gran cantidad de tumores en
relación al tamaño de la mama. Las
recurrencias deben ser manejadas con mastectomía.
El estado de los ganglios linfáticos axilares (ALN) determina la
necesidad de radioterapia y terapia sistémica adyuvante. La disección
de ALN en el momento de la cirugía fue la atención estándar hasta la
década de
1990, pero a menudo resultó en dolor, entumecimiento, edema y
disminución de la movilidad en el brazo
afectado. En pacientes con ganglios clínicamente negativos, una biopsia
intraoperatoria de ganglio linfático centinela (SLN) negativa descarta
la necesidad de
disección de ALN.
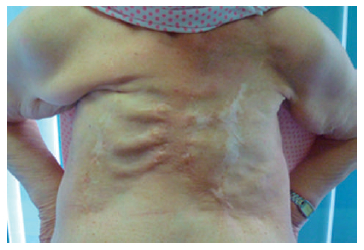
Figura 1. Paciente con mastectomia suprarradical
derecha y mastectomia radical izquierda por cáncer
de mama bilateral metacrónico (Cortesía Dra María
Claudia Ramírez)
La biopsia de SLN reduce los síntomas del brazo en
comparación con la disección de ALN. La biopsia del
GLC tiene una sensibilidad de 95 a 100%, una tasa de
falsos negativos del 5,5% (17), y un valor predictivo
negativo del 98%. Un análisis prospectivo proporciona
evidencia de que las pacientes con cáncer de mama en
estadio temprano que tienen un SLN negativo tienen
una mejor supervivencia libre de enfermedad y en general en comparación
con las pacientes que tienen una
disección de ALN negativa (18). Esto es más probable
debido a una estadificación axilar más precisa en pacientes del grupo
de SLN. La disección de ALN está
indicada para todas las mujeres con ganglios linfáticos
palpables o un SLN positivo.
Evolución del tratamiento sistémico
de CM
Si bien la estratificación histológica sigue siendo una
práctica común, los avances tecnológicos han desentrañado más
complejidades con la aparición de al menos cinco subtipos moleculares
distintos (Luminal A,
Luminal B, Basal, HER2 enriquecido Clowdin Low)
(8). Sobre esta base, los análisis combinados genómico/
transcriptómico de cánceres de mama han dado como
resultado la identificación de diez subtipos distintos
de cáncer de mama basados en grupos integrados (9).
En línea con estos avances, también se han realizado
esfuerzos para segregar aún más algunos de los subtipos histológicos
establecidos para los cánceres de mama
ER-negativos y triple negativos. Estos estudios han identificado al
menos cuatro subtipos distintos de cáncer de
mama ER negativo y seis subtipos de cáncer de mama
triple negativo, respectivamente (10). El progreso realizado en estas
áreas destaca la intrincada complejidad
de los subtipos de cáncer de mama y es probable que en
el futuro se descubran caracterizaciones más definidas
y precisas basadas en nuevos parámetros (por ejemplo,
metabolitos). Sin embargo, cabe destacar que existe una
brecha entre los métodos de investigación y la práctica
clínica actual. Aunque la subtipificación intrínseca del
CM se ha empleado en el ámbito de la investigación
durante más de dos décadas.
Con la experiencia acumulada a lo largo de los años se
ha evidenciado que no todos los CM tienen un comportamiento similar
desde el punto de vista clínico, ya que
las pacientes tienden a presentar respuestas diferentes
frente a los tratamientos y resultados variables, a pesar
de ser diagnosticadas en idéntico estadio tumoral. A
raíz de ello, se ha buscado introducir la información
molecular en clasificación clínica (sistema TNM) para
determinar el pronóstico y planificar el tratamiento de
forma individualizada (19). En la práctica, la información necesaria
para identificar el subtipo molecular se
obtienen antes de la cirugía, mediante el análisis inmunohistoquímico
de la muestra histológica obtenida en
la biopsia generalmente mediante aguja trucut . Asimismo, la
determinación del genotipo tumoral resulta
de gran utilidad en las pacientes con cáncer de mama
infiltrante en estadio precoz, proporciona información
sobre la probabilidad de recidiva y, por tanto, sobre la
conveniencia o no de recibir quimioterapia adyuvante.
Los tumores se pueden clasificar en subtipos que se
distinguen por diferencias dominantes de los patrones
de expresión genética (8) y estos subtipos se pueden
inferir mediante el estudio de inmunohistoquímica de
receptores hormonales, HER2 y KI 67.
El subtipo Luminal A Representa más del 50% de los
CM, suele ser de grado histológico bajo y su pronóstico es el más
favorable de todos, con una supervivencia
a los 5 años mayor del 80% (20). El porcentaje de tumores multifocales
y multicéntricos es del 30-44% y el
9-37%, respectivamente. Las metástasis tienden a afectar con
preferencia al hueso, el subtipo Luminal B. Su
incidencia media es del 15%. Inicialmente se describían tasas de
supervivencia a los 5 años del 40% (20).
Terapia de primera línea HER2 positivo
El receptor 2 del factor de crecimiento epidérmico humano (HER2) se ha
identificado en aproximadamente
el 20% de todos los pacientes con CM y corresponde
a tumores de grado histológico intermedio o alto, con
tendencia a ser multifocales. Su supervivencia a los 5
años era del 31% antes de la introducción del trastuzumab. Las
metástasis tienen predilección por el hueso,
el cerebro, el hígado y el pulmón (21).
En los últimos 20 años, múltiples agentes anti-HER2
abarcan una serie de clases de fármacos incorporados
a la práctica clínica, incluidos los anticuerpos monoclonales
(trastuzumab y pertuzumab), los inhibidores de la
tirosina quinasa intracelular de molécula pequeña (lapatinib y
neratinib) y el fármaco de anticuerpos conjugado
(ADC) ado-trastuzumab emtansina (T-DM1) (22).
El resultado del primer ensayo clínico de fase III proporcionado por
Slamon
et al. (23) en 2001,
demostró
que trastuzumab aumentó el beneficio clínico de la quimioterapia de
primera línea en MBC que sobreexpresa
HER2. Los pacientes con CMM HER2 positivo se dividieron al azar en dos
grupos en la terapia de primera
línea, uno fue quimioterapia con trastuzumab (n = 235)
y el otro fue quimioterapia sola (n = 234). Una mejora significativa en
el tiempo hasta la progresión (TTP)
(7,4 frente a 4,6 meses; P <0,001) y SG (25,1 vs.20,3 meses; P =
0,01) se había obtenido con una mediana de
seguimiento de 30 meses. El evento adverso más importante fue la
disfunción cardíaca (23).
Luego, se probó trastuzumab en combinación con varios medicamentos de
quimioterapia. Robert y
col.
asignaron al azar a 196 pacientes a trastuzumab y paclitaxel con o sin
carboplatino. Sin embargo, la adición de
carboplatino al paclitaxel y trastuzumab mejoró la tasa
de respuesta objetiva (TRO) (52% frente al 36%) y la
SLP (10,7 frente a 7,1 meses) en mujeres con cáncer de
mama mestastásico (CMM) HER2 positivo, sin diferencias significativas
en la SG (35,7 frente a 32,2 meses,
(P = 0,76) y se observó mas toxicidad hematológica (24).
De manera similar, el estudio 007 del Breast Cancer
International Research Group (BCIRG) evaluó trastuzumab y docetaxel con
o sin carboplatino, y encontró
que la adición de carboplatino no mejora la actividad
antitumoral (25).
Dos ensayos de fase III compararon trastuzumab
más taxano o vinorelbina como terapia de primera
línea. Los tratamientos con trastuzumab / taxano y
trastuzumab / vinorelbina fueron eficaces y tolerables
para las pacientes CMM HER2 positivo. Y ambos esquemas pueden
considerarse como una opción alternativa de tratamiento de primera
línea (26,27).
Pertuzumab es un anticuerpo monoclonal humanizado recombinante que se
une a un epítope de HER2
diferente al trastuzumab (28), en el ensayo de fase III
CLEOPATRA, pertuzumab se agregó al estándar de
tratamiento de primera línea de docetaxel más trastuzumab; pacientes
con CMM HER2 positivo se aleatorizaron para recibir trastuzumab más
docetaxel más
placebo (grupo de control) o trastuzumab más docetaxel más pertuzumab
(grupo de pertuzumab) como
terapia de primera línea. La mediana de la SLP evaluada de forma
independiente para la adición de pertuzumab se prolongó en 6,1 meses
(12,4 frente a 18,5 meses,
P <0,001) (29). Los resultados finales preespecificados
de SG con una mediana de seguimiento de 50 meses
informaron 56,5 meses en el grupo de pertuzumab y
mejoraron significativamente en comparación con
40,8 meses en el grupo de control (P <0,001) (30).
El ensayo MARIANNE ( 31) mostró que el grupo de
T-DM1 y el grupo de T-DM1 más pertuzumab tenían
una SLP no inferior en comparación con trastuzumab más taxano (T-DM1,
14,1 meses; T-DM1 más pertuzumab, 15,2 meses; trastuzumab más taxano,
13,7 meses).
y ninguno de los brazos experimentales mostró superioridad en la SLP a
trastuzumab más taxano para el tratamiento de primera línea de CMM HER2
positivo. La
incidencia de eventos adversos de grado ≥3 fue significativamente mayor
en el grupo de trastuzumab más
taxano (54,1%) que en el grupo de T-DM1 (45,4%) y
el grupo de T-DM1 más pertuzumab (46,2%). En los
brazos de T-DM1, hubo menos pacientes que interrumpieron el tratamiento
debido a eventos adversos
Por lo tanto, actualmente pertuzumab, trastuzumab
más docetaxel es el tratamiento estándar en la terapia
de primera línea para CMM HER2 positivo, T-DM1
puede ser una alternativa.
Terapia de segunda línea HER2
positivo
Las opciones terapéuticas basadas en evidencia incluyen la continuación
de trastuzumab con un compañero de quimioterapia diferente. El ensayo
de fase III del
estudio German Breast Group 26 (32) demostró que
la continuación de trastuzumab más capecitabina tuvo
una mejora significativa en la respuesta general y TTP
en comparación con capecitabina sola en pacientes
con cáncer de mama HER-2 positivo que tuvieron progresión durante el
tratamiento con trastuzumab, pero
la diferencia de SG no fue estadísticamente significativa (25,5 frente
a 20,4 meses, P = 0,257).
El lapatinib es un inhibidor de la tirosina quinasa de
pequeña molécula dirigida al receptor del factor de crecimiento
epidérmico (EGFR) y HER2 disponible por
vía oral. El estudio MA.31 (33) comparó lapatinib con
trastuzumab, ambos combinados con un taxano en primera línea
metastásica demostró que lapatinib con la
terapia con taxanos se asocia con una SLP más corta
en comparación con trastuzumab con taxano . Pero,
lapatinib más capecitabina es una opción para los pacientes que
progresaron con trastuzumab. Un ensayo de
fase III de Geyer
et al. (34)
comparando lapatinib más
capecitabina vs. capecitabina sola en pacientes que habían progresado
con un tratamiento previo basado en
trastuzumab, se encontró que había una mejoría significativa en la SLP
(8,4
vs. 4,4 meses, P
<0,001). Aunque
la terminación prematura de la inclusión y el posterior
cruce resultaron en un poder insuficiente para detectar
diferencias en la SG, los análisis exploratorios finales
demostraron una tendencia hacia una ventaja de supervivencia con
lapatinib más capecitabina.
T-DM1 es un conjugado de anticuerpo dirigido contra HER2 y emtamsine
(antineoplásico DM1) que
incorpora las propiedades antitumorales de trastuzumab dirigidas a HER2
con la actividad citotóxica del
agente inhibidor de microtúbulos. El ensayo EMILA
(35), que comparó T-DM1 y lapatinib-capecitabina
para pacientes que habían sido tratados previamente
con trastuzumab y taxano, informó una ventaja de SG
estadísticamente significativa a favor de T-DM1 en el
segundo análisis intermedio en el año 2012, llevó al
registro y rápida adopción clínica de T-DM1. En 2017,
el análisis final de EMILA mostró que la mediana de
SG fue más prolongada con T-DM1 que con lapatinib-capecitabina (29,9
vs.25,9 meses), aunque 136
(27%) de 496 pacientes pasaron del control a T-DM1,
después del segundo análisis de supervivencia global
provisional. Además, las tasas de eventos adversos de
grado 3 o 4 fueron numéricamente más altas en lapatinib más
capecitabina frente a T-DM1 (57% frente
a 41%). Pero, la trombocitopenia y el aumento de los
niveles séricos de aminotransferasas fueron mas frecuente para los
pacientes que recibieron T-DM1.
Por lo tanto, en la actualidad, T-DM1 es el tratamiento estándar en la
terapia de segunda línea para CMM
HER2 positivo.
Rara vez se informa sobre un ensayo de fase III para
la terapia anti-HER2 en el entorno de tercera línea. En
el estudio TH3RESA (36), incluyó pacientes (n = 602)
tratados previamente con trastuzumab, lapatinib, un taxano y con
progresión en dos o más regímenes dirigidos por HER2 en enfermedad
avanzada. Los pacientes
fueron aleatorizados en una forma 2: 1 a T-DM1 y la
elección de la terapia por parte del médico. En el punto
de corte de los datos, el 47% de los pacientes del grupo
de elección del médico habían pasado a T-DM1. La SG
fue significativamente más prolongada con T-DM1 en
comparación con el tratamiento control elegido por el
médico (22,7 frente a 15,8 meses, P = 0,0007).
Nuevos agentes en anti-HER2
Neratinib es un inhibidor irreversible y activo por vía
oral de la tirosina quinasa HER-2 que bloquea la transducción de
señales a través de un amplio espectro de 3
receptores, erbB-1, erbB-2 y erbB-4 (37). El primer ensayo abierto
multicéntrico de fase II con neratinib en monoterapia para pacientes
con cáncer de mama avanzado
incluyó pacientes que se dividieron en dos cohortes, la
cohorte con tratamiento previo con trastuzumab (n =
66) y la cohorte sin tratamiento previo con trastuzumab
(n = 70). Los resultados mostraron que las tasas de SLP
a las 16 semanas fueron del 59% para los pacientes con
tratamiento previo con trastuzumab y del 78% para los
pacientes sin tratamiento previo con trastuzumab. La
mediana de SLP fue de 22,3 y 39,6 semanas. La diarrea fue el evento
adverso mas frecuente, grados 3 a 4 ,
en el 30% de los pacientes con tratamiento previo con
trastuzumab y en el 13% de los pacientes sin tratamiento previo con
trastuzumab (38). El ensayo clínico aleatorizado NEfERT-T (39) mostró
que en las pacientes
con CMM HER2 positivas de primera línea, neratinibpaclitaxel no era
superior a trastuzumab-paclitaxel en
términos de SLP. Pero neratinib-paclitaxel puede retrasar la progresión
de la enfermedad a sistema nervioso
central. Estos resultados deben ser confirmados por ensayos
aleatorizados a gran escala.
Margetuximab es un anticuerpo anti-HER2 modificado
con Fc que se une con elevada afinidad a las formas de
menor y mayor afinidad de CD16A, importante para
la citotoxicidad mediada por células dependiente de
anticuerpos (ADCC) contra las células tumorales. Un
estudio de fase I en pacientes con CMM HER2 positivo
mostró que el margetuximab se tolera bien y tiene una
actividad prometedora como agente único. Se están realizando más
esfuerzos de desarrollo de agentes únicos o
en combinación con otros agentes terapéuticos (40)
MM-302 es un liposoma PEGilado dirigido a HER2
que encapsula la doxorrubicina para facilitar su administración a las
células tumorales que sobreexpresan
HER2. Está en marcha un ensayo aleatorizado de fase
2 (HERMIONE) de MM-302 más trastuzumab vs. quimioterapia a elección del
médico más trastuzumab en
pacientes con CMM HER2 positivo, sin antraciclinas
y previamente tratado (41,42)
Nuevas combinaciones (con
inhibidores de mTOR o inhibidores de
PI3K) en pacientes HER positivo
Las mutaciones en la vía PI3K son frecuentes en el
cáncer de mama y provocan resistencia a los agentes
dirigidos a HER 2. PI3K está aguas abajo de HER2 y
mTOR está aguas abajo de PI3K, por lo tanto esta vía
puede ser un paso importante para superar la resistencia a trastuzumab
en CMM HER2 positivo. En el estudio BOLERO-3 fueron asignados al azar
everolimus
o placebo en pacientes con CM avanzado resistente
a trastuzumab y demostró que la adición de everolimus a trastuzumab más
vinorelbine prolonga significativamente la SLP (7,0 frente a 5,78; p =
0,0067),
pero con mayor frecuencia de eventos adversos (43).
El ensayo de fase III BOLERO-1 compara paclitaxel y
trastuzumab con o sin everolimus para el tratamiento
de primera línea de mujeres con CMM HER2 positivo
(44). Aunque la SLP no fue significativamente diferente entre los
grupos de la población completa, se observó una prolongación de 7,2
meses con la adición de
everolimus en la población HER2 positiva y receptores
hormonales negativos.
Pilaralisib (SAR245408) es un inhibidor de PI3K panclase I. Se realizó
un estudio de fase I / II de pilaralisib en combinación con trastuzumab
o paclitaxel más
trastuzumab en pacientes con CMM HER2 positivo
que habían progresado con un régimen previo que contenía trastuzumab y
dio como resultado que pilaralisib
en combinación con trastuzumab con o sin paclitaxel
tuvo un nivel aceptable en el perfil de seguridad y con
actividad clínica en el grupo de paclitaxel (45).
Ca de mama receptor hormona
positivo
La terapia hormonal tiene el propósito de prevenir la
interacción entre los estrógenos y las vías dependientes
de estrógenos para estimular las células neoplásicas. Se
puede realizar a través de:
1. Bloqueo de la producción de
estrógenos:
- quirúrgico (ooforectomía);
- radiológico;
- químico (análogos de LH-RH);
- inhibidores de la aromatasa (conversión enzima de los precursores de
andrógenos en estrógenos).
2. Bloquear la acciónde los estrógenos
sobre células tumorales:
- SERM: actúan como agonistas de estrógenos, antagonistas o ambos,
según el objetivo tisular: tamoxifeno, toremifeno, raloxifeno;
- SERD - inhibición de la actividad de ER: fulvestrant, antagonista
de ER sin efectos agonistas de
estrógenos.
El análogo de LH-RH utilizado en la práctica actual es
goserelina 3,6 mg, intradérmico a los 28 días. Los inhibidores de la
aromatasa que se utilizan actualmente
son los inhibidores de la aromatasa no esteroideos de
3ª generación (reversibles): Anastrozol 1 mg / día p.o y
Letrozol 2,5 mg / día p.o o esteroideos (irreversibles):
Exemestan 25 mg / día p.o. Activo solo en pacientes
posmenopáusicas. No existe resistencia cruzada entre
los dos tipos de inhibidores de la aromatasa. El tamoxifeno es el SERM
más utilizado, activo en pre y posmenopausia en la dosis de 20 mg / día
p.o; la respuesta al
tamoxifeno varía según el porcentaje de ER y PR de
las células de cáncer de mama HR +. El beneficio de la
terapia con tamoxifeno continúa después de la finalización del
tratamiento (46) y es independiente y se suma
al beneficio de la quimioterapia. Actúa como antagonista de estrógenos
en células de cáncer de mama HR
positivo, agonista de estrógenos parcialmente en células
endometriales y agonista de estrógenos en células óseas.
Oxford Review (2005-5) en ensayos clínicos aleatorizados mostró que la
terapia adyuvante (46) ofrecía beneficio en sobrevida libre de
progresión para las pacientes
con tumores receptores hormonales positivos.
La terapia hormonal adyuvante está indicada en todas
las pacientes con neoplasia de mama HR positivo. No
se recomienda su administración concomitante a la quimioterapia, pero
puede administrarse durante la radioterapia. En la premenopausia
consiste en Tamoxifeno
+/- inhibición ovárica quirúrgica / química. Es equivalente a la
quimioterapia CMF y puede reemplazarla.
También está indicado para pacientes premenopáusicas
que no presentaron amenorrea después de la quimioterapia (47).
Disminuye el riesgo de recurrencia en un
6% y el riesgo de muerte por cáncer de mama en un
6,3%. A diferencia de la inhibición quirúrgica o radiológica, la
inhibición química ovárica no es definitiva, que
es una ventaja en pacientes jóvenes, cuya fertilidad se
conserva. Por ahora, no se ha demostrado un beneficio
claro de asociar el tratamiento con análogos de LH-RH
al tamoxifeno en enfermedad adyuvante, pero según el
consenso de Lisboa (2011), se recomienda utilizar la
asociación de análogos de LH-RH en los dos primeros
años de tratamiento en pacientes menores de 35 años
con neoplasia de mama HR positivo, que reciben tratamiento adyuvante
con Tamoxifeno (los dos primeros años representan el período con mayor
incidencia
de recidivas locales y/o distantes en la historia natural de un cáncer
de mama). En pacientes posmenopáusicas, la terapia hormonal adyuvante
es el tamoxifeno o
inhibidores de la aromatasa (8). La terapia adyuvante
con inhibidores de la aromatasa está indicada desde el
inicio en pacientes de “alto riesgo” (por ejemplo Her2
positivo, invasión importante de ganglios linfáticos) o
en pacientes con contraindicación para Tamoxifeno por
comorbilidad. Hay estudios que demostraron el beneficio de la terapia
adyuvante en la posmenopausia con
Tamoxifeno 2-3 años, seguido de Exemestan 3-2 años
(48). Además, teniendo en cuenta la larga historia natural del cáncer
de mama HR positivo, donde las recidivas suelen aparecer entre los años
6-15, existen estudios
clínicos que demostraron el beneficio del tratamiento
adyuvante con un inhibidor de la aromatasa durante 5
años, después de 5 años. período de un año de tratamiento adyuvante con
tamoxifeno (49)
Casi la mitad de las pacientes con neoplasia de mama
HR positivo tienen resistencia de novo o adquirida a la
terapia hormonal, siendo uno de los mecanismos de resistencia a la
terapia hormonal la activación de la vía
celular mTor. La quinasa beta-1 S6, el sustrato del complejo mTor,
fosforila el dominio activador independiente del ligando de ER. El
inhibidor de mTor Everolimus
bloquea la reacción y puede revertir la resistencia a la
terapia hormonal. El ensayo clínico Bolero 2 demostró
que la asociación de Everolimus 10 mg / día VO con
Exemestane 25 mg / día VO en pacientes con HR positivo, su cáncer de
mama 2- metastásico en progresión
bajo un inhibidor de aromatasa no esteroideo duplica
SLP comparado con Exemestane solo (50).
Las quinasas dependientes de ciclina 4 y 6, que regulan el crecimiento
y la división celular, son inhibidas
por Palbociclib. Los estudios clínicos demostraron que
las pacientes sin tratamiento hormonal con cáncer de
mama HR positivo, Her2- avanzado que recibieron
125 mg / día de palbociclib y 2,5 mg / día de letrozol
por vía oral tuvieron una SLP de 24,8 meses en comparación con 14,5
meses para las pacientes que recibieron solo letrozol. (Paloma 2), (51)
y pacientes con
HR positivo, Her2 - neoplasia de mama metastásica en
progresión en terapia hormonal el ribociclib ha demostrado mejoría en
la sobrevida global (52).
Conclusión
En conclusión, me gustaría citar al profesor Gabriel
Hortobagyi del MD Anderson Cancer Center: “El
cáncer de mama es un conglomerado de síndromes
múltiples definidos molecularmente, que son diferentes en cuanto a su
historia natural, evolución clínica y
sensibilidad a agentes terapéuticos externos”.
Referencias
1. Bray F, Ferlay J, Soerjomataram I,
Siegel R, Torre L, Jemal A. Global cancer statistics 2018: GLOBOCAN
estimates of incidence and mortality worldwide for 36 cancers in
185 countries. CA A Cancer J Clin.2018;68(6):394-424.
2. Ginsburg O, Bray F, Coleman M,
Vanderpuye V, Eniu
A, Kotha S et al. The global burden of women’s cancers: a grand
challenge in global health. Lancet.
2017;389(10071):847-860.
3. DANE [Internet]. Dane.gov.co. 2020
[consultado 18 Octubre 2020].Disponible en:
http://www.dane.gov.co/files/investigaciones/poblacion/defunciones/defun-2005/CUADRO5.xls
4. Murillo R, Piñeros M, Hernández G.
Atlas de mortalidad
por cáncer en Colombia. Bogotá. Instituto Nacional de
Cancerología, Instituto Geográfico Agustín Codazzi; Bogotá: INC, 2004.
5. Piñeros M, Hernández G, Bray F.
Increasing mortality rates of common malignancies in Colombia: an
emerging
problem. Cancer. 2004;101(10):2285-92.
6. Hernández G, Herrán S, Cantor LF.
Análisis de las
tendencias de mortalidad por cáncer de mama en Colombia y Bogotá, 1981
a 2000. Rev Colomb Cancerol.
2007;11(1):32-9.
7. Observatorio Nacional de Cáncer
[Internet]. Minsalud.
gov.co. 2020 [consultado 18 Octubre 2020]. Disponible
en:
https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/ED/GCFI/guia-ross-cancer.pdf
8. Perou C, Sørlie T, Eisen M, van de
Rijn M, Jeffrey S, Rees
C et al. Molecular portraits of human breast tumours. Nature.
2000;406(6797):747-752.
9. Curtis C, Shah S, Chin S,
Turashvili G, Rueda O, Dunning
M et al. The genomic and transcriptomic architecture of
2,000 breast tumours reveals novel subgroups. Nature.
2012;486(7403):346-352.
10. Lehmann B, Jovanović B, Chen X,
Estrada M, Johnson K,
Shyr Y et al. Refinement of Triple-Negative Breast Cancer
Molecular Subtypes: Implications for Neoadjuvant Chemotherapy
Selection. PLOS ONE. 2016;11(6):e0157368.
11. Crónica de la Medicina. Tomo I.
2º Edición. Edit. Plaza y
Janés. Barcelona, 1995.
12. Halsted WS. The results of
operation for the cure of cancer of the breast performed at John
Hopkins Hospital from
June 1889 to January 1894. Ann Surg. 1894;20(5):497-
555.
13. McGuire K, Santillan A, Kaur P,
Meade T, Parbhoo J,
Mathias M et al. Are Mastectomies on the Rise? A 13-
Year Trend Analysis of the Selection of Mastectomy Vs.
Breast Conservation Therapy in 5865 Patients. Ann Surg
Oncol. 2009;16(10):2682-2690.
14. Fisher B, Jeong J, Anderson S,
Bryant J, Fisher E, Wolmark N. Twenty-Five-Year Follow-up of a
Randomized
Trial Comparing Radical Mastectomy, Total Mastectomy,
and Total Mastectomy Followed by Irradiation. N Engl J
Med. 2002;347(8):567-575.
15. Fisher B, Anderson S, Bryant J,
Margolese R, Deutsch
M, Fisher E et al. Twenty-Year Follow-up of a Randomized Trial
Comparing Total Mastectomy, Lumpectomy, and
Lumpectomy plus Irradiation for the Treatment of Invasive
Breast Cancer. N Engl J Med. 2002;347(16):1233-1241.
16. Diao K, Chen Y, Catalano P, Lee
S, Milani N, Killoran J et al.
Radiation toxicity in patients with collagen vascular disease
and intrathoracic malignancy treated with modern radiation
techniques. Radiother Oncol. 2017;125(2):301-309.
17. Gill G. Sentinel-Lymph-Node-Based
Management or
Routine Axillary Clearance? One-Year Outcomes of
Sentinel Node Biopsy Vs. Axillary Clearance (SNAC): A
Randomized Controlled Surgical Trial. Ann Surg Oncol.
2008;16(2):266-275.
18. Langer I, Guller U, Hsu-Schmitz
S, Ladewig A, Viehl C,
Moch H et al. Sentinel lymph node biopsy is associated
with improved survival compared to level I & II axillary
lymph node dissection in node negative breast cancer
patients. Eur J Surg Oncol. 2009;35(8):805-813.
19. Cancer Staging Manual. 8va ed.
2020.
20. Dai, X., Li, T., Bai, Z., Yang,
Y., Liu, X., Zhan, J., & Shi,
B.Breast cancer intrinsic subtype classification, clinical
use and future trends. Am J CancerRes. 2015;5(10):2929–
2943.
21. Slamon D, Clark G, Wong S, Levin
W, Ullrich A, McGuire W. Human breast cancer: correlation of relapse
and
survival with amplification of the HER-2/neu oncogene.
Science. 1987;235(4785):177-182.
22. Baselga J, Albanell J. Mechanism
of action of anti-HER2
monoclonal antibodies. Ann Oncol. 2001;12:S35-S41.
23. Slamon D, Leyland-Jones B, Shak
S, Fuchs H, Paton
V, Bajamonde A et al. Use of Chemotherapy plus a Monoclonal Antibody
against HER2 for Metastatic Breast
Cancer That Overexpresses HER2. N Engl J Med.
2001;344(11):783-792.
24. Robert N, Leyland-Jones B, Asmar
L, Belt R, Ilegbodu
D, Loesch D et al. Randomized Phase III Study of Trastuzumab,
Paclitaxel, and Carboplatin Compared With
Trastuzumab and Paclitaxel in Women With HER-2–
Overexpressing Metastatic Breast Cancer. J Clin Oncol.
2006;24(18):2786-2792.
25. Valero V, Forbes J, Pegram M,
Pienkowski T, Eiermann
W, von Minckwitz G et al. Multicenter Phase III Randomized Trial
Comparing Docetaxel and Trastuzumab
With Docetaxel, Carboplatin, and Trastuzumab As FirstLine Chemotherapy
for Patients With HER2-Gene-Amplified Metastatic Breast Cancer (BCIRG
007 Study):
Two Highly Active Therapeutic Regimens. J Clin Oncol.
2011;29(2):149-156.
26. Andersson M, Lidbrink E, Bjerre
K, Wist E, Enevoldsen
K, Jensen A et al. Phase III Randomized Study Comparing Docetaxel Plus
Trastuzumab With Vinorelbine Plus
Trastuzumab As First-Line Therapy of Metastatic or Locally Advanced
Human Epidermal Growth Factor Receptor
2–Positive Breast Cancer: The HERNATA Study. J Clin
Oncol. 2011;29(3):264-271.
27. Burstein H, Keshaviah A, Baron A,
Hart R, Lambert-Falls
R, Marcom P et al. Trastuzumab plus vinorelbine or taxane chemotherapy
for HER2-overexpressing metastatic
breast cancer: The trastuzumab and vinorelbine or taxane
study. Cancer. 2007;110(5):965-972.
28. Cortés J, Fumoleau P, Bianchi G,
Petrella T, Gelmon K,
Pivot X et al. Pertuzumab Monotherapy After TrastuzumabBased Treatment
and Subsequent Reintroduction of Trastuzumab: Activity and Tolerability
in Patients With Advanced Human Epidermal Growth Factor Receptor
2–Positive
Breast Cancer. J Clin Oncol. 2012;30(14):1594-1600.
29. Baselga J, Cortes J, Kim SB, et
al. Pertuzumab plus trastuzumab plus docetaxel for metastatic breast
cancer. N
Engl J Med 2012;366:109-19
30. Swain S, Baselga J, Kim S, Ro J,
Semiglazov V, Campone M et al. Pertuzumab, Trastuzumab, and Docetaxel
in
HER2-Positive Metastatic Breast Cancer. N Engl J Med.
2015;372(8):724-734.
31. Perez E, Barrios C, Eiermann W,
Toi M, Im Y, Conte P
et al. Trastuzumab Emtansine With or Without Pertuzumab Vs. Trastuzumab
Plus Taxane for Human Epidermal
Growth Factor Receptor 2–Positive, Advanced Breast
Cancer: Primary Results From the Phase III MARIANNE
Study. J Clin Oncol. 2017;35(2):141-148.
32. von Minckwitz G, du Bois A,
Schmidt M, Maass N, Cufer
T, de Jongh F et al. Trastuzumab Beyond Progression in
Human Epidermal Growth Factor Receptor 2–Positive
Advanced Breast Cancer: A German Breast Group 26/
Breast International Group 03-05 Study. J Clin Oncol.
2009;27(12):1999-2006.
33. Gelmon K, Boyle F, Kaufman B,
Huntsman D, Manikhas
A, Di Leo A et al. Open-label phase III randomized controlled trial
comparing taxane-based chemotherapy (Tax)
with lapatinib (L) or trastuzumab (T) as first-line therapy
for women with HER2+ metastatic breast cancer: Interim
analysis (IA) of NCIC CTG MA.31/GSK EGF 108919. J
Clin Oncol. 2012;30(15_suppl):LBA671-LBA671.
34. Geyer CE, Forster J, Lindquist D,
et al. Lapatinib plus capecitabine for HER2-positive advanced breast
cancer. N
Engl J Med 2006;355:2733-43.
35. Verma S, Miles D, Gianni L, Krop
I, Welslau M, Baselga J
et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer.
N Engl J Med. 2012;367(19):1783-
1791.
36. Krop I, Kim S, Martin A, LoRusso
P, Ferrero J, BadovinacCrnjevic T et al. Trastuzumab emtansine vs.
treatment
of physician's choice in patients with previously treated
HER2-positive metastatic breast cancer (TH3RESA): final overall
survival results from a randomised open-label
phase 3 trial. Lancet Oncol. 2017;18(6):743-754.
37. Rabindran S, Discafani C,
Rosfjord E, Baxter M, Floyd M,
Golas J et al. Antitumor Activity of HKI-272, an Orally Active,
Irreversible Inhibitor of the HER-2 Tyrosine Kinase.
Cancer Res. 2004;64(11):3958-3965.
38. Burstein H, Sun Y, Dirix L, Jiang
Z, Paridaens R, Tan A et
al. Neratinib, an Irreversible ErbB Receptor Tyrosine Kinase Inhibitor,
in Patients With Advanced ErbB2-Positive
Breast Cancer. J Clin Oncol. 2010;28(8):1301-1307.
39. Awada A, Colomer R, Inoue K,
Bondarenko I, Badwe
R, Demetriou G et al. Neratinib Plus Paclitaxel vs Trastuzumab Plus
Paclitaxel in Previously Untreated Metastatic ERBB2-Positive Breast
Cancer. JAMA Oncology.
2016;2(12):1557.
40. Bang Y, Giaccone G, Im S, Oh D,
Bauer T, Nordstrom
J et al. First-in-human phase 1 study of margetuximab
(MGAH22), an Fc-modified chimeric monoclonal antibody, in patients with
HER2-positive advanced solid tumors.
Ann Oncol. 2017;28(4):855-861.
41. Munster P, Krop I, LoRusso P, Ma
C, Siegel B, Shields
A et al. Safety and pharmacokinetics of MM-302, a
HER2-targeted antibody–liposomal doxorubicin conjugate, in patients
with advanced HER2-positive breast
cancer: a phase 1 dose-escalation study. Br J Cancer.
2018;119(9):1086-1093.
42. Miller K, Cortes J, Hurvitz SA,
et al. HERMIONE: a randomized Phase 2 trial of MM-302 plus trastuzumab
vs.
chemotherapy of physician's choice plus trastuzumab
in patients with previously treated, anthracycline-naive,
HER2-positive, locally advanced/metastatic breast cancer. BMC Cancer
2016;16:352
43. André F, O'Regan R, Ozguroglu M,
Toi M, Xu B, Jerusalem G et al. Everolimus for women with
trastuzumabresistant, HER2-positive, advanced breast cancer (BOLERO-3):
a randomised, double-blind, placebo-controlled
phase 3 trial. Lancet Oncol. 2014;15(6):580-591.
44. Hurvitz S, Andre F, Jiang Z, Shao
Z, Mano M, Neciosup
S et al. Combination of everolimus with trastuzumab plus
paclitaxel as first-line treatment for patients with HER2-
positive advanced breast cancer (BOLERO-1): a phase 3,
randomised, double-blind, multicentre trial. Lancet Oncol.
2015;16(7):816-829.
45. Tolaney S, Burris H, Gartner E,
Mayer I, Saura C, Maurer M
et al. Phase I/II study of pilaralisib (SAR245408) in combination with
trastuzumab or trastuzumab plus paclitaxel in
trastuzumab-refractory HER2-positive metastatic breast
cancer. Breast Cancer Res Treat. 2014;149(1):151-161.
46. Adjuvant chemotherapy in
oestrogen-receptor-poor
breast cancer: patient-level meta-analysis of randomised
trials. The Lancet. 2008;371(9606):29-40.
47. Bernhard J, Zahrieh D,
Castiglione-Gertsch M, Hürny
C, Gelber R, Forbes J et al. Adjuvant Chemotherapy
Followed By Goserelin Compared With Either Modality Alone: The Impact
on Amenorrhea, Hot Flashes, and
Quality of Life in Premenopausal Patients—The International Breast
Cancer Study Group Trial VIII. J Clin Oncol.
2007;25(3):263-270.
48. Rose C, Vtoraya O, Pluzanska A,
Davidson N, Gershanovich M, Thomas R et al. An open randomised trial of
second-line endocrine therapy in advanced breast cancer. Eur J Cancer.
2003;39(16):2318-2327.
49. Coombes R, Hall E, Gibson L,
Paridaens R, Jassem J,
Delozier T et al. A Randomized Trial of Exemestane after Two to Three
Years of Tamoxifen Therapy in Postmenopausal Women with Primary Breast
Cancer. N Engl J
Med. 2004;350(11):1081-1092.
50. Baselga J, Campone M, Piccart M,
Burris H, Rugo H,
Sahmoud T et al. Everolimus in Postmenopausal Hormone-Receptor–Positive
Advanced Breast Cancer. N Engl J
Med. 2012;366(6):520-529.
51. Finn R, Martin M, Rugo H, Jones
S, Im S, Gelmon K et al.
Palbociclib and Letrozole in Advanced Breast Cancer. N
Engl J Med. 2016;375(20):1925-1936.
52. Im S, Lu Y, Bardia A, Harbeck N,
Colleoni M, Franke F et
al. Overall Survival with Ribociclib plus Endocrine Therapy in Breast
Cancer. NEngl J Med. 2019;381(4):307-316.
Recibido:
Noviembre 02, 2020
Aprobado: Diciembre 03, 2020
Correspondencia:
Hernán Carranza
carranza.hernan@gmail.com



