Resumen
La secuenciación de nueva generación es una nueva herramienta de
secuenciación masiva de ADN y
ARN que ha cambiado radicalmente el diagnóstico molecular del cáncer.
Esta tecnología implementada de manera correcta permite seleccionar
nuevos tratamientos dirigidos contra el cáncer con base en
la detección de biomarcadores moleculares predictivos. En este artículo
revisaremos las aplicaciones
de la secuenciación de nueva generación para el diagnóstico molecular
del cáncer, el monitoreo de respuesta o resistencia, así como los
nuevos fármacos que se encuentran disponibles o en desarrollo para
alteraciones moleculares específicas, en pro de la promoción de la
oncología de precisión.
Palabras clave: NGS; oncología; medicina de precisión.
NEXT GENERATION SEQUENCING (NGS)
AND PRECISION ONCOLOGY
Abstract
Next-generation sequencing is a new massive DNA and RNA sequencing
tool that has radically changed cancer’s molecular diagnosis. This
correctly implemented technology makes it
possible to select new targeted treatments against cancer-based
detection of predictive molecular biomarkers. This article will review
the applications of next-generation sequencing for
the molecular diagnosis of cancer, the monitoring of response or
resistance, and the available
new drugs or in development for specifi c molecular alterations to
promote precision oncology.
Keywords: NGS;
oncology; precisión medicine.


¹ MD PhD. Centro de Educación Médica e Investigaciones
Clínicas (CEMIC), Buenos Aires, Argentina.
Introducción
Por más de una década la secuenciación de nueva
generación o NGS ha revolucionado el diagnóstico
molecular del cáncer, abriendo nuevas oportunidades
para el desarrollo de tratamientos innovadores y, como
herramienta de estudio, ha permitido una mayor comprensión de la gran
mayoría de los tipos de cáncer con
proyectos como The Cancer Genome Atlas (TCGA)
(1). También la integralidad de los datos de NGS en
plataformas de uso público como cBioportal y otras
plataformas para clasificación de variantes y su accionabilidad como
OncoKB, ClinVar y COSMIC ha facilitado el acceso a información ya
curada y ordenada
para la interpretación de datos (2). NGS comprende
diferentes tecnologías y técnicas entre las que se incluyen la
secuenciación de pequeños fragmentos en
paneles génicos, la secuenciación de ARN del exoma
o genoma. En este artículo nos referiremos a tecnologías de
secuenciación de fragmentos cortos, tanto por
métodos de secuenciación por síntesis como por ligación (3). En este
proceso revisaremos las aplicaciones
que tiene NGS en la oncología de precisión para el
diagnóstico, monitoreo de sensibilidad y resistencia,
así como las alteraciones moleculares más relevantes
detectadas por NGS y las terapias dirigidas desarrolladas.
Aplicaciones de NGS en la oncología
de precisión
La secuenciación de nueva generación ha impulsado
el desarrollo de nuevos tratamientos con base en biomarcadores para
múltiples tipos de tumores pediátricos y adultos. Con el tiempo NGS se
ha convertido en
una herramienta de menor costo y mayor accesibilidad
para los pacientes, gracias al desarrollo de plataformas
centralizadas de testeos moleculares y al impulso de
plataformas de secuenciación que se pueden realizar
en el sitio de atención de los pacientes como hospitales
académicos (3). Utilizando bajas cantidades de ADN
y ARN las diferentes plataformas de NGS permiten
estudiar en simultáneo múltiples alteraciones moleculares que son
potenciales blancos terapéuticos (4).
Esto ha sido de especial relevancia en el tratamiento
del cáncer de pulmón no escamoso, en el que el desarrollo de la
medicina de precisión ha evolucionado
desde el entendimiento de las mutaciones activatrices
de EGFR en el 2004 hasta la actualidad en la cual se
encuentran en desarrollo fármacos para alrededor de
una decena de alteraciones moleculares (5,6). Adicionalmente, la
secuenciación de nueva generación ha
facilitado el desarrollo de tratamientos basados en alteraciones
moleculares en colangiocarcinoma, cáncer
de vejiga, cáncer de próstata, cáncer de ovario, mama,
y biomarcadores llamados “tumor agnostic” o agnósticos que pueden estar
presentes en diferentes tumores
y son predictivos de respuesta a un tipo de fármacos.
La utilidad de la NGS tanto en tejido como en plasma
es versátil, y con el solo fin de resumir algunas de sus
aplicaciones hemos clasificado las instancias donde se
presenta la oportunidad para estudios moleculares en
cáncer en el diagnóstico, monitoreo de eficacia o progresión a
tratamientos y detección de alteraciones que
conllevan a resistencia a terapias dirigidas.
El estudio molecular en la práctica diaria es un hito
fundamental para orientar el diagnóstico en algunos
tumores como los del sistema nervioso central y sarcomas. Sin embargo,
presenta una gran importancia
como biomarcador para guiar el tratamiento de varios
tumores. Muchos de los biomarcadores que se conocen han sido
descubiertos utilizando técnicas de biología molecular de menor
complejidad como pueden
ser las mutaciones de
EGFR, BRAF y
KIT. Hasta hace
relativamente poco tiempo, el diagnóstico de mutaciones activadoras de
EGFR en cáncer de pulmón se
hacían mediante
PCR y
secuenciación Sanger,
lo mismo
que las mutaciones de
BRAF V600X
en melanoma.
Si bien ha sido considerado el
gold
standard, la sensibilidad de este
método es baja, requiriendo que estas alteraciones estuvieran presentes
en el 20% de las células tumorales en la muestra, siendo de crucial
importancia la selección de la muestra (7). Métodos más
sensibles se desarrollaron luego como kits de PCR en
tiempo real para detección de mutaciones puntuales
e inserciones y deleciones (indels) con una sensibilidad del 5% (8).
Otras alteraciones moleculares como
fusiones de genes como ALK, ROS1, RET o NTRK
pueden ser detectadas por otros métodos como la combinación de
inmunohistoquímica (IHQ) e hibridación
fluorescente
in situ (FISH)
dependiendo del caso (9).
Las alteraciones moleculares que conllevan a splicing
alternativo patogénico del exón 14 del oncogén MET
son más complejas de detectar por secuenciación sanger, y métodos como
PCR de tiempo real (qPCR) son
opciones no validadas para la identificación de pacientes que podrían
beneficiarse de inhibidores selectivos
de MET (10,11). Adicionalmente, con el desarrollo de
inhibidores selectivos de KRAS G12C, e inhibidores
potentes de EGFR/HER2 en el contexto de inserciones en el exón 20, el
espectro de blancos moleculares
accionables se amplía a casi el 40% de los tumores
no escamosos de pulmón. La aplicación de NGS en
el diagnóstico de cáncer de pulmón permite interrogar todos estos
biomarcadores y otros con potenciales
implicancias en un solo estudio y utilizando pequeñas
cantidades de ADN. Dado que todos estos biomarcadores son necesarios en
el diagnóstico molecular de
pacientes con cáncer de pulmón, realizar estas determinaciones por
separado consume tiempo, tejido y es
más costoso. Un estudio realizado en Estados Unidos
ha revelado que el uso de NGS permite ahorrar tiempo
y costos en los centros centros que trabajan con Medicare o Medicaid y
pagadores privados en ese país (12).
El beneficio de utilizar NGS y su impacto en la oncología de precisión
no se traslada necesariamente a
todos los tipos tumorales ni pacientes cuando se utiliza
de manera global. Varios estudios han demostrado que
un pequeño subgrupo de pacientes se benefician de la
secuenciación masiva sin selección clínica. En el estudio MOSCATO-01
del Instituto Gustave Roussy se incluyeron pacientes con cáncer
avanzado que hubieran
experimentado progresión de enfermedad al menos a
una línea de tratamiento con biopsia suficiente para
realizar NGS con panel multigénico, secuenciación de
ARN (RNAseq) e hibridación genómica comparativa
(aCGH) (13).
De manera similar, el estudio WINTHER exploró la
utilización de NGS basado en ADN y ARN para la selección de tratamiento
en pacientes con cáncer avanzado (14). Se incluyeron 303 pacientes de
los cuales 107
(35%) fueron evaluables para tratamiento. De los 107
pacientes, 69 (22% del total consentido) recibieron un
tratamiento basado en resultados de NGS con ADN,
y 38 pacientes (12,5%) recibieron tratamiento basado
en selección por NGS en ARN. Este estudio incluyo
principalmente pacientes con tumores gastrointestinales, tumores de
cabeza y cuello y cáncer de pulmón.
La tasa de pacientes con enfermedad estable mayor a 6
meses fue del 26,2%, y 11,2% de los pacientes tratados
experimentaron una respuesta parcial o completa. La
mediana de sobrevida en los 107 pacientes fue de 5,9
meses (14).
Asimismo, el estudio multicéntrico I-PREDICT también evaluó la
selección de tratamientos dirigidos basados en el perfil molecular de
tumores de pacientes
con diferentes tipos de cáncer, principalmente tumores
gastrointestinales, ginecológicos y mamarios (15). En
este estudio se realizó NGS a partir de tejido, plasma
y expresión tisular de PD-L1. De un total de 149 pacientes incluidos,
con enfermedad avanzada y progresión a tratamiento estándar, 83
recibieron tratamiento
y fueron incluidos en el análisis. De ellos, 73 pacientes
recibieron una terapia personalizada de acuerdo con
el perfil molecular del tumor, representando el 49% de
los pacientes enrolados en el estudio. Los tratamientos
que fueron administrados incluyeron inmunoterapia,
terapia dirigida contra la vía ERBB, la vía de las “mitogen-activated
protein” (MAP) quinasas, vía de PI3K y otros (15). En el estudio
I-PREDICT, el 30% de los
pacientes presentó control de enfermedad mayor o
igual a 6 meses. En aquellos pacientes cuyos tumores
tienen mayor cantidad de alteraciones tratables la tasa
de control de enfermedad fue, como era esperado, superior.
Estos estudios demuestran que hay un subgrupo de
pacientes que presentan un beneficio con tratamientos
dirigidos cuando se utiliza una estrategia basada en
el perfilado molecular extensivo de diferentes tipo de
cáncer. Para estos pacientes, esto representa una oportunidad única de
tratamiento, sin embargo, a nivel poblacional, la utilización de
secuenciación de próxima
generación en forma masiva impresiona tener un bajo
impacto en beneficio en términos de supervivencia.
Si se orienta la utilización de secuenciación de próxima generación de
acuerdo al tipo de patología y acceso a nuevas terapias, el impacto
puede ser mayor.
Si se tiene en cuenta que, en pacientes con cáncer de
pulmón de células no pequeñas de histología no escamosa, la prevalencia
de alteraciones moleculares con
blancos terapéuticos aprobados o en vías de desarrollo
alcanza el 40% de la población (16). Si bien la prevalencia de
alteraciones moleculares varían de acuerdo
a la población y el sitio geográfico, en occidente las
mutaciones de
EGFR ocurren
en alrededor del 14%
de los pacientes, las mutaciones de BRAF en el 1-2%,
rearreglos de
ALK en 3-7%,
ROS1 y RET en alrededor
del 2%, “skipping” del exón 14 de
MET
en el 4%, mutaciones de KRAS G12C en 9-11%, inserciones en el
exón 20 de HER2 en el 2% y fusiones de
NTRK en el
0.2% (16–18). Para todas estas alteraciones moleculares hay drogas
aprobadas o en vías de aprobación con
actividad clínica demostrada en estudios de fase I/II, y
la identificación de los mismos es necesaria para poder
ofrecer terapias.
Hay otros tipos tumorales en los que la prevalencia
de alteraciones moleculares es significativa y ameritan su estudio. En
cáncer de vejiga, las mutaciones de
FGFR3 y fusiones de FGFR2 o FGFR3 ocurren en
aproximadamente el 20% de los carcinomas uroteliales invasores, siendo
reportado en 15% mutaciones de
FGFR3 y en 6% fusiones, siendo las más frecuentes la
fusión de FGFR3-TACC3 (19). En colangiocarcinomas
intrahepáticos, las fusiones de FGFR2 han sido reportadas en el 7% -
9%, las fusiones de ROS1 en el 8% y
mutaciones de BRAF V500E en el 5%. Existen drogas
con clara actividad clínica para pacientes cuyos tumores presentan
estas alteraciones (20). En cáncer de ovario las alteraciones en genes
de la reparación homóloga como BRCA1 y BRCA2 ocurren de forma germinal
en el 13-15% de las pacientes y en forma somática en
el 7%, llevando a una alta proporción de pacientes
que pueden recibir tratamientos con inhibidores de
PARP (21). En cáncer de tiroides anaplásico la prevalencia de
mutaciones de BRAF alcanza el 40% (22).
En tumores papilares de tiroides también se reportan
fusiones de RET (3%), NTRK (5%) y ALK (1%). En
carcinoma endometriales, alrededor del 20-30% de los
tumores presentan déficit de la reparación del ADN
por la vía “missmatch repair” y en un 10% adicional
presentan mutaciones en el gen de la polimerasa épsilon (POLE) que
afecta la capacidad de corrección en
la síntesis del ADN o función de “proofreading” (23).
En ambos contextos, estos tumores presentan fenotipos “hipermutados”
que los vuelven susceptibles a la
muerte celular mediado por el sistema inmune cuando
es estimulado con inhibidores de punto de control contra el eje
PD-L1/PD-1. En estos tumores y otros, en
los que la prevalencia de alteraciones moleculares con
potenciales implicancias terapéuticas es alta, el uso de
la secuenciación de próxima generación se vuelve necesaria.
Adicionalmente a blancos moleculares específicos
para cada tipo tumoral, existen otras alteraciones moleculares –que de
estar presentes en cualquier tipo tumoral– son considerados blancos
terapéuticos “agnósticos” o tejido inespecífico. Las fusiones de NTRK,
la inestabilidad microsatelital por déficit de “missmatch
repair” y, más recientemente y controversialmente, la
alta tasa mutacional o “tumor mutational burden” han
emergido como biomarcadores universales, independiente del tipo
tumoral.
La importancia de la aplicación de NGS en el diagnóstico molecular
radica en el rol predictivo de alteraciones
moleculares específicas para el tratamiento con terapias
dirigidas. También, los resultados obtenidos de estudios
de NGS pueden dar información pronostica acerca de
la biología tumoral y, en algunos casos, proveer información predictiva
negativa para ciertos tratamientos, es
decir que posiblemente el paciente no responda a una
terapia determinada de acuerdo con el perfil molecular.
Otra de las aplicaciones que potencialmente tendrá
NGS es en el monitoreo de la carga de enfermedad
mediante la secuenciación de ADN tumoral circulante en plasma. Esta no
es una práctica estándar en la
oncología al momento, sin embargo, la misma permite
identificar mediante el monitoreo de las frecuencias
alélicas de mutaciones somáticas tumorales el nivel de
volumen de enfermedad, predecir respuesta o beneficio al tratamiento y
recaídas previo a la evaluación mediante imágenes como la tomografía
computarizada
(24). Este modelo ha sido imitado a lo ya establecido
en el seguimiento de leucemias y otras enfermedades
hematológicas y ha sido demostrado en patologías
como cáncer de colon, cáncer de pulmón, cáncer de
mama entre otros (25–27).
La tercer aplicación que tiene una visión más asociada
a la investigación y el desarrollo de fármacos es el estudio de
mecanismos de resistencia utilizando NGS. De
esta manera se han identificado múltiples alteraciones
genómicas en genes que codifican proteínas que son
blancos terapéuticos, impidiendo la unión del fármaco,
o eluden la inhibición de señales intracelular, o generan
resistencia a las inmunoterapias disponibles (28). Existen en modo
general tres grupos de mecanismos principales de resistencia a
inhibidores de quinasas como
blancos terapéuticos: la adquisición de mutaciones que
impiden la unión del fármaco al blanco, o la amplificación del blanco,
para lo cual la cantidad de droga es
insuficiente para su inhibición; la activación de una vía
de señalización intracelular paralela por mutaciones,
amplificaciones o sobre expresión o sobre activación; y
un tercer mecanismo menos conocido que implica modificaciones
epigenéticas, alteraciones de la apoptosis o
transformaciones histológicas (28).
El estudio sistemático de los mecanismos de resistencia mediante NGS es
un desafío. En el estudio
MATCH-R en curso en el Instituto Gustave Roussy de
Francia, se busca identificar mecanismos de resistencia a una
diversidad amplia de fármacos, incluyendo
inhibidores de quinasas, inmunoterapia, inhibidores
de ciclinas y hormonoterapia (29). En pacientes que
experimentaron una respuesta parcial o estabilidad de
enfermedad mayor o igual a 6 meses, al momento de la
progresión se toma una muestra tumoral y muestras de
plasma. La muestra de tumor es analizada mediante
secuenciación con paneles a partir de ADN, secuenciación completa de
ARN, secuenciación de exoma
completo y también se deriva una porción de la biopsia
para el desarrollo de modelos murinos. De un total de
333 pacientes incluidos, 303 tenían material suficiente
para la realización de al menos un estudio molecular
(90%). De estas muestras, se realizó NGS en el 92% de
los casos, 72% secuenciación exomica completa y 71%
secuenciación de ARN. De 127 pacientes tratados con
una terapia blanco, a la resistencia se detectó una alteración
molecular con potencial implicancias terapéuticas en 57 pacientes (45%)
(29).
Más allá de este estudio que lo realiza en forma sistemática a través
de distintos tipos tumorales, se ha generado una gran cantidad de
evidencia acerca de los
mecanismos genómicos de resistencia usando NGS
que permitieron y aun permiten el desarrollo de nuevas drogas.
Alteraciones moleculares con
implicancias terapéuticas detectables
con NGS
Existen múltiples alteraciones moleculares que son
biomarcadores de eficacia en los tratamientos actualmente aprobados o
en desarrollo. Las guías de la Sociedad Europea de Oncología Clínica
(ESMO) sobre
el uso de NGS recomiendan hacer este tipo de estudio
en cáncer de pulmón no escamoso, cáncer de colon si
no es posible por PCR, en colangiocarcinomas, cáncer de ovario y
búsqueda de TMB para un subtipo de
tumores (cuello uterino, glándulas salivares, tiroides,
tumores y cáncer de vulva) (30). Para todas estas enfermedades el panel
de NGS debe incluir genes en la
categoría I de “ESMO Scale for Clinical Actionability
of molecular Targets” (ESCAT) (31). Las alteraciones
categorizadas como “tier I” son blancos terapéuticos
disponibles para diagnóstico de rutina con drogas disponibles y
recomendadas para ser utilizadas con base
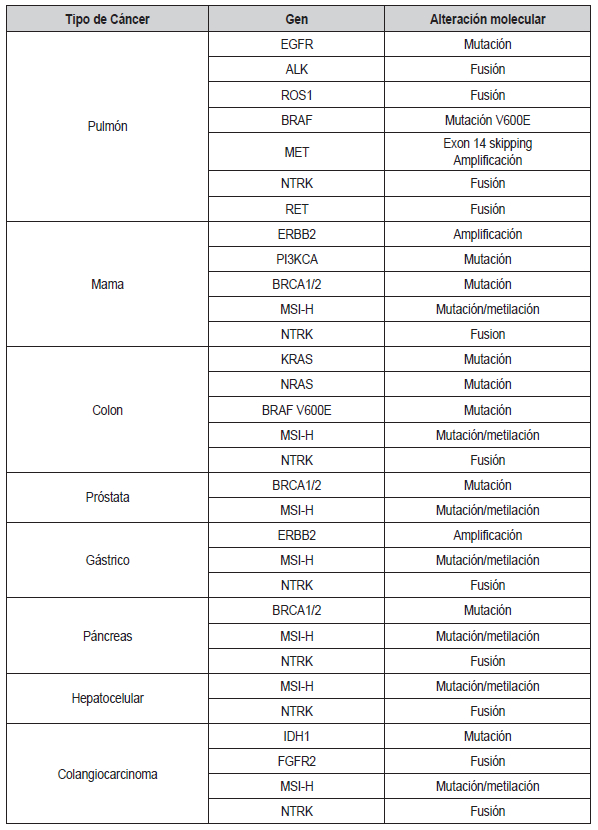
en ese biomarcador. Un resumen de todas las alteraciones moleculares
clasificadas como Tier I se presentan en la
Tabla 1. A continuación se detallan
algunas
características biológicas y tratamientos para las alteraciones
moleculares más frecuentemente diagnosticadas con tecnología de NGS.
EGFR
El receptor del factor de crecimiento epidérmico
(EGFR) es codificado por el gen
ERBB1
y es un receptor de tirosina quinasa de la familia de receptores de
factores epidérmicos como HER2, HER3 y HER4. En
condiciones fisiológicas, este receptor es activado mediante la unión
de su ligando, el factor de crecimiento
epidérmico (EGF), estimulando la homo- (EGFREGFR) o heterodimerización
del receptor con otro
receptor (ej: EGFR-HER3), resultando en la fosforilación de su dominio
tirosina quinasa y la señalización
intracelular mediante adaptadores que conllevan a la
activación de múltiples vías como la de MAPK, PI3KCA/AKT/mTOR, JAK/STAT
entre otras (32). El
receptor de EGFR se encuentra involucrado en múltiples tipos de cáncer,
desde glioblastomas hasta carcinomas colorectales en varias
alteraciones que incluyen
la sobre-expresión, la amplificación y las más comúnmente conocida en
cáncer de pulmón, la mutación del
dominio tirosina quinasa del receptor. Las mutaciones
del dominio tirosina quinasa de EGFR se encuentran comprendidas entre
los exones 18-21 del mismo,
siendo las “clásicamente” asociadas a sensibilidad
con inhibidores de tirosina quinasa (ITQ) de EGFR
caracterizadas en el año 2004 (33). Estas mutaciones
son las deleciones en el exón 19 y la mutación puntual
L858R en el exón 21. Otras alteraciones moleculares
comprendidas en los exones 18 y 20 como mutaciones
puntuales consideradas infrecuentes activan la quinasa
en forma constitutiva y son también pasibles de inhibición con ITQ de
EGFR.
Se han desarrollado varios ITQ de EGFR siendo los
de primera generación erlotinib y gefitinib, inhibidores
de segunda generación afatinib y dacomitinib y el inhibidor de tercera
generación osimertinib los que están
comercialmente disponibles y aprobados en nuestra
región (34). En China, además se encuentra aprobado
el Icotinib, que es un inhibidor de primera generación
de EGFR (35). Los inhibidores de primera generación
y afatinib tienen un espectro de actividad similar con
tasas de respuesta que rondan entre el 62 y 84% de
acuerdo al estudio, sobrevidas libre de progresión entre 8 y 13 meses y
una sobrevida global de alrededor de
28 a 31 meses. En estudios comparativos no se observaron diferencias en
eficacia entre inhibidores de primera generación erlotinib y gefitinib
(CTONG 0901)
ni entre gefitinib y afatinib (LUX-LUNG 7)(36,37).
Dacomitinib, por el contrario, demostró mayor eficacia en términos de
supervivencia libre de progresión
y supervivencia global que gefitinib en el estudio ARCHER-1050, 14,7
meses comparado a 9,2 meses (HR
0,59; P < 0,0001) y 34.1 meses versus 26,8 meses (HR
0,76; P = 0,0438), respectivamente (38). En aquellos pacientes que
progresan a un inhibidor de primera o
segunda generación, con detección en plasma o tejido
de la mutación de resistencia T790M, son candidatos a
recibir tratamiento con osimertinib, el inhibidor de tercera generación
(39). Recientemente, osimertinib pasó
a ser un tratamiento estándar de primera línea basado
en los resultados del estudio FLAURA que comparó
osimertinib con inhibidores de primera generación
erlotinib o gefitinib, demostrando mejoría en sobrevida libre de
progresión y sobrevida global, 17,7 meses
versus 9,7 meses (HR 0,45; P < 0,001) y 38,6 versus
31,8 meses (HR 0,79; P = 0,046) (40).
Tabla 1. Resumen de los genes y alteraciones moleculares en
diferentes tipos de cancer que son categorizados como Tier
I por el ESCAT.
Las inserciones en el exón 20 de EGFR, también tienen un efecto
oncogénico, resultando en una activación constitutiva del receptor por
modificaciones estructurales que aumenta la afinidad de la quinasa por
el ATP (41). Sin embargo, estas últimas no son susceptibles a los
inhibidores comercialmente disponibles
en las dosis recomendadas. Nuevos inhibidores como
poziotinib, mobosertinib (TAK-788) y el uso de osimertinib al doble de
dosis (160 mg) tienen actividad
en este grupo de pacientes, aunque suele ser de menor
impacto que las mutaciones clásicas o de sensibilidad
(42). También se encuentran en desarrollo otras moléculas como
Amivantamab, un anticuerpo monoclonal
bi-específico MET-EGFR con resultados promisorios
en este grupo de pacientes. Asimismo, se encuentra en
proceso de ampliación el uso de inhibidores de EGFR
en estadios más precoces mostrando beneficio en termino de sobrevida
libre de enfermedad en pacientes
con cáncer de pulmón resecado EGFR mutados (43).
Si bien estas alteraciones moleculares pueden ser detectadas usando
métodos que estudian solo EGFR
como kits de PCR en tiempo real recomendados, el
uso de NGS en este grupo de pacientes puede identificar otras
alteraciones moleculares que pueden tener un
rol pronóstico. Por ejemplo la detección concomitante de mutaciones en
los genes RB1 y TP53 se asocian
con un mayor riesgo de transformación histológica a
carcinoma de células pequeñas y con menor sobrevida
libre de progresión (44). Lo mismo ha sido reportado
con las mutaciones de TP53 y aquellos tumores con
alta tasa mutaciones (TMB) (45). También, con la mayor profundidad de
secuenciación con NGS es posible
detectar al diagnóstico tumores que presentan poblaciones subclonales
con comutación de EGFR T790M
previo al inicio de tratamiento en primera línea, permitiendo la
selección de estos pacientes a tratamiento
con osimertinib.
En el monitoreo de respuesta y resistencia a estas terapias, el uso de
NGS cobra nueva relevancia. La negativización de la detección de
mutaciones de EGFR a los
3 y 6 meses de iniciado el tratamiento con inhibidores
de EGFR en biopsia líquida ha sido asociada a mejor
supervivencia (46). Esto puede tener implicancias futuras en el diseño
de estudios que utilicen intensificación
de tratamientos en pacientes que no presentan caída
de la frecuencia alélica utilizando combinaciones con
quimioterapia o antiangiogénicos entre otros tratamientos. En el
estudio de la resistencia a osimertinib el
uso de NGS probablemente tendrá un rol fundamental
para seleccionar tratamientos subsecuentes. La amplificación de
MET es un evento que ocurre entre
el 5%
y 15% de los tumores a la progresión con esta droga, y
combinaciones de inhibidores de MET y EGFR como
savolitinib con osimertinib han demostrado eficacia
clínica en el estudio TATTON (47). Entre otras causas
de resistencia que pueden ser identificadas con
NGS
están: mutaciones de resistencia como la EGFR C797S
entre otras, fusiones de genes como
ALK
y RET entre
otros, mutaciones de
BRAF y
otros oncogenes que activan vías de señalización paralelas a la
inhibición de
EGFR (48).
ALK
Los rearreglos o fusiones que involucran el dominio
tirosina quinasa de ALK ocurren en 3%-7% de los adenocarcinomas de
pulmón, y en alrededor del 50% tumores miofibroblástco inflamatorios
pediátricos y del
adulto. También las fusiones de ALK han sido reportadas ocasionalmente
en otros tipos de tumores como
adenocarcinoma de colon, tumores de ovario, tiroides,
cerebro (49). Mutaciones en el dominio tirosina quinasa de ALK son otro
mecanismo de activación constitutiva de este receptor y han sido
descripta solo en
neuroblastomas pediátricos.
Al momento se han desarrollado clinicamente seis inhibidores de ALK,
crizotinib un inhibidor de primera
generación, ceritinib, alectinib, brigatinib y ensartinib
de segunda generación y el inhibidor de tercera generación, lorlatinib.
El tratamiento con inhibidores de
ALK es altamente efectivo, llevando la supervivencia
de casi la mitad de los pacientes más allá de 4 años
desde el diagnóstico de enfermedad metastásica (50).
El primer tratamiento instaurado para este tipo de
tumores fue el uso de crizotinib, también inhibidor
de ROS1 y MET, que demostró ser superior al tratamiento con
quimioterapia. Gracias a la comprensión
de los mecanismos biológicos de resistencia que desarrollaban las
células tumorales como la mutación
ALK L1196M o G1269A se desarrollaron inhibidores de segunda generación
diseñados para unirse a
la quinasa de ALK en presencia de estas mutaciones
(51). De allí, el tratamiento con ceritinib, alectinib y
brigatinib en pacientes que presentan progresión de
enfermedad con crizotinib conlleva a una tasa de respuesta entre el 40%
y 56% y sobrevida libre de progresión entre 8 y 16 meses (34). El
tratamiento con
lorlatinib en pacientes que progresaron a crizotinib
y un inhibidor de segunda generación sería la tercera
línea de elección confiriendo tasas de respuesta del
40% y sobrevida libre de progresión de 6 meses (52).
Más recientemente, el abordaje de los pacientes con
tumores ALK dependientes a cambiado, con la evidencia clínica que los
inhibidores de segunda generación conllevan a una mayor sobrevida libre
de progresión, mayor control y menor incidencia de metástasis
cerebrales (53,54). Lo mismo se observa con el tratamiento en primera
línea con lorlatinib, con una franca
reducción del riesgo de progresión sistémica y cerebral
comparado con crizotinib (55).
El monitoreo de respuesta y resistencia a inhibidores
de ALK usando NGS también fue estudiado por varios
grupos de investigación, dando lugar al descubrimiento
de diversos mecanismos de resistencia a inhibidores de
ALK (56). A diferencia de los inhibidores de EGFR,
existen más de una decena de mutaciones de resistencia
a ITQ de ALK con sensibilidad diferencial de acuerdo
al tipo de mutación. Si bien el desarrollo de los inhibidores de ALK no
requirió la selección molecular de las
terapias con base en el perfil genómico del tumor a la
resistencia, el conocimiento de los mismos puede dirigir
mejor el tratamiento o estimar el potencial beneficio de
una terapia. Por ejemplo, en aquellos pacientes en cuyos
tumores o plasma se detectaron mutaciones de resistencia de ALK, la
tasa de respuesta con lorlatinib fue del
60% comparado con 30% en el grupo de pacientes en
los que no se identificaron mutaciones de resistencia de
ALK, lo que sugiere que lorlatinib es francamente más
activo contra tumores que presentan mecanismos de
resistencia ALK-dependientes (57). La secuenciación
de nueva generación también puede facilitar el entendimiento de la
distribución alélica de mutaciones de resistencia cuando se encuentran
dos o más mutaciones
del dominio tirosina quinasa de
ALK.
Las mutaciones
“compuestas” o en
cis
(presentes en el mismo alelo)
son el principal mecanismo de resistencia a lorlatinib
(58,59). Se pueden identificar si las dos mutaciones se
encuentran próximas en el mismo amplicon secuenciado. Esta
identificación puede tener implicancias en el
futuro ya que se encuentran en desarrollo fármacos específicos contra
mutaciones compuestas determinadas.
ROS1
Las fusiones que involucran el dominio tirosina quinasa de ROS1 son
menos frecuentes y rondan el 2% de
los adenocarcinomas pulmonares (60). Como ALK, las
fusiones de
ROS1 han sido
descriptas en otros tumores incluyendo colangiocarcinoma intrahepático,
tumores
del sistema nervioso central y sarcomas entre otros. El
diagnóstico clásico se realiza por tamizaje con inmunohistoquímica y
confirmación con FISH. El tratamiento
de pacientes con cáncer de pulmón con fusión de ROS1
es con inhibidores de tirosina quinasa como crizotinib
o entrectinib (61,62). En ambos casos, estos inhibidores
confieren tasas de respuesta de alrededor del 72%-77%
con supervivencia libre de progresión de 19 meses. Ya
se han descripto varias mutaciones de resistencia que
pueden ser detectadas por NGS en tejido o plasma que
causan resistencia a estos inhibidores, pero que son
susceptibles a inhibidores de nueva generación como
Repotrectinib o DS-6051b (63). Es posible que en el futuro cercano
seleccionemos el tratamiento subsecuente
conn base en estas mutaciones de resistencia, y el uso de
NGS sea necesario para identificarlas.
BRAF
La mutación
BRAF V600E, ya
bien conocida por sus
efectos en la biología tumoral del melanoma es también un blanco
terapéutico en cáncer de pulmón, carcinoma anaplásico de tiroides,
colangiocarcinomas, intrahepático y cáncer de colon. Esta mutación
permite
la fosforilación de BRAF y su señalización como un
monómero, independiente de la activación de efectores que activen la
vía de señalización de MAPK (64).
Su identificación en diferentes tumores tiene implicancias
terapéuticas, ya que se ha demostrado que el uso
combinado de inhibidores de BRAF y MEK conllevan
a tasas de respuesta significativas y control de enfermedad. Esto ha
sido observado para la combinación
de dabrafenib y trametinib en cáncer de pulmón, carcinomas anaplásico
de tiroides y colangiocarcinomas
(65–67). También los inhibidores de BRAF/MEK
combinados con anticuerpos monoclonales contra
EGFR son una opción de tratamiento en carcinomas
colorectales BRAF mutados. Hay kits aprobados de
PCR en tiempo real para el diagnóstico específico
de la mutación BRAF V600E. Sin embargo, debido a
que en el cáncer de pulmón y colangiocarcinomas por
ejemplo hay biomarcadores a estudiar, el uso de NGS
permite optimizar el material de biopsia para estudiar
múltiples biomarcadores en simultáneo.
La implementación de NGS en el estudio de resistencia a estos
inhibidores también ha permitido identificar alteraciones moleculares
en diversas vías como
la vía de MAPK y PI3K/AKT/mTOR como principales causas de resistencia
adquirida (ej: mutaciones
de NRAS, PTEN, etc) (68). Si bien esto no ha guiado
el desarrollo de nuevas terapias al momento, permite comprender mejor
como deberán desarrollarse las
nuevas estrategias terapéuticas en el futuro.
RET
La activación oncogénica del receptor RET se da por
dos vías principalmente, las fusiones del dominio
de tirosina quinasa de
RET o
mutaciones puntuales
(69). Los rearreglos de
RET
ocurren en el 5-10% de
los carcinomas papilares de tiroides, en el 1-2% de los
adenocarcinomas pulmonares, pero también han sido
ocasionalmente detectados en cáncer de mama, colon,
entre otros. Las mutaciones germinales puntuales en
el dominio extracelular (síndrome MEN2A) o en el
dominio de tirosina quinasa (síndrome MEN2B) se
asocian a la génesis de tumores hereditarios. Las mutaciones somáticas
son detectadas en alrededor del
65% de los carcinomas medulares de tiroides esporádicos, siendo los más
comunes el
RET M918T, E768D y
A883F. Con el advenimiento de NGS, también se han
detectado mutaciones de RET en feocromocitomas,
paragangliomas, cáncer de mama, cáncer de colon y
carcinoma de células de Merkel.
Existen varios inhibidores de tirosina quinasa no especificos de ret o
también llamados “multiquinasa” utilizados en el tratamiento de los
pacientes con cáncer de
tiroides. Sin embargo, recientemente, se han desarrollado inhibidores
específicos de RET como el selpercatinib (LOXO-292) y el pralsetinib
(BLU-667) (70,71).
Ambos inhibidores selectivos de RET han sido aprobados por la FDA para
el tratamiento de pacientes
con cáncer de pulmón y rearreglos de RET. La tasa
de respuesta con estos inhibidores es de alrededor del
61% al 85%, dependiendo de si son dados en primera línea o luego de
tratamiento con otros fármacos,
con duraciones de respuesta prolongadas y actividad
intracraneal.
NTRK
Los rearreglos de
NTRK1, NTRK2 y
NTRK3 pueden
ocurrir con frecuencias muy disímiles en un extenso
repertorio de tumores, siendo considerado un marcador agnóstico
predictor de eficacia a inhibidores de tirosina quinasa de NTRK (72).
Las fusiones de
NTRK
son casi patognomónicas en carcinoma secretorio mamario de
adultos e infantes (92% de los casos) y en
el fibrosarcoma juvenil (91-100% de los casos) y los
tumores salivares MASC (90-100%). Se encuentran
también frecuentemente en tumores spitzoides (16%),
nefroma congénito (83%); carcinomas de tiroides pediátricos (9-25%) y
adultos (1,5-14%) y tumores del
SNC pediátricos (10%). En tumores más prevalentes,
las fusiones de
NTRK son
infrecuentes: cáncer de pulmón (0,2%), colon (1,5%), melanoma (0,3%),
GIST
(3,2%), colangiocarcinoma (3,2%), tumores de cerebro
del adulto (0,4-3,1%). Estas alteraciones pueden ser tamizadas con
inmunohistoquímica en la mayor parte
de los tejidos y confirmado por FISH. Sin embargo, el
uso de NGS con paneles que detectan estas fusiones
permite incorporar el estudio de las mismas en el marco del estudio de
otros oncogenes.
El desarrollo de los inhibidores de NTRK de primera generación,
larotrectinib y entrectinib, involucró
un diverso grupo de pacientes con diferentes tipos tumorales (73,74).
Larotrectinib demostró unas tasas de
respuesta en pacientes adultos y pediátricos del 81%
con duraciones de respuestas prolongadas y buena
tolerancia. En pacientes adultos, la tasa de respuesta
con entrectinib fue del 57,4% con sobrevida libre de
progresión de 11,2 meses y sobrevida global de 20,9
meses. Interesantemente, debido al uso de NGS se
han descubierto mutaciones de resistencia homólogas
a otros genes similares como
ALK y
ROS1. Ya se encuentran en desarrollo fármacos como el
seletrecinib
y el repotrectinib para poder sobrellevar la resistencia,
inducidos por el tratamiento con inhibidores de primera generación
(63,75,76). Por ello, el uso de NGS al
diagnóstico y la resistencia serán de gran importancia
para guiar el tratamiento de estos pacientes.
FGFR
El gen del receptor del factor de crecimiento fibroblástico (FGFR) se
encuentra mutado en varios tumores
siendo las mutaciones de
FGFR3
las más frecuentes en
carcinomas uroteliales, en los que puede estar presente
en hasta el 20% de las muestras, especialmente de estirpe papilar y
bajo grado (19). También se identifican
fusiones de
FGFR3 y FGFR2 en
esta patología. Erdafitinib es un inhibidor de FGFR1-4 selectivo
aprobado
para esta indicación en pacientes con carcinoma urotelial avanzado y
alteraciones de FGFR. La tasa de respuesta con erdafitinib es del 40% y
la sobrevida libre
de progresión de 5,5 meses (77). Se estima que en otros
15 tumores se encuentran alteraciones de
FGFR que
podrían ser pasibles de tratamientos con este inhibidor,
representando una prevalencia de este biomarcador en
alrededor del 3,7% de los tumores (78). Pemigatinib
también fue recientemente aprobado para el tratamiento de pacientes con
colangiocarcinomas intrahepáticos
que tienen fusiones de
FGFR2.
La prevalencia de esta
alteracion es de alrededor del 7-9% de los colangiocarcinomas, y el
tratamiento con pemigatinib fue del 35%
y la mediana de sobrevida libre de progresión fue de
6,5 meses (79). El estudio mediante NGS en plasma y
tejido al momento de la progresión con inhibidores de
FGFR ha identificado varias mutaciones de resistencia en el dominio
tirosina quinasa (80). Hay múltiples estudios evaluando el tratamiento
con inhibidores de
FGFR en distintos tipos tumorales (81).
MET
El oncogén
MET participa del
desarrollo y propagación de múltiples tipos diferentes de cáncer a
través
de varios mecanismos: el empalme patogénico o “skipping” del exón 14,
mutaciones en el dominio de tirosina quinasa, la amplificación, la
sobreexpresión y las
fusiones que contienen el dominio tirosina quinasa
de
MET (82). Salvo la
sobreexpresión, los demás son
mecanismos que ocurren a nivel genómico y son todos detectables
utilizando secuenciación de próxima
generación. Las mutaciones o deleciones que afectan
los sitios dadores y aceptores de empalme o “splicing”
del exón 14 pueden ser detectados por NGS con paneles genómicos que
comprendan toda la extensión del
exón y sus intrones flanqueantes, permitiendo detectar
las más de 100 variantes que dan como resultado un
empalme patológico y pérdida del exón 14 (83). Esto
es más fácilmente detectable utilizando NGS a partir
de ARN como para la detección de fusiones. Mediante el uso de ARN por
secuenciación de nueva generación puede detectarse esta fusión
intragénica entre los
exones 13-15 que es el reflejo de la pérdida del exón
14. El dominio juxtamembrana que es codificado
parcialmente por exón 14 donde se contiene el residuo Y1003, que es
clave para la unión de la proteína
ubiquitinizadora CBL, participa en la degradación del
receptor. Cuando se produce la pérdida del exón 14 y
de este dominio yuxtamembrana del receptor, la vida
media del mismo se prolonga, resultando en señalización oncogénica. El
skipping del exón 14 puede ser detectado por PCR real time también, sin
embargo, este
método no ha sido validado. El “skipping” del exón 14
de
MET ocurre en alrededor
del 4% de los pacientes
con cáncer de pulmón, y es de suma importancia su
detección ya que hay inhibidores selectivos de MET
aprobados y en vías de aprobación para su uso en esta
indicación como capmatinib y tepotinib (84). Ambos
fármacos han demostrado beneficio clínico para los
pacientes, con tasas de respuesta que oscilan entre el
40 y 68% y sobrevida libre de progresión entre 5 y 9
meses de acuerdo con la línea de tratamiento en que
fueron utilizados.
El uso de NGS a la progresión ha permitido identificar varios
mecanismos de resistencia genómicos como
mutaciones puntuales en el dominio tirosina quinasa
(MET Y1230X, D1228X, L1195X) algunas siendo posibles de sobrellevar
utilizando inhibidores de tipo II de
MET como cabozantinib o merestinib (85). También
ha permitido identificar mecanismos de activación alternativa de vías
de señalización como amplificación
de
EGFR, KRAS y mutaciones de
KRAS que puede
orientar el desarrollo de fármacos como inhibidores
duales EGFR-MET. Así, la amplificación de MET
puede ser detectada mediante secuenciación de nueva generación, y en
pacientes con cáncer de pulmón y
amplificación de
MET
(definido como 10 o más copias
de
MET), datos iniciales con
inhibidores selectivos han
demostrado resultados promisorios. Para tumores con
mutaciones puntuales en el dominio tirosina quinasa
de
MET como los clásicamente
descriptos carcinomas
papilares renales, se encuentran en desarrollo tratamientos dirigidos,
pero no son tratamientos estándar
actualmente.
HER2
El oncogén
ERBB2 codifica
para la proteína HER2
que se encuentra amplificada en alrededor del 25% de
los cánceres de mama, liderando el desarrollo de las
terapias dirigidas contra
HER2
en esa patología. La
amplificación de
HER2 es
detectable por técnicas de
inmunohistoquímica y FISH o ISH. La amplificación
de
HER2 puede ser detectada
en otros tumores como
los adenocarcinomas gástricos, colangiocarcinomas
intrahepáticos y adenocarcinomas de endometrio y
cérvix. En cáncer de pulmón, las inserciones o duplicaciones en el exón
20 conllevan a la activación constitutiva de este receptor en 1-2% de
los pacientes (86).
Ha habido muchos intentos de trasladar el beneficio de
los anticuerpos monoclonales y anticuerpos conjugados como trastuzumab
y TDM1 en el tratamiento de
los pacientes con cáncer de pulmón e inserciones del
exón 20 de
HER2 (87). Sin
embargo, no se observó un
beneficio clínico significativo con estos tratamientos.
Recientemente el desarrollo de trastuzumab deruxtecan (DS-8201) ha
demostrado señales de actividad en
ese grupo de pacientes con tasas de respuesta del 62%
y sobrevida libre de progresión de 14 meses en este
grupo de pacientes (88,89).
KRAS
KRAS es uno de los oncogenes más frecuentemente mutados en cáncer y sin
embargo, hasta ahora no
había sido posible desarrollar tratamiento específicos
contra este blanco. La mutación
KRAS
G12C, presente en 9-11% de los cánceres de pulmón no escamosos,
de páncreas y colon, presenta una particularidad siendo que retiene
capacidad de hidrólisis de GTP para
pasar transitoriamente a una forma inactiva (90).
También en este contexto se forma un bolsillo críptico con la cisteína
en el codón 12 que es pasible de
inducir un bloqueo de la quinasa en estado inactivo
(unido a GDP) mediante un nuevo grupo de inhibidores covalentes.
Fármacos como sotorasib (AMG
510) y adagrasib (MRTX-849) son inhibidores selectivos de KRAS G12C con
tasas de respuesta del 32% y
45% respectivamente, reportados en la fase I/II de estos fármacos al
momento (91,92). Las mutaciones de
KRAS no eran rutinariamente estudiadas en cáncer de
pulmón, pero se ha modficado debido al desarrollo de
estos fármacos y la disponibilidad de ensayos clínicos
para los pacientes. Las mutaciones de KRAS también
sirven como un biomarcador pronóstico negativo en
cáncer de colon para el tratamiento con anticuerpos
monoclonales contra EGFR. Estas mutaciones pueden también estudiarse
por PCR real time utilizando
kits validados.
Carga mutacional tumoral (TMB)
El valor de la carga tumoral es discutida en la práctica clínica como
un biomarcador aislado de beneficio
al tratamiento con inmunoterapia con inhibidores de
punto de control del eje PD-1/PD-L1 y de CTLA-4.
El TMB es el número de mutaciones somáticas en regiones codificantes,
no sinónimas, por megabase de
ADN. Trabajos iniciales en cáncer de pulmón utilizando secuenciación de
exomas mostraban un beneficio en pacientes cuyos tumores presentaban un
valor
alto de TMB (93). Sin embargo esto no se replicó de
manera consistente en todos los escenarios, siendo un
facor asociado a beneficio en algunos ensayos como el
CheckMate-026 con nivolumab, el estudio MYSTIC
con durvalumab, el estudio CheckMate 227 con ipilimumab y nivolumab y
análisis
post hoc del KEYNOTE
042 y 010 (94–96). Sin embargo, esto no se ha replicado en otros
estudios de combinación de inmunoterapia con inmunoterapia.
El estudio KEYNOTE-158 es un estudio de fase 2 de
múltiples brazos que revisó el rol de pembrolizumab
en pacientes cuyos tumores (10 tipos tumorales) tenían
una tasa mutacional mayor o igual a 10 mutaciones
por megabase, utilizando la plataforma de Foundation
Medicine (97). La tasa de respuesta en el grupo de
TMB alto fue del 29% (30/102), incluyendo respuestas
en pacientes con cáncer de cuello uterino, endometrio,
neuroendocrinos de bajo o moderado grado, tumores
salivares, carcinoma de células pequeñas de pulmón,
cáncer de tiroides y vulva. En pacientes con tumores
anales, biliares y mesotelioma la tasa de respuesta fue
mayor en tumores con TMB bajo. La FDA aprobó el
uso de pembrolizumab en tumores con más de 10 mutaciones por megabase
de TMB independiente del tipo
de tumor, si bien solo estaban incluidos ciertos subtipos tumorales en
el estudio.
Uno de los principales desafíos del TMB es la falta de
armonización entre las diferentes plataformas. Aunque se están llevando
a cabo esfuerzos para hacerlo, aquellos paneles que no realizan
secuenciación germinal en
simultáneo con el tumor tienden a reportar valores de
TMB más bajos que quienes filtran por variantes germinales (98) 297. Lo
que sí es consistente a través de
los diferentes estudios es la pobre correlacón entre el
TMB y la expresión de PD-L1, lo que los convierten
en biomarcadores independientes y complementarios
a la hora de decidir tratamientos (99).
Desafíos para la implementación de
NGS en Latinoamérica
Aun cuando todo lo anteriormente reportado denota
un escenario ideal de acceso a secuenciación masiva
y tratamientos innovadores, en nuestra región existen
severas disparidades en el acceso a la atención oncológica, al
diagnóstico histológico y tratamientos estándares (100). Las
tecnologías para la implementación
de secuenciación de nueva generación no está ampliamente disponible en
el continente, si bien hay equipamientos distribuidos en las grandes
urbes que permiten
este estudio. También se encuentran disponibles plataformas
internacionales de secuenciación como Foundation Medicine, Caris y
otras. Sin embargo, el valor
que tienen estos estudios puede rondar los USD$3.000
- USD$4.000, que constituyen un alto costo a pagar
para la mayoría de los pacientes en países en vías de
desarrollo como son la mayoría en nuestro continente.
También, la interpretación de estos resultados requiere
del trabajo en equipo y el desarrollo de comités moleculares para poder
evaluar la patogenicidad y accionabilidad de estas alteraciones
moleculares y abocar o dirigir al paciente al mejor tratamiento
disponible (101).
Conflictos de interés
El autor funge como consultor/asesor de Amgen,
Pfizer, Roche.
Financiación de la investigación
Amgen. Becas de viaje: AstraZeneca, Pfizer.
Conclusiones
La secuenciación de nueva generación es una herramienta fundamental
para el diagnóstico molecular
moderno, permitiendo identificar en los tumores o
plasma de las personas con cáncer alteraciones moleculares que permiten
dirigir con precisión el tratamiento oncológico. Esta implementación
tecnológica
debe ser hecha de manera accesible y en condiciones
en las que el acceso de los pacientes a los medicamentos aprobados, a
ensayo clínicos y a moléculas en uso
compasivo sea posible.
Referencias
1. Weinstein JN, Collisson EA, Mills
GB, Shaw KRM, Ozenberger BA, Ellrott K et al. The Cancer Genome Atlas
PanCancer analysis project. Nat Genet. 2013;45(10):1113–
20.
2. Li X, Warner JL. A Review of
Precision Oncology Knowledgebases for Determining the Clinical
Actionability of Genetic Variants. Front cell Dev Biol. 2020;8:48.
3. Goodwin S, McPherson JD, McCombie
WR. Coming of
age: ten years of next-generation sequencing technologies. Nat Rev
Genet. 2016;17(6):333–51.
4. Zehir A, Benayed R, Shah RH, Syed
A, Middha S, Kim
HR, et al. Mutational landscape of metastatic cancer revealed from
prospective clinical sequencing of 10,000
patients. Nat Med. 2017;23(6):703–13.
5. Shames DS, Wistuba II. The
evolving genomic classification of lung cancer. J Pathol.
2014;232(2):121–33.
6. Inamura K. Update on
Immunohistochemistry for the Diagnosis of Lung Cancer. Cancers (Basel).
2018;10(3):72.
7. Tsiatis AC, Norris-Kirby A, Rich
RG, Hafez MJ, Gocke CD,
Eshleman JR, et al. Comparison of Sanger sequencing,
pyrosequencing, and melting curve analysis for the detection of KRAS
mutations: diagnostic and clinical implications. J Mol Diagn.
2010;12(4):425–32.
8. Normanno N, Denis MG, Thress KS,
Ratcliffe M, Reck
M. Guide to detecting epidermal growth factor receptor
(EGFR) mutations in ctDNA of patients with advanced
non-small-cell lung cancer. Oncotarget. 2017;8(7):12501–
16.
9. Kalemkerian GP, Narula N, Kennedy
EB, Biermann WA,
Donington J, Leighl NB, et al. Molecular Testing Guideline for the
Selection of Patients With Lung Cancer for
Treatment With Targeted Tyrosine Kinase Inhibitors:
American Society of Clinical Oncology Endorsement of
the College of American Pathologists/International Association for the
. J Clin Oncol. 2018;36(9):911–9.
10. Guo R, Berry LD, Aisner DL,
Sheren J, Boyle T, Bunn PAJ,
et al. MET IHC Is a Poor Screen for MET Amplification or
MET Exon 14 Mutations in Lung Adenocarcinomas: Data
from a Tri-Institutional Cohort of the Lung Cancer Mutation Consortium.
J Thorac Oncol. 2019;14(9):1666–71.
11. Descarpentries C, Lepretre F,
Escande F, Kherrouche Z,
Figeac M, Sebda S et al. Optimization of Routine Testing
for MET Exon 14 Splice Site Mutations in NSCLC Patients. J Thorac
Oncol. 2018;13(12):1873–83.
12. Pennell NA, Mutebi A, Zhou Z-Y,
Ricculli ML, Tang W,
Wang H, et al. Economic Impact of Next-Generation Sequencing Versus
Single-Gene Testing to Detect Genomic
Alterations in Metastatic Non–Small-Cell Lung Cancer
Using a Decision Analytic Model. JCO Precis Oncol.
201916;(3):1–9.
13. Massard C, Michiels S, Ferte C,
Le Deley M-C, Lacroix
L, Hollebecque A, et al. High-Throughput Genomics
and Clinical Outcome in Hard-to-Treat Advanced Cancers: Results of the
MOSCATO 01 Trial. Cancer Discov.
2017;7(6):586–95.
14. Rodon J, Soria J-C, Berger R,
Miller WH, Rubin E, Kugel
A, et al. Genomic and transcriptomic profiling expands
precision cancer medicine: the WINTHER trial. Nat Med.
2019;25(5):751–8.
15. Sicklick JK, Kato S, Okamura R,
Schwaederle M, Hahn
ME, Williams CB, et al. Molecular profiling of cancer patients enables
personalized combination therapy: the IPREDICT study. Nat Med.
2019;25(5):744–50.
16. Jordan EJ, Kim HR, Arcila ME,
Barron D, Chakravarty
D, Gao J, et al. Prospective Comprehensive Molecular
Characterization of Lung Adenocarcinomas for Efficient
Patient Matching to Approved and Emerging Therapies.
Cancer Discov. 2017;7(6):596–609.
17. Sholl LM, Aisner DL,
Varella-Garcia M, Berry LD, DiasSantagata D, Wistuba II et al.
Multi-institutional Oncogenic Driver Mutation Analysis in Lung
Adenocarcinoma. J
Thorac Oncol. 2015;10(5):768–777.
18. Barlesi F, Mazieres J, Merlio
J-P, Debieuvre D, Mosser J,
Lena H et al. Routine molecular profiling of patients with
advanced non-small-cell lung cancer: results of a 1-year
nationwide programme of the French Cooperative Thoracic
Intergroup (IFCT). Lancet . 2016;387(10026):1415-1426.
19. Knowles MA, Hurst CD. Molecular
biology of bladder cancer: new insights into pathogenesis and clinical
diversity.
Nat Rev Cancer. 2015;15(1):25–41.
20. Lamarca A, Kapacee Z, Breeze M,
Bell C, Belcher D,
Staiger H et al. Molecular Profiling in Daily Clinical Practice:
Practicalities in Advanced Cholangiocarcinoma and
Other Biliary Tract Cancers. J Clin Med. 2020;9(9):2854.
21. Konstantinopoulos PA, Norquist B,
Lacchetti C, Armstrong D, Grisham RN, Goodfellow PJ et al. Germline
and Somatic Tumor Testing in Epithelial Ovarian Cancer:
ASCO Guideline. J Clin Oncol. 2020;38(11):1222–45.
22. Yoo S-K, Song YS, Lee EK, Hwang
J, Kim HH, Jung G,
et al. Integrative analysis of genomic and transcriptomic
characteristics associated with progression of aggressive
thyroid cancer. Nat Commun. 2019;10(1):2764.
23. Talhouk A, McConechy MK, Leung S,
Li-Chang HH,
Kwon JS, Melnyk N et al. A clinically applicable molecularbased
classification for endometrial cancers. Br J Cancer.
2015;113(2):299–310.
24. Chang Y, Tolani B, Nie X, Zhi X,
Hu M, He B. Review of
the clinical applications and technological advances of circulating
tumor DNA in cancer monitoring. Ther Clin Risk
Manag. 2017;13:1363–74.
25. Jiang J, Adams H-P, Lange M,
Siemann S, Feldkamp M,
McNamara S et al. Plasma-based longitudinal mutation
monitoring as a potential predictor of disease progression
in subjects with adenocarcinoma in advanced non-small
cell lung cancer. BMC Cancer. 2020;20(1):885.
26. Tarazona N, Gimeno-Valiente F,
Gambardella V, Zuñiga
S, Rentero-Garrido P, Huerta M et al. Targeted next-generation
sequencing of circulating-tumor DNA for tracking
minimal residual disease in localized colon cancer. Ann
Oncol. 2019;30(11):1804–12.
27. Kang J-K, Heo S, Kim H-P, Song
S-H, Yun H, Han S-W et
al. Liquid biopsy-based tumor profiling for metastatic colorectal
cancer patients with ultra-deep targeted sequencing. PLoS One .
2020;15(5):e0232754.
28. Rotow J, Bivona TG. Understanding
and targeting resistance mechanisms in NSCLC. Nat Rev Cancer.
2017;17(11):637–58.
29. Recondo G, Mahjoubi L, Maillard
A, Loriot Y, Bigot L, Facchinetti F et al. Feasibility and first
reports of the MATCHR repeated biopsy trial at Gustave Roussy. NPJ
Precis
Oncol. 2020;4:27.
30. Mosele F, Remon J, Mateo J,
Westphalen CB, Barlesi F,
Lolkema MP et al. Recommendations for the use of nextgeneration
sequencing (NGS) for patients with metastatic cancers: a report from
the ESMO Precision Medicine
Working Group. Ann Oncol Off J Eur Soc Med Oncol.
2020;(11):1491-505.
31. Mateo J, Chakravarty D,
Dienstmann R, Jezdic S, Gonzalez-Perez A, Lopez-Bigas N, et al. A
framework to rank
genomic alterations as targets for cancer precision medicine: the ESMO
Scale for Clinical Actionability of molecular Targets (ESCAT). Ann
Oncol. 2018;29(9):1895–902
32. Herbst RS. Review of epidermal
growth factor receptor biology. Int J Radiat Oncol Biol Phys. 2004;59(2
Suppl):21–6.
33. Paez JG, Janne PA, Lee JC, Tracy
S, Greulich H, Gabriel S, et al. EGFR mutations in lung cancer:
correlation with clinical response to gefitinib therapy. Science.
2004;304(5676):1497–500.
34. Recondo G, Facchinetti F,
Olaussen KA, Besse B, Friboulet L. Making the first move in EGFR-driven
or ALK-driven
NSCLC: first-generation or next-generation TKI? Nat Rev
Clin Oncol. 2018;15(11):694-708.
35. Shi Y, Zhang L, Liu X, Zhou C,
Zhang L, Zhang S et al.
Icotinib versus gefitinib in previously treated advanced
non-small-cell lung cancer (ICOGEN): a randomised,
double-blind phase 3 non-inferiority trial. Lancet Oncol.
2013;14(10):953–61.
36. Yang JJ, Zhou Q, Yan HH, Zhang
XC, Chen HJ, Tu HY
et al. A phase III randomised controlled trial of erlotinib
vs gefitinib in advanced non-small cell lung cancer with
EGFR mutations. Br J Cancer. 2017;116(5):568–74.
37. Paz-Ares L, Tan E-H, O’Byrne K,
Zhang L, Hirsh V, Boyer M et al. Afatinib versus gefitinib in patients
with EGFR
mutation-positive advanced non-small-cell lung cancer:
overall survival data from the phase IIb LUX-Lung 7 trial.
Ann Oncol. 2017;28(2):270–7.
38. Mok TS, Cheng Y, Zhou X, Lee KH,
Nakagawa K, Niho
S et al. Improvement in Overall Survival in a Randomized Study That
Compared Dacomitinib With Gefitinib in Patients With Advanced
Non-Small-Cell Lung
Cancer and EGFR-Activating Mutations. J Clin Oncol.
2018;36(22):2244-2250.
39. Mok TS, Wu Y-L, Ahn M-J,
Garassino MC, Kim HR, Ramalingam SS et al. Osimertinib or
Platinum-Pemetrexed
in EGFR T790M-Positive Lung Cancer. N Engl J Med.
2017 ;376(7):629–40.
40. Ramalingam SS, Vansteenkiste J,
Planchard D, Cho BC,
Gray JE, Ohe Y et al. Overall Survival with Osimertinib in
Untreated, EGFR-Mutated Advanced NSCLC. N Engl J
Med. 2020;382(1):41–50.
41. Robichaux JP, Elamin YY, Tan Z,
Carter BW, Zhang S, Liu
S et al. Mechanisms and clinical activity of an EGFR and
HER2 exon 20-selective kinase inhibitor in non-small cell
lung cancer. Nat Med. 2018;24(5):638–46.
42. Remon J, Hendriks LEL, Cardona
AF, Besse B. EGFR
exon 20 insertions in advanced non-small cell lung cancer:
A new history begins. Cancer Treat Rev. 2020;90:102105.
43. Wu Y-L, Tsuboi M, He J, John T,
Grohe C, Majem M et al.
Osimertinib in Resected EGFR-Mutated Non-Small-Cell
Lung Cancer. N Engl J Med. 2020;383(18):1711–23.
44. Offin M, Chan JM, Tenet M, Rizvi
HA, Shen R, Riely GJ
et al. Concurrent RB1 and TP53 Alterations Define a Subset of
EGFR-Mutant Lung Cancers at risk for Histologic
Transformation and Inferior Clinical Outcomes. J Thorac
Oncol. 2019;14(10):1784–93.
45. Offin M, Rizvi H, Tenet M, Ni A,
Sanchez-Vega F, Li BT et
al. Tumor Mutation Burden and Efficacy of EGFR-Tyrosine Kinase
Inhibitors in Patients with EGFR-Mutant Lung
Cancers. Clin cancer Res. 2019;25(3):1063–9.
46. Provencio-Pulla M, Serna R,
Franco F, Sanchez A, García
Girón C, Domine M et al. ctDNA levels before treatment
predict survival in non-small cell lung cancer patients
treated with a tyrosine kinase inhibitor. J Clin Oncol. 2020
20;38(15_suppl):9542.
47. Sequist L V, Han J-Y, Ahn M-J,
Cho BC, Yu H, Kim S-W
et al. Osimertinib plus savolitinib in patients with EGFR
mutation-positive, MET-amplified, non-small-cell lung
cancer after progression on EGFR tyrosine kinase inhibitors: interim
results from a multicentre, open-label, phase
1b study. Lancet Oncol. 2020;21(3):373–86.
48. Leonetti A, Sharma S, Minari R,
Perego P, Giovannetti E, Tiseo M. Resistance mechanisms to osimertinib
in
EGFR-mutated non-small cell lung cancer. Br J Cancer.
2019;121(9):725–37.
49. Hallberg B, Palmer RH.
Mechanistic insight into ALK receptor tyrosine kinase in human cancer
biology. Nat Rev
Cancer. 2013;13(10):685–700.
50. Solomon BJ, Kim D-W, Wu Y-L,
Nakagawa K, Mekhail T,
Felip E et al. Final Overall Survival Analysis From a Study Comparing
First-Line Crizotinib Versus Chemotherapy
in ALK-Mutation-Positive Non-Small-Cell Lung Cancer. J
Clin Oncol. 2018;36(22):2251-2258.
51. Katayama R, Shaw AT, Khan TM,
Mino-Kenudson M,
Solomon BJ, Halmos B, et al. Mechanisms of Acquired
Crizotinib Resistance in ALK- Rearranged Lung Cancers.
Sci Transl Med Febr. 2012;8(4120):120–17.
52. Solomon BJ, Besse B, Bauer TM,
Felip E, Soo RA, Camidge DR et al. Lorlatinib in patients with
ALK-positive
non-small-cell lung cancer: results from a global phase 2
study. Lancet Oncol. 2018;19(12):1654-1667.
53. Peters S, Camidge DR, Shaw AT,
Gadgeel S, Ahn JS,
Kim D-W, et al. Alectinib versus Crizotinib in Untreated
ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med.
2017;377(9):829–38.
54. Camidge DR, Kim HR, Ahn M-J, Yang
JC-H, Han
J-Y, Lee J-S et al. Brigatinib versus Crizotinib in ALKPositive
Non-Small-Cell Lung Cancer. N Engl J Med.
2018;379(21):2027-2039.
55. Shaw AT, Bauer TM, de Marinis F,
Felip E, Goto Y, Liu G, et
al. First-Line Lorlatinib or Crizotinib in Advanced ALK-Positive Lung
Cancer. N Engl J Med. 2020;383(21):2018–29.
56. Gainor JF, Dardaei L, Yoda S,
Friboulet L, Leshchiner
I, Katayama R, et al. Molecular Mechanisms of Resistance to First- and
Second-Generation ALK Inhibitors in ALK-Rearranged Lung Cancer. Cancer
Discov.
2016;6(10):1118–33.
57. Shaw AT, Solomon BJ, Besse B,
Bauer TM, Lin C-C,
Soo RA et al. ALK Resistance Mutations and Efficacy
of Lorlatinib in Advanced Anaplastic Lymphoma KinasePositive
Non-Small-Cell Lung Cancer. J Clin Oncol.
2019;37(16):1370–9.
58. Yoda S, Lin JJ, Lawrence MS,
Burke BJ, Friboulet L, Langenbucher A et al. Sequential ALK Inhibitors
Can Select
for Lorlatinib-Resistant Compound ALK Mutations in ALKPositive Lung
Cancer. Cancer Discov. 2018;8(6):714-729.
59. Recondo G, Mezquita L,
Facchinetti F, Planchard D, Gazzah A, Bigot L, et al. Diverse
Resistance Mechanisms to the
Third-Generation ALK Inhibitor Lorlatinib in ALK-Rearranged Lung
Cancer. Clin cancer Res. 2020;26(1):242–55.
60. Davies KD, Doebele RC. Molecular
pathways: ROS1
fusion proteins in cancer. Clin cancer Res. 2013;19(15):
4040–5.
61. Shaw AT, Ou S-HI, Bang Y-J,
Camidge DR, Solomon BJ,
Salgia R et al. Crizotinib in ROS1 -Rearranged Non–SmallCell Lung
Cancer. N Engl J Med. 2014;371(21):1963–71.
62. Drilon A, Siena S, Dziadziuszko
R, Barlesi F, Krebs MG,
Shaw AT et al. Entrectinib in ROS1 fusion-positive nonsmall-cell lung
cancer: integrated analysis of three phase
1-2 trials. Lancet Oncol. 2020;21(2):261–70.
63. Drilon A, Ou S-HI, Cho BC, Kim
D-W, Lee J, Lin JJ et
al. Repotrectinib (TPX-0005) Is a Next-Generation
ROS1/TRK/ALK Inhibitor That Potently Inhibits ROS1/
TRK/ALK Solvent- Front Mutations. Cancer Discov.
2018;8(10):1227–36.
64. Yaeger R, Corcoran RB. Targeting
Alterations in the RAFMEK Pathway. Cancer Discov. 2019;9(3):329–41.
65. Planchard D, Besse B, Groen HJM,
Souquet P-J, Quoix
E, Baik CS et al. Dabrafenib plus trametinib in patients
with previously treated BRAF(V600E)-mutant metastatic
non-small cell lung cancer: an open-label, multicentre
phase 2 trial. Lancet Oncol. 2016;17(7):984–93.
66. Subbiah V, Kreitman RJ, Wainberg
ZA, Cho JY, Schellens JHM, Soria JC et al. Dabrafenib and Trametinib
Treatment in Patients With Locally Advanced or Metastatic BRAF
V600-Mutant Anaplastic Thyroid Cancer. J Clin
Oncol. 2018;36(1):7–13.
67. Subbiah V, Lassen U, Élez E,
Italiano A, Curigliano G,
Javle M, et al. Dabrafenib plus trametinib in patients with
BRAF(V600E)-mutated biliary tract cancer (ROAR): a
phase 2, open-label, single-arm, multicentre basket trial.
Lancet Oncol. 2020;21(9):1234–43.
68. Ortiz-Cuaran S, Mezquita L,
Swalduz A, Aldea M, Mazieres J, Leonce C et al. Circulating Tumor DNA
Genomics
Reveal Potential Mechanisms of Resistance to BRAFTargeted Therapies in
Patients with BRAF-Mutant Metastatic Non-Small Cell Lung Cancer. Clin
cancer Res.
2020;26(23):6242-6253.
69. Subbiah V, Cote GJ. Advances in
Targeting RET-Dependent Cancers. Cancer Discov. 2020;10(4):498–505.
70. Drilon A, Oxnard GR, Tan DSW,
Loong HHF, Johnson M,
Gainor J et al. Efficacy of Selpercatinib in RET FusionPositive
Non-Small-Cell Lung Cancer. N Engl J Med.
2020;383(9):813–24.
71. Subbiah V, Gainor JF, Rahal R,
Brubaker JD, Kim JL, Maynard M et al. Precision Targeted Therapy with
BLU-667 for
RET-Driven Cancers. Cancer Discov. 2018;8(7):836–49.
72. Cocco E, Scaltriti M, Drilon A.
NTRK fusion-positive
cancers and TRK inhibitor therapy. Nat Rev Clin Oncol.
2018;15(12):731–47.
73. Drilon A, Laetsch TW, Kummar S,
DuBois SG, Lassen
UN, Demetri GD, et al. Efficacy of Larotrectinib in TRK
Fusion-Positive Cancers in Adults and Children. N Engl J
Med. 2018;378(8):731–9.
74. Doebele RC, Drilon A, Paz-Ares L,
Siena S, Shaw AT,
Farago AF, et al. Entrectinib in patients with advanced
or metastatic NTRK fusion-positive solid tumours: integrated analysis
of three phase 1-2 trials. Lancet Oncol.
2020;21(2):271–82.
75. Fuse MJ, Okada K, Oh-Hara T,
Ogura H, Fujita N, Katayama R. Mechanisms of Resistance to NTRK
Inhibitors
and Therapeutic Strategies in NTRK1-Rearranged Cancers. Mol Cancer
Ther. 2017;16(10):2130–43.
76. Drilon A, Nagasubramanian R,
Blake JF, Ku N, Tuch BB,
Ebata K et al. A Next-Generation TRK Kinase Inhibitor
Overcomes Acquired Resistance to Prior TRK Kinase
Inhibition in Patients with TRK Fusion-Positive Solid Tumors. Cancer
Discov. 2017;7(9):963–72.
77. Loriot Y, Necchi A, Park SH,
Garcia-Donas J, Huddart
R, Burgess E et al. Erdafitinib in Locally Advanced
or Metastatic Urothelial Carcinoma. N Engl J Med.
2019;381(4):338–48.
78. de Almeida Carvalho LM, de
Oliveira Sapori Avelar S,
Haslam A, Gill J, Prasad V. Estimation of Percentage of
Patients With Fibroblast Growth Factor Receptor Alterations Eligible
for Off-label Use of Erdafitinib. JAMA Netw
Open. 2019;2(11):e1916091.
79. Abou-Alfa GK, Sahai V,
Hollebecque A, Vaccaro G, Melisi D, Al-Rajabi R et al. Pemigatinib for
previously treated, locally advanced or metastatic cholangiocarcinoma:
a multicentre, open-label, phase 2 study. Lancet Oncol.
2020;21(5):671–84.
80. Silverman IM, Hollebecque A,
Friboulet L, Owens S, Newton RC, Zhen H, et al. Clinicogenomic analysis
of FGFR2-
rearranged cholangiocarcinoma identifies correlates of
response and mechanisms of resistance to pemigatinib.
Cancer Discov. 2020;:CD-20-0766.
81. Facchinetti F, Hollebecque A,
Bahleda R, Loriot Y, Olaussen KA, Massard C, et al. Facts and New Hopes
on Selective FGFR Inhibitors in Solid Tumors. Clin cancer Res.
2020;26(4):764–74.
82. Recondo G, Che J, Jänne PA, Awad
MM. Targeting MET
Dysregulation in Cancer. Cancer Discov. 2020;10(7):922–34.
83. Frampton GM, Ali SM, Rosenzweig
M, Chmielecki J, Lu
X, Bauer TM et al. Activation of MET via diverse exon 14
splicing alterations occurs in multiple tumor types and
confers clinical sensitivity to MET inhibitors. Cancer Discov.
2015;5(8):850–9.
84. Awad MM, Oxnard GR, Jackman DM,
Savukoski DO, Hall
D, Shivdasani P et al. MET Exon 14 Mutations in NonSmall-Cell Lung
Cancer Are Associated With Advanced
Age and Stage-Dependent MET Genomic Amplification
and c-Met Overexpression. J Clin Oncol. 2016;34(7):721–
30.
85. Fujino T, Kobayashi Y, Suda K,
Koga T, Nishino M, Ohara
S et al. Sensitivity and Resistance of MET Exon 14 Mutations in Lung
Cancer to Eight MET Tyrosine Kinase Inhibitors In Vitro. J Thorac
Oncol. 2019;14(10):1753-1765.
86. Arcila ME, Chaft JE, Nafa K,
Roy-Chowdhuri S, Lau C,
Zaidinski M et al. Prevalence, clinicopathologic associations, and
molecular spectrum of ERBB2 (HER2) tyrosine
kinase mutations in lung adenocarcinomas. Clin Cancer
Res. 2012;18(18):4910–8.
87. Li BT, Shen R, Buonocore D, Olah
ZT, Ni A, Ginsberg
MS et al. Ado-Trastuzumab Emtansine for Patients With
HER2-Mutant Lung Cancers: Results From a Phase II
Basket Trial. J Clin Oncol. 2018;36(24):2532–7.
88. Tsurutani J, Iwata H, Krop I,
Jänne PA, Doi T, Takahashi
S et al. Targeting HER2 with Trastuzumab Deruxtecan:
A Dose-Expansion, Phase I Study in Multiple Advanced
Solid Tumors. Cancer Discov. 2020;10(5):688–701.
89. Smit EF, Nakagawa K, Nagasaka M,
Felip E, Goto Y, Li BT
et al. Trastuzumab deruxtecan (T-DXd; DS-8201) in patients with
HER2-mutated metastatic non-small cell lung
cancer (NSCLC): Interim results of DESTINY-Lung01. J
Clin Oncol . 2020;38(15_suppl):9504.
90. Moore AR, Rosenberg SC, McCormick
F, Malek S. RAStargeted therapies: is the undruggable drugged? Nat Rev
Drug Discov. 2020;19(8):533–52.
91. Hong DS, Fakih MG, Strickler JH,
Desai J, Durm GA, Shapiro GI et al. KRAS(G12C) Inhibition with
Sotorasib in Advanced Solid Tumors. N Engl J Med. 2020;383(13):1207–
17.
92. Hallin J, Engstrom LD, Hargis L,
Calinisan A, Aranda R,
Briere DM et al. The KRAS(G12C) Inhibitor MRTX849
Provides Insight toward Therapeutic Susceptibility of
KRAS-Mutant Cancers in Mouse Models and Patients.
Cancer Discov. 2020;10(1):54–71.
93. Rizvi N a., Hellmann MD, Snyder
a., Kvistborg P, Makarov V, Havel JJ, et al. Mutational landscape
determines
sensitivity to PD-1 blockade in non-small cell lung cancer.
Science. 2015;348(6230):124-128.
94. Herbst RS, Lopes G, Kowalski DM,
Nishio M, Wu Y-L, de
Castro Junior G et al. LBA79 - Association between tissue
TMB (tTMB) and clinical outcomes with pembrolizumab
monotherapy (pembro) in PD-L1-positive advanced NSCLC in the
KEYNOTE-010 and -042 trials. Ann Oncol.
2019;30:916–7.
95. Peters S, Cho BC, Reinmuth N, Lee
KH, Luft A, Ahn M-J
et al. Abstract CT074: Tumor mutational burden (TMB) as
a biomarker of survival in metastatic non-small cell lung
cancer (mNSCLC): Blood and tissue TMB analysis from
MYSTIC, a Phase III study of first-line durvalumab ± tremelimumab vs
chemotherapy. Clinical Trials2019;.
96. Sholl LM, Hirsch FR, Hwang D,
Botling J, Lopez-Rios F,
Bubendorf L et al. The Promises and Challenges of Tumor Mutation Burden
as an Immunotherapy Biomarker: A
Perspective from the International Association for the Study of Lung
Cancer Pathology Committee. J Thorac Oncol.
2020;15(9):1409–24.
97. Marabelle A, Fakih M, Lopez J,
Shah M, Shapira-Frommer R, Nakagawa K et al. Association of tumour
mutational burden with outcomes in patients with advanced solid
tumours treated with pembrolizumab: prospective biomarker analysis of
the multicohort, open-label, phase 2 KEYNOTE-158 study. Lancet Oncol.
2020;21(10):1353–65.
98. Vokes NI, Liu D, Ricciuti B,
Jimenez-Aguilar E, Rizvi H,
Dietlein F et al. Harmonization of Tumor Mutational Burden
Quantification and Association With Response to
Immune Checkpoint Blockade in Non–Small-Cell Lung
Cancer. JCO Precis Oncol . 2019 12;(3):1–12.
99. Lamberti G, Spurr LF, Li Y,
Ricciuti B, Recondo G, Umeton R et al. Clinicopathological and genomic
correlates
of programmed cell death ligand 1 (PD-L1) expression
in nonsquamous non-small-cell lung cancer. Ann Oncoll.
2020;S0923-7534(20):36078-6.
100. Calderón-Aparicio A, Orue A.
Precision oncology in Latin
America: current situation, challenges and perspectives.
Ecancermedicalscience. 2019:13.
101. Kurnit KC, Dumbrava EEI,
Litzenburger B, Khotskaya YB,
Johnson AM, Yap TA, et al. Precision Oncology Decision
Support: Current Approaches and Strategies for the Future. Clin Cancer
Res . 2018;24(12):2719–2731.
Recibido:
Noviembre 24, 2020
Aprobado: Noviembre 24,
2020
Correspondencia:
Gonzalo Recondo
grecondoh@cemic.edu.ar




