VIH/SIDA, LA PANDEMIA DEL CAMBIO DE MILENIO
Ángela María Ruiz Sternberg1 , Eduardo Barajas Sandoval2
Resumen
La irrupción del VIH-SIDA en el panorama de las enfermedades
contemporáneas, significó retos
insospechados para la ciencia y desató fenómenos inéditos dentro de la
cultura popular y el manejo
de las políticas públicas. Este artículo hace un recuento de la lucha
contra la pandemia desde los
momentos inciertos de las exploraciones iniciales para identificar su
origen, hasta el hallazgo de medicamentos antivirales que han logrado
frenar el ritmo de su expansión. Además de repasar las cifras
de los estragos que el SIDA ha causado en ciertas poblaciones, presenta
la secuencia de las principales
creencias y reacciones sociales que, por una parte facilitaron el
surgimiento de una cultura de discriminación en contra de ciertos
grupos sociales, y por otra, motivaron acciones de defensa de las
víctimas
de la pandemia y de solidaridad con la causa de luchar contra el
contagio del virus. Finalmente, entra
de lleno a presentar el SIDA como problema público y describe el
proceso del desarrollo científico que,
a partir de la identificación del VIH, condujo a la producción de
antivirales, siempre con la mirada
puesta en la obtención de una vacunaPalabras clave: VIH; Síndrome de Inmunodeficiencia Adquirida; Historia; Brotes de Enfermedades; Enfermedades Transmisibles Emergentes; Pandemias.


1 MD, Gineco-Obstetra, Fellow en
Medicina Reproductiva, MSc en Epidemiología. Universidad del Rosario.
Bogotá, Colombia.
2 Abogado, MA Politics and Goverment,
MA Entreprises Publiques et Développement. Universidad del Rosario.
Bogotá, Colombia
HIV/AIDS, THE PANDEMIC OF THE TURN OF THE MILLENNIUM
Abstract
The emergence of HIV-AIDS in the scenery of contemporary diseases posed
unsuspected
challenges for science, and unleashed unprecedented phenomena within
popular culture and
the management of public policy. This article recounts the fight
against the pandemic from the
uncertain moments of the initial explorations to identify its origin,
to the discovery of antiviral
drugs that have managed to slow down the rate of its expansion. In
addition to reviewing the
figures of the impact of AIDS on certain populations, it presents the
sequence of beliefs and
social reactions that facilitated the rise of a culture of
discrimination against people affected
by the disease, as well as exploring how this phenomenon created a
movement of defense of
and solidarity with victims of the pandemic. Finally, it presents AIDS
as a public problem and
describes the scientific development process that, starting with the
identification of HIV, has
lead to the production of antivirals, always with the aim of developing
a vaccineKeywords: HIV; Acquired Immunodeficiency Syndrom; History; Disease outbreaks; Communicable Diseases; Emerging; Pandemics.
La irrupción del SIDA en el escenario mundial
Dada su semejanza con el virus de inmunodeficiencia de los simios (SIV), se cree que el agente causal del que ahora se conoce como Síndrome de Inmunodeficiencia Adquirida, SIDA, pasó de los chimpancés a los humanos por transmisión entre especies, alrededor de 1930. Los primeros casos de infección se rastrearon en África antes de la aparición de la epidemia en la zona central del mismo continente, y luego en América, en los años sesenta (1). La identificación de esa entidad patológica, caracterizada por un severo compromiso de la inmunidad, se remonta a junio de 1981, cuando el Centro de Control de Enfermedades de los Estados Unidos (CDC en inglés) publicó en su reporte semanal, MMWR, el primer informe relacionado con cinco casos de Pneumocystis carinii en hombres homosexuales, en Los Ángeles. Este hallazgo inusual de infecciones oportunistas en jóvenes previamente sanos, entre quienes se encontró evidencia paraclínica de infección previa o concurrente por Citomegalovirus (CMV), sugirió la posibilidad de una disfunción de la inmunidad celular relacionada con una exposición común, y alertó sobre el posible rol del CMV (2).Esa publicación, que alertó a la comunidad médica cuatro meses antes de la publicación del primer artículo científico revisado por pares, estaba relacionada con las reiteradas solicitudes de Isotionato de Pentamidina, fármaco utilizado para el manejo de la Neumonía por Pneumocistis Carini, que para ese entonces aún no había sido aprobado para venta en el mercado y cuyo suministro dependía del CDC. El aumento en la demanda de esta medicación, usada casi exclusivamente en pacientes con cáncer u otras condiciones asociadas a inmunosupresión severa, había disparado las alarmas (3).
Entre octubre y diciembre de ese año aparecieron publicados reportes casi simultáneos en Los Ángeles y Nueva York, de esta y otras enfermedades oportunistas en homosexuales (4-6). El CDC, entonces bajo el liderazgo del Dr. William Foege, conformó un equipo de vigilancia epidemiológica de Sarcoma de Kaposi y otras enfermedades oportunistas, y estableció la primera definición de caso para el seguimiento del brote. Esta definición incluía, confirmación histológica de Sarcoma de Kaposi en paciente menor de 60 años o confirmación patológica o por cultivo de infección oportunista fatal, o que amenazara la vida en pacientes sin enfermedades subyacentes o historia de terapia inmunosupresora (3).
Para finales de ese año, el Dr. David T. Durack, en su editorial del NEJM, afirmaba: “aunque esta asociación sea nueva y sorprendente, ya se han recopilado suficientes casos para establecer su realidad. En la actualidad, se están analizando más de 160 casos en el CDC, y se informan cinco o seis nuevos cada semana” (7).
En junio de 1982, el CDC reportó brotes de neumonía por Pneumocystis carinii y de Sarcoma de Kapossi, con comportamientos particularmente agresivos en homosexuales jóvenes, sin riesgo aparente para ese raro tipo de enfermedades. En la nota editorial, el CDC mencionaba la hipótesis de que la inmunodeficiencia celular adquirida, que parecía subyacer a estos casos, podría derivarse de la transmisión, a través del contacto sexual, de un agente infeccioso todavía no bien definido. Como hipótesis alternativa se consideraba que la causa de esta inmunodeficiencia podría estar relacionada con la exposición a otros agentes, como estimulantes sexuales inhalados (los llamados “poppers” de butil o amyl nitrato), agentes psicotrópicos, u otro tipo de “drogas callejeras” propios del estilo de vida de cierta población homosexual (8).
El nombre SIDA, Síndrome de Inmunodeficiencia adquirida (AIDS en inglés) vino a ser recomendado por el CDC en septiembre de 1982 (9). Aunque la enfermedad inicialmente se consideró ligada sólo a los homosexuales, pronto se describieron casos similares en Europa y Estados Unidos, relacionados con pacientes hemofílicos. También se identificaron casos entre migrantes haitianos, en su mayoría heterosexuales y sin factores de riesgo conocidos. Desde Europa se reportaban dos tipos de epidemia: una entre homosexuales y otra predominantemente en heterosexuales migrantes de África central. En diciembre de 1982 el CDC recibió el reporte de un caso de inmunodeficiencia celular e infección oportunista en un niño hemofílico, de 20 meses de edad, quien había recibido múltiples transfusiones, incluyendo la de un individuo diagnosticado posteriormente con SIDA. La similitud con las características de la enfermedad previamente identificada en homosexuales, usuarios de drogas y hemofílicos, orientó hacia una posible etiología infecciosa, que permitía ya vislumbrar la transmisión del agente causal a través de contacto sexual o de la exposición a sangre o sus derivados (10).
En su Discurso Nobel, el Dr. Luc Montaigner afirmó que el virus causante de la enfermedad fue por primera vez aislado a partir de la biopsia de una adenopatía cervical de un paciente en 1983, que identificó partículas virales semejantes a las de algunos retrolentivirus animales. El grupo del Instituto Pasteur, liderado por el Dr. Montaigner y la Dra. Françoise Barré-Sinoussi, presentó el hallazgo en la revista Science, en mayo de ese año, de manera casi coincidente con el artículo del doctor Robert Gallo, líder del equipo del Instituto Nacional de Salud de los Estados Unidos. El virus, denominado LAV y HTLV-III, por los dos grupos respectivamente, fue confirmado como el agente causal del SIDA en 1884 y renombrado como HIV (iniciales en inglés para virus de la inmunodeficiencia humana) por el Comité Internacional de Nomenclatura de Virus. En 1986 se aisló un segundo virus, HIV-2, de pacientes provenientes de África occidental, de transmisión heterosexual. Muy pronto fue también evidente que el virus no se transmitía por contactos casuales (11-13).
La epidemia del SIDA en cifras
Durante los primeros dos años de la epidemia, el número de pacientes identificados con SIDA creció paulatinamente. Para junio de 1981 se habían reportado al CDC 1.200 casos provenientes de 34 estados de los Estados Unidos, el Distrito de Columbia y 15 países más, con 450 muertes y una tasa de fatalidad por caso mayor del 60% en los pacientes diagnosticados durante el primer año (14).Las transfusiones de sangre o sus derivados, contaminados con el virus, fueron frecuentes entre 1981 y 1984. Se calcula que en los Estados Unidos cerca de 15.000 hemofílicos fueron infectados por esta vía. De igual forma, los consumidores de drogas intravenosas se exponían al compartir agujas. Solo hasta 1984 aparecieron los programas de reemplazo de agujas usadas por drogadictos, en Holanda y otros países europeos (9).
Para finales de 1987 se habían reportado en los Estados Unidos 50.000 casos de SIDA y cerca de 28.000 personas habían fallecido a causa de la enfermedad. Sin embargo, era evidente que el número de infectados era significativamente mayor, estimándose entre 1 y 1,5 millones de personas (15). Según ONUSIDA, Programa Conjunto de las Naciones Unidas sobre el VIH/SIDA, desde que comenzó la epidemia y hasta finales de 2018, cerca de 75 millones de personas en el mundo habían contraído la infección por VIH, y de ellas, cerca de 32 millones habían fallecido por enfermedades relacionadas (16).
Desde que se alcanzó el máximo pico de contagios, en 1997, las infecciones se han reducido en un 40%. Las nuevas infecciones disminuyeron de 2,9 millones en 1997 a 2,1 millones en 2010 y a 1,7 millones en 2018. Los grupos de población clave (hombres que tiene sexo con hombres, personas que se inyectan drogas intravenosas, trabajadores sexuales, personas transgénero) y sus parejas sexuales, representan más de la mitad de las nuevas infecciones por VIH a nivel mundial. La tasa anual de muertes igualmente ha descendido de 1,7 millones en el 2004, cuando presentó su máximo pico, a 770.000 en 2018 (17) (Figura 1).
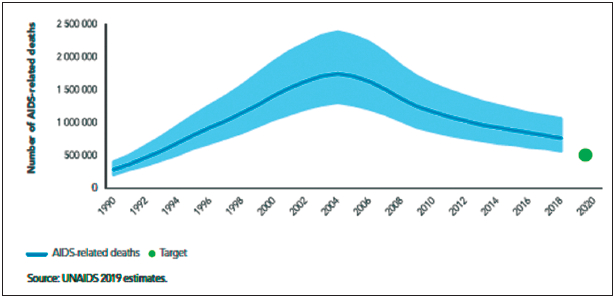
Figura 1. Muertes relacionadas con SIDA, Global 1990-2018 y Objetivo 2020
Las estadísticas más recientes señalan que actualmente alrededor de 38 millones de personas viven con VIH, más de la mitad de ellos en África oriental y del sur; cerca del 80% saben que están infectados y 62% tienen acceso a terapia antirretrovírica (aproximadamente 24,5 millones para mediados de 2019). En el subgrupo de mujeres embarazadas que viven con VIH, el 82% tuvo acceso a terapia para evitar la transmisión vertical del virus a sus hijos (16). La razón global de incidencia/prevalencia, que es un buen estimativo de la forma como ha progresado el control de la epidemia, ha declinado de 11,2% en el año 2000 a 6,6% en el 2010 y a 4,6% en el 2018 (Figura 2). Se estima que 18 países han alcanzado el punto de referencia de 3%, (3 infecciones de VIH por cada 100 personas viviendo con VIH por año) señalado por ONUSIDA como el punto de corte por debajo del cual la infección irá disminuyendo globalmente hasta dejar de ser una amenaza para la salud pública, lo que representa una promesa en el camino que conduzca al fin de la pandemia (17).
Desde el punto de vista social, la epidemia de SIDA se ha caracterizado por fuertes rasgos de discriminación, marginalización, tabús y estigmatización hacia la población infectada, así como por inequidades en el acceso a tratamiento, y manifestaciones diversas de desigualdad dentro del espectro del balance internacional del poder.
La infección ha afectado de manera extrema a regiones y grupos vulnerables. La mayor proporción de infectados se concentra en el continente africano, que presenta la mayor tasa de coinfección con enfermedades como la tuberculosis, a su vez principal causa de muerte en pacientes con VIH y donde existe la mayor limitación de acceso a terapias antirretrovirales. El mayor riesgo de infección lo tienen grupos marginales y segregados, la población LGTBI, las y los trabajadores sexuales, la población carcelaria y las personas sometidas a explotación sexual. También ha cobrado un importante número de víctimas entre los niños (cerca del 4,5% de la población vive con HIV) y las mujeres. Semanalmente se infectan en el mundo 6.000 mujeres entre 15 y 24 años, y en el África subsahariana las mujeres representan cuatro de cada cinco nuevas infecciones en adolescentes entre 15 y 19 años. En esa misma región, las jóvenes entre 15 y 24 años tienen el doble de riesgo de vivir con VIH que los varones (16).
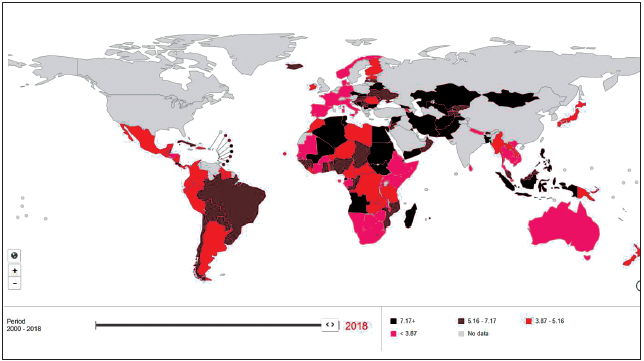
Figura 2. Métricas de transición de la epidemia. Razón Incidencia/Prevalencia, por países, 2018
Representaciones sociales del SIDA
Pocas enfermedades, como el SIDA, han generado tal cantidad de sentimientos más allá del círculo de quienes la padecen. Su irrupción, a finales del Siglo XX, no solamente afectó el entorno inmediato de los pacientes, sino que produjo notables impactos sociales, hasta cubrir un espectro de dimensiones insospechadas, mucho más que, en su momento, la tuberculosis y el cáncer.Tal vez el origen y las primeras interpretaciones respecto de la población que podía ser objeto de la enfermedad, acentuaron el señalamiento hacia las personas susceptibles de contraerla, como fue el caso de los homosexuales. En torno a ellos germinaron el terror, la idea de culpa, el señalamiento despectivo cargado de juicios morales, la discriminación social y la condena implacable (19).
La caracterización de “incurable” contribuyó a que en torno al SIDA aparecieran “construcciones culturales” de rechazo, basadas en la homofobia, su vínculo con la drogadicción, el espanto por el desaseo atribuible a ciertas personas, y el menosprecio por comunidades, como la afrodescendiente y en particular la haitiana. Fenómenos que se acrecentaron cuando se supo de la posible ampliación del espectro del contagio a todo el género humano (19).
Tal vez ninguna enfermedad ha sido objeto de tanta curiosidad y de tanta exploración, ordenada y desordenada, autorizada e improvisada, como el SIDA. Más allá de la juiciosa actividad científica, apareció la curiosidad -individual y social- por entender los riesgos propios de la circulación del virus y las formas de evitar la infección, que degeneró en prevenciones en cuanto al contacto con personas infectadas, y en el surgimiento de interpretaciones populares de toda índole.
La circulación de teorías hechizas e interpretaciones acomodaticias llegó a tener tanta fuerza, que por un tiempo consiguió eclipsar, en el ambiente social, la difusión de los resultados propios de la investigación científica. De manera que circularon, sin mayor contrapeso, explicaciones llenas de prejuicios, postulados seudocientíficos y fantasías fáciles de digerir y absorber, a las que muchos se sintieron con derecho de agregar su “cuota de enriquecimiento”.
La relación entre homofobia y enfermedad, fue tal vez el aspecto más sobresaliente de todas estas interpretaciones animadas por el terror que produce la presencia de un contagio epidémico de características originalmente inexplicables. A ello se sumaron teorías conspirativas, presentes en casos de pandemia, que atribuían a una u otra nación la autoría de la creación del virus y su dispersión perversa con aparentes motivaciones científicas, vengativas, propagandísticas, experimentales o políticas (20).
Los correspondientes comportamientos sociales no se hicieron esperar. Muchos se negaban a recibir transfusiones de sangre, otros evitaban la cercanía de personas infectadas. Niños con SIDA fueron expulsados de los colegios, y empleados despedidos de sus trabajos. Se dijo que ciertos drogadictos preferían contraer la infección para mantener la costumbre de compartir agujas; que las prostitutas eran reservorios de la enfermedad; que la transmisión heterosexual solo se podía dar en la dirección de hombre a mujer, y que en África la misma transmisión se presentaba porque la penetración anal era un método anticonceptivo (20).
El esclarecimiento de todas estas interpretaciones terminó implicando a activistas de la comunidad gay y grupos afines, en busca de argumentos para contrarrestar la avalancha de prejuicios y equivocaciones que tanto daño les hacía. Por ese camino consiguieron no solo reducir la presión social en su contra, sino ganar espacios de respeto por su condición y vocería de sus intereses en el seno de la sociedad.
Dentro del panorama de acciones orientadas a esclarecer la naturaleza y el impacto del SIDA, ocupa un lugar especial, por su valor simbólico, el esfuerzo realizado a través de la exposición ‘Against Aids: Posters from Around the World’, que se llevó a cabo en el Museum für Kunst und Gewerbe de Hamburg entre febrero y abril de 2006. De una colección original de más de mil posters relacionados con HIV-SIDA y sexo seguro, se presentó una selección que demostró el poderío social de las expresiones visuales y sintéticas para interpretar fenómenos históricos, científicos o culturales, con todo lo que un poster puede reunir a través de colores, formas y mensajes escritos, para transmitir lo esencial del objeto de su contenido (21).
La apelación a muchos otros medios de difusión permitió apreciar la presencia global del fenómeno y la riqueza de expresiones de solidaridad con sus víctimas. Ejercicio valioso, en cuanto fortaleció la perspectiva de acciones universales frente a amenazas que no respetan distinciones de raza, credo, nacionalidad, y mucho menos fronteras estatales.
El SIDA como problema público
Como fenómeno de salud pública, la lucha contra el SIDA planteó exigencias de responsabilidad y liderazgo a los Estados y los organismos internacionales. El contagio entró a ocupar renglón importante dentro de la lista de preocupaciones que requieren respuestas a través de políticas públicas y cooperación internacional, tanto en la prevención como en el tratamiento y la previsión de eventualidades futuras. Por eso figura en la agenda, junto a nuevas dimensiones de los Derechos Humanos, la inclusión de comunidades de preferencias sexuales diversas, y la marginalidad vinculada al nivel de desarrollo económico y social, o determinada condición étnica.Gobiernos, comunidades académicas y científicas, medios, analistas sociales, semiólogos, activistas de la sociedad civil, y artistas, entre otros, han tenido que comprender y explicar el contagio, los peligros que conlleva, la manera de evitarlo, y sus consecuencias individuales y sociales, sobre la base de que, sin perjuicio del compromiso de erradicarlo, por ahora hay que aceptar su presencia en el seno de la sociedad.
Esta aceptación, que no equivale a resignarse frente a su amenaza, se ha convertido en aliciente para el avance de la ciencia y de la práctica médica, al tiempo que permite advertir dimensiones renovadas de comportamiento social más favorables a las poblaciones originalmente discriminadas y malentendidas, más llenas de esperanza de vida para los pacientes y los miembros de su entorno, y más favorables a la lucha contra la expansión del virus en la vida cotidiana.
Comprensión de la epidemia el SIDA y medidas de salud pública
Como suele suceder con la aparición de las plagas, la interpretación que la sociedad da al fenómeno, equivocada o cierta, marca los comportamientos colectivos. Como ya se dijo, en el imaginario popular, lo que inicialmente fue percibido como una infección exclusiva de homosexuales, tratada por los medios como “the gay plague”, pronto se convirtió en una amenaza real que podría afectar a heterosexuales y otros grupos poblacionales, incluyendo los niños.Los avances que se fueron dando en el entendimiento de la enfermedad, produjeron cambios en el comportamiento social y marcaron el rumbo de las recomendaciones que empezaron a surgir por parte de las entidades responsables de la salud pública y de los tomadores de decisiones. Basándose en los datos epidemiológicos, y aún antes de tener una idea clara del agente causal, el Instituto Nacional de Salud de los Estados Unidos, (NIH), en conjunto con la FDA y el CDC, emitieron recomendaciones para la prevención de la infección, incluyendo precauciones para el manejo de transfusiones sanguíneas e indicaciones para evitar el contacto sexual con pacientes diagnosticados o con sospecha de tener SIDA (3).
A medida que la hipótesis de un agente infeccioso se hacía evidente, el CDC emitió recomendaciones para médicos, odontólogos, personal de salud y personal de laboratorio que manipulara secreciones o sangre provenientes de pacientes con sospecha o diagnóstico de SIDA. Partiendo de la observación de que los pacientes con SIDA seguían un patrón de distribución de la enfermedad similar al de los pacientes con Hepatitis B, las recomendaciones eran básicamente las mismas que se tenían para manejar dichos pacientes: se debían evitar accidentes ocupacionales, usar material de protección para el manejo de sangre o secreciones, atender recomendaciones sobre la forma de desechar agujas y material contaminado, y además, la prohibición expresa para pacientes diagnosticados o sospechosos, de donar sangre u órganos (22).
Desde etapas tempranas, los hallazgos epidemiológicos sugerían que las personas con riesgo de transmitir el SIDA serían difíciles de identificar. Se había advertido ya la existencia de alteraciones en la inmunidad celular en pacientes completamente asintomáticos y sin hallazgos clínicos reveladores. Parecía existir un “periodo de latencia” desde meses y hasta 2 años entre la exposición y la aparición de síntomas, lo que implicaba que la transmisibilidad podría preceder al reconocimiento de hallazgos clínicos. Se hacía entonces, cada vez más necesaria, una prueba de laboratorio que pudiera identificar a aquellos con la enfermedad o en riesgo de desarrollarla. Entretanto, se recomendaba evitar el contacto sexual con personas diagnosticadas o en riesgo, y se enfatizaban las precauciones dirigidas a bancos de sangre (23).
La identificación del Virus de la Inmunodeficiencia Adquirida por los grupos de los doctores Montaigner y Gallo, y el conocimiento de sus características biológicas, permitió avanzar rápidamente en el desarrollo de las pruebas para tamizaje de la población de riesgo y para evaluación de derivados sanguíneos en bancos de sangre. Para 1984 se habían descrito tres técnicas serológicas para la detección de anticuerpos contra el virus: una prueba de inmuno-absorción ligada a enzimas (ELISA) para el virus completo; un ensayo de radioinmunoprecipitación, que identificaba la proteína viral p25; y un ensayo de anticuerpos contra antígenos virales principales, mediante la técnica de Western Blot. La realización de estas pruebas, en grupos de alto riesgo, permitió identificar evidencia serológica de exposición al virus y mostró, indiscutiblemente, que la infección era más frecuente de lo que se pensaba y que la enfermedad podía tener un espectro variado de manifestaciones y severidad, con periodos de latencia prolongados. Las implicaciones individuales, en caso de que la prueba resultara positiva, todavía no eran claras; no era posible establecer, con los resultados serológicos aislados, la presencia de infección activa o de inmunidad. Tampoco era claro el tiempo necesario para sero-convertirse después de la exposición viral (24).
Las guías de 1987 del CDC para la consejería y realización de pruebas, señalaban una alta sensibilidad (99%) de la prueba comercialmente disponible de ELISA (EIA), haciendo que la posibilidad de un falso negativo fuese remota, excepto en aquellos casos en que la prueba se realizara en las primeras semanas posteriores a la exposición. A pesar de tener también una muy alta especificidad (99%), se recomendaba que un test positivo fuera seguido de una confirmación con pruebas de ELISA subsecuentes, o con un Western blot. Dado lo sensible de la información, se incluían recomendaciones para el manejo confidencial de la misma, el reporte de los resultados y el mantenimiento de altos estándares de control de calidad. Igualmente, las guías mencionaban por primera vez la necesidad de rastreo y notificación de contactos de los casos confirmados. Sabiendo ya que era crucial mantener la confianza del público, con el propósito de incrementar el número de pacientes diagnosticados, se volvió indispensable asegurar todas las medidas necesarias para mantener la privacidad de los resultados y evitar que los casos confirmados fueran objeto de discriminación en el trabajo, los espacios educativos, la vivienda y la provisión de servicios de salud (25). El desarrollo de técnicas de biología molecular permitió la introducción de nuevas pruebas diagnósticas, y modificó los algoritmos para identificar con precisión a las personas infectadas con VIH. Además del diagnóstico serológico con metodologías de cuarta y quinta generación, la detección del genoma VIH, la viremia plasmática, las pruebas de resistencia y las pruebas rápidas, entre otras, han venido a completar el armamentario diagnóstico (26).
El mejor conocimiento de la historia natural de la enfermedad y de los mecanismos de transmisión, facilitó recomendaciones adicionales sobre medidas para prevenir la propagación de la infección. Pronto se hizo evidente que, además del contacto sexual, la transmisión parenteral por sangre o sus derivados, o el compartir agujas infectadas, era posible la transmisión vertical del virus de madres a hijos durante el embarazo y el parto. Buscando disminuir este riesgo, se extendió la recomendación de hacer consejería y pruebas de tamizaje a mujeres embarazadas pertenecientes a los grupos de riesgo (27). Esta recomendación se volvió universal para todas las mujeres embarazadas en 1995, poco después de que el estudio PACTG 076 demostrara que el uso de terapia antirretroviral, desde el segundo trimestre del embarazo y en los recién nacidos hasta por 6 semanas, podía disminuir drásticamente la infección de los productos de madres infectadas. Actualmente, la prueba de tamizaje es práctica habitual del control prenatal (28). El advenimiento de terapia antirretroviral combinada durante el embarazo, las recomendaciones de cesárea electiva para mujeres infectadas, la realización de pruebas rápidas intraparto en mujeres no previamente tamizadas durante el embarazo y la recomendación de no lactar para mujeres infectadas, han reducido -aún más- el riesgo de transmisión madre-hijo (29).
Los médicos y trabajadores de la salud han sido siempre una población particularmente expuesta al riesgo de transmisión en casos de pandemias. En el caso del SIDA, las recomendaciones iniciales se relacionaron con las llamadas “precauciones universales”. A medida que avanzó el conocimiento de la enfermedad, se enfatizaron otras medidas de precaución, especialmente en caso de procedimientos invasivos o con alto riesgo de contacto con fluidos corporales. Las recomendaciones de manejo frente a una exposición fueron evolucionando con el tiempo. Inicialmente, el manejo de dichos accidentes implicaba la información al paciente y la realización inmediata de pruebas serológicas. Si el paciente resultaba positivo, se recomendaba la realización de pruebas para el trabajador de la salud y seguimiento clínico y serológico. Después del advenimiento de la terapia antirretroviral, estas recomendaciones incluyeron el uso de terapia profiláctica después del accidente ocupacional (30).
A lo largo de la historia de esta pandemia, se ha discutido también el riesgo de que un médico, odontólogo u otro trabajador de la salud infectado por SIDA, pueda transmitir la infección a su paciente. A partir de la experiencia con la Hepatitis B, se ha considerado que ciertos procedimientos invasivos quirúrgicos y dentales pueden tener una mayor propensión a exposición. Los ejemplos varían de una especialidad a otra. A pesar de que el riesgo eventual de transmisión del HIV en estas circunstancias es significativamente menor que el de la Hepatitis B, para minimizarlo se ha recomendado una estricta adherencia a los principios de las precauciones universales, a las recomendaciones de esterilización/desinfección, y a los principios de prevención y control de infecciones. El personal de salud involucrado en procedimientos invasivos o que tengan una particular propensión a exposición, tiene el deber ético de conocer su estado serológico y hacerse pruebas periódicas. A pesar de que al comienzo de la epidemia se recomendó a los trabajadores de salud seropositivos abstenerse de realizar procedimientos invasivos o con mayor propensión a exposición, actualmente se considera que, con consejería y tratamiento médico experto, una estricta adherencia a terapia antirretroviral efectiva y una carga viral indetectable, no deberían tener restricciones en la actividad profesional. En cualquier caso, se deben manejar políticas transparentes, que preserven la seguridad del paciente y que garanticen también el derecho del trabajador de la salud al manejo confidencial de su información médica personal (32,33).
En cuanto se hizo evidente que la posibilidad de infección, en todos los casos, se relacionaba con comportamientos modificables, se hizo cada vez más relevante el factor educativo orientado a modificar las conductas riesgosas. Para las autoridades de salud, era claro que, en ausencia de una vacuna o de un tratamiento antiviral seguro y efectivo, la educación era el camino más efectivo disponible para el control de la epidemia. Teniendo en cuenta que el HIV es un virus principalmente de transmisión sexual, las medidas educativas dirigidas a niños y adolescentes no dejaron de ser objeto de acaloradas discusiones y reacciones en diferentes estamentos de la sociedad. Los programas promovidos desde los gobiernos, buscaron incluir en los procesos de toma de decisión a todas las instancias representativas del sector educativo, así como a líderes religiosos, grupos minoritarios, médicos y asociaciones médicas, para minimizar el impacto, legitimar las recomendaciones y garantizar el compromiso en la implementación y mantenimiento de los programas. Se buscaba en particular evitar el uso de drogas intravenosas y postergar el inicio de la vida sexual. Para los que ya tenían relaciones sexuales, se enfatizaba la importancia de la monogamia, el uso de condón y la asesoría especializada (34).
El éxito de los antivirales
La identificación del virus causante del SIDA, y el conocimiento de sus características moleculares y biológicas, facilitaron la búsqueda de tratamientos efectivos. Esta carrera ha presentado éxitos significativos en el control de la enfermedad, pero no ha estado exenta de retos y dificultades, particularmente relacionados con toxicidad, resistencia viral, adherencia al tratamiento, costos y limitaciones en el acceso a las terapias. Hasta la fecha, más de 30 medicamentos antirretrovirales han sido aprobados por la FDA para el tratamiento de la enfermedad (35).En 1987 se inició el uso de drogas antirretrovirales. La primera de ellas, el AZT (acidotimidina), eficiente inhibidor de la transcriptasa reversa del HIV. Infortunadamente, dada la alta tasa de mutación del virus, muy pronto aparecieron cepas resistentes que hicieron necesaria la utilización de combinaciones de antirretrovirales (11).
En 1996 se introdujo la terapia antirretroviral combinada (con un inhibidor de la proteasa como pieza central del tratamiento), conocida como HAART (en inglés highly active antiretroviral therapy), que gracias a su efectividad, fue posible que el SIDA pasara de enfermedad letal a enfermedad crónica. Se calcula que su uso ha salvado cerca de 7,8 millones de vidas en el mundo entre los años 2000 y 2014. Sin embargo, esta terapia no está exenta de toxicidad y efectos secundarios frecuentes, que incluyen complicaciones cardiovasculares, hematológicas, endocrinas, y necrosis grasa. A pesar de esos posibles efectos secundarios, la evidencia actual permite recomendar su uso de manera temprana y continua, independientemente de los conteos de células T CD4+, así como la profilaxis preexposición (PrEP) para prevenir infección en pacientes HIV negativos con alto riesgo de infección o ante la evidencia de un contacto con una persona infectada (36).
A pesar del tratamiento exitoso con antirretrovirales combinados de alta eficacia, con disminución significativa del reservorio viral, el HIV exhibe mecanismos de persistencia. Se sabe que el virus puede permanecer latente y silencioso, integrándose al DNA de las células hospederas, infectando células T CD4+ de memoria inmunológica de larga vida o permaneciendo dentro de los ganglios linfáticos que actúan como un “santuario inmune”, manteniendo al virus insensible a las drogas y fuera del alcance del sistema inmune. Todo esto hace que una terapia curativa con los tratamientos actualmente disponibles no sea posible (37).
El hecho de que personas de origen europeo con una mutación homocigota para CCR5, correceptor de citoquinas necesario para la entrada del virus a la célula blanco y presente en el 1% de individuos, tengan una resistencia natural a la infección, así como el reporte de dos casos de eliminación completa del virus en pacientes viviendo con HIV que recibieron trasplante de células progenitoras hematopoyéticas provenientes de pacientes homocigotos para esta mutación, conocidos como paciente de Berlín y paciente de Londres, abrieron nuevas fronteras en el desarrollo de una terapia que pueda ser curativa (37).
La meta de lograr el fin de la pandemia es teóricamente alcanzable. La frase “fin del VIH / SIDA” no se refiere a la erradicación completa del virus, sino a la desaparición de la enfermedad como un problema de salud pública. Para esto, se requiere que el número de infecciones nuevas sea menor al de muertes; que la prevalencia sea <1 caso de SIDA / 1.000 habitantes; que el 73% de las personas que viven con VIH reciban tratamiento; que el 86% de ellos experimenten supresión viral y que la transmisión de madre a hijo sea <5%. Para hacerlo posible se requerirá del esfuerzo mancomunado y continuo de gobiernos, sector privado, ONGs, industria, sociedad civil y pacientes (38).
La lucha por una vacuna
El desarrollo de una vacuna segura y efectiva ha sido uno de los grandes retos en la historia de esta pandemia. En 1984, poco después de la identificación del virus, Margaret Heckler, entonces Secretaria de Salud de los Estados Unidos, declaró que una vacuna estaría disponible dentro de los siguientes dos años. Desde entonces, han trascurrido más de 35 de investigación y se han probado más de cien candidatos (9).La secuencia completa del genoma viral del HIV fue publicada en 2009. Un virus RNA de 9Kb, con 9 genes que codifican 15 proteínas (39). Ésta caracterización fue un importante primer paso, pero la lógica de las vacunas clásicas, que imitan la inmunidad natural que ocurre en individuos recuperados de la infección, no es aplicable en este caso, pues los infectados por HIV no se recuperan espontáneamente como parte de la historia natural de la enfermedad. Diversas características confieren al virus una particular complejidad:
- Su blanco son los linfocitos T CD4, células que orquestan la respuesta inmune a los virus. Al infectarlos o destruirlos se facilita la diseminación y la persistencia viral.
- El ciclo de vida del virus favorece el rápido establecimiento de una infección crónica, difícil de eliminar.
- Se han identificado diferentes subtipos de VIH; se sabe que el subtipo B es común en Norteamérica y Europa, mientras el C predomina en el sur y en el este de África. Entonces una vacuna que protege contra un subtipo puede no brindar protección contra otros.
- El VIH muta a gran velocidad y los cambios frecuentes hacen que el virus sea blanco difícil para una vacuna. Algunos factores que pueden explicar esta alta tasa de mutación son la alta frecuencia de errores en el proceso de transcripción reversa, la recombinación genética de virus diferentes que infectan una misma célula y el estrés oxidativo.
- Finalmente, la gran diversidad de la glicoproteína de la envoltura viral dificulta la generación de anticuerpos ampliamente neutralizantes.
Además de las dificultades técnicas para el desarrollo de vacunas, ha sido necesario sortear el obstáculo de la utilización de modelos animales (primates no humanos) usados para investigar la eficacia de las vacunas, que resultan particularmente costosos y no garantizan necesariamente que los fármacos funcionen en humanos(40,41). Los hitos más importantes en la búsqueda de una vacuna han provenido de los ensayos clínicos de eficacia. En la Figura 3 se resumen los estudios más importantes hasta la fecha.
Algunos de estos fueron suspendidos por razones relacionadas con seguridad. Otros fallaron en demostrar eficacia. El único estudio que ha demostrado una respuesta protectora fue el RV144, ensayo de base comunitaria en Tailandia, que probó la eficacia y seguridad de un esquema con dos vacunas experimentales. La primera fue una vacuna recombinante que usaba un virus de la viruela del canario, con genes insertados que codifican proteínas antigénicas del VIH (ALVAC), seguida de un refuerzo de ALVAC + Vacuna compuesta por la proteína de superficie gp120 genéticamente modificada. Este estudio mostró una tasa de protección inicial del 60%, que desafortunadamente cayó a 31% después de 6 meses (42).
De acuerdo con lo señalado por Bekker en el artículo publicado en Lancet de 2019, nos encontramos en una etapa muy activa de investigación, con fases avanzadas de ensayos clínicos de 3 candidatos a vacuna:
- HVTN 702 ensayo de fase 2b / 3 que evalúa la seguridad y eficacia de la vacuna ALVAC + Una vacuna bivalente del subtipo C (variantes apropiadas para la cohorte Sur Africana) de la proteína gp120, con un refuerzo adicional para mantener la respuesta de anticuerpos protectores;
- HVTN 705, ensayo de fase 2b que prueba una vacuna principal fabricada a partir de cuatro secuencias mosaico Ad26-mosaico + Vacuna del subtipo C de la proteína gp140
- PrEPVacc, estudio de fase 2b que evaluará la combinación de una vacuna contra el VIH (ADN, virus de Ankara vaccinia modificado, y proteína Env más adyuvante) + profilaxis previa a la exposición.
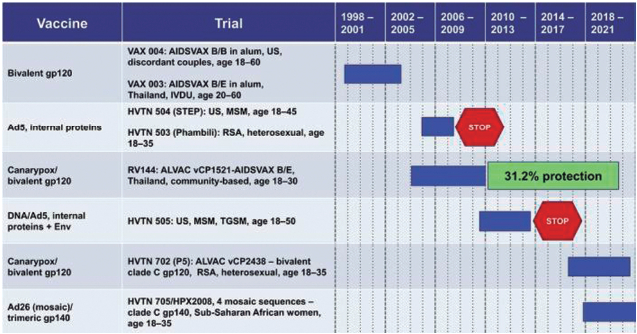
Figura 3. Ensayos clínicos de eficacia de Vacunas para VIH
También han despertado interés los llamados “controladores de élite”, personas con infección por VIH que mantienen cargas virales reducidas, sin estar en tratamiento antirretroviral y que no desarrollan SIDA, así como personas, que a pesar de repetidas exposiciones al virus, no se han infectado, con la esperanza de que puedan dar luces en el desarrollo de vacunas efectivas.
Los proyectos de investigación y desarrollo de vacunas contra el VIH han contado con el apoyo y financiación de organismos multilaterales públicos y privados, así como de redes colaborativas de investigación y grupos filantrópicos. Como señala Eisinger, el desarrollo de una vacuna moderadamente efectiva que pueda sumarse a la óptima implementación de los tratamientos y las medidas de prevención existentes, parece ser una pieza clave para el control de la pandemia (38).
Hacia un futuro menos incierto
El SIDA es hasta ahora la pandemia más larga de la historia contemporánea, la más costosa en todo sentido y también la que ha generado más reacciones y ha involucrado más agentes sociales. Desde el punto de vista de la investigación, ha representado una oportunidad única para profundizar en el conocimiento científico y ha permitido descubrimientos innovadores en áreas fundamentales de la biología celular y molecular. La prolífica producción científica da cuenta de esto (44).Ha servido además para demostrar que, si no existe cooperación internacional, colaboración interdisciplinaria e involucramiento de diferentes actores, no se conseguirán resultados frente a retos universales en materia de salud pública. De las acciones de diferente índole desarrolladas, la ciencia, la sociedad y los gobiernos pueden extraer lecciones útiles para el futuro.
Referencias
1. Vangroenweghe, D. The Earliest
Cases of Human Immunodeficiency Virus Type 1 Group M in Congo-Kinshasa,
Rwanda and Burundi and the Origin of Acquired Immune Deficiency
Syndrome. Philosophical Transactions:
Biological Sciences. 2001; 356(1410): 923-925.
2. CDC. Pneumocystis pneumonia—Los
Ángeles. MMWR.
1981; 30: 1–3.
3. Curran JW, Jaffe HW; Centers for
Disease Control and
Prevention (CDC). AIDS: the early years and CDC’s response. MMWR Suppl.
2011; 60(4): 64-69.
4. Gottlieb MS, Schroff R, Schanker
HM, et al. Pneumocystis carinii pneumonia and mucosal candidiasis in
previously healthy homosexual men: evidence of a
new acquired cellular immunodeficiency. N Engl J Med.
1981; 305(24): 1425-1431
5. Friedman-Kien AE. Disseminated
Kaposi’s sarcoma
syndrome in young homosexual men. J Am Acad Dermatol. 1981; 5(4):
468-471.
6. Hymes KB, Cheung T, Greene JB, et
al. Kaposi’s sarcoma in homosexual men-a report of eight cases. Lancet.
1981; 2(8247): 598-600.
7. Durack DT. Opportunistic
infections and Kaposi’s sarcoma in homosexual men. N Engl J Med. 1981;
305(24):
1465-1467.
8. CDC. A Cluster of Kaposi’s Sarcoma
and Pneumocystis
carinii Pneumonia among Homosexual Male Residents
of Los Angeles and range Counties, California MMWR.
1982; 31(23): 305-7.
9. Greene WC. A history of AIDS:
looking back to see
ahead [published correction appears in Eur J Immunol.
2008 Jan; 38(1): 309]. Eur J Immunol. 2007; 37 Suppl
1: S94-S102.
10. CDC. Epidemiologic Notes and
Reports Possible Transfusion-Associated Acquired Immune Deficiency
Syndrome (AIDS) – California. MMWR. 1982; 31(48): 652-4.
11. Montagnier L. 25 years after HIV
discovery: prospects
for cure and vaccine. Virology. 2010; 397(2): 248-254.
12. Barré-Sinoussi F, Chermann JC,
Rey F, et al. Isolation
of a T-lymphotropic retrovirus from a patient at risk for
acquired immune deficiency syndrome (AIDS). Science.
1983; 220(4599): 868-871.
13. Gallo RC, Salahuddin SZ, Popovic
M, et al. Frequent
detection and isolation of cytopathic retroviruses (HTLVIII) from
patients with AIDS and at risk for AIDS. Science.
1984; 224(4648): 500-503.
14. CDC. Current Trends Prevention of
Acquired Immune
Deficiency Syndrome (AIDS): Report of Inter-Agency
Recommendations MMWR. 1983; 32(8): 101-3.
15. CDC. AIDS and Human
Immunodeficiency Virus Infection in the United States: 1988 Update.
MMWR. 1989;
38(S-4): 1-14.
16. ONUSIDA [Internet]. Hoja
Informativa- Últimas estadísticas sobre el estado de la epidemia de
SIDA, Día Mundial del Sida 2019. [Acceso: 8 de mayo de 2020].
Disponible en https://www.unaids.org/es/resources/fact-sheet
17. UNAIDS [Internet]. Data 2019.
[Acceso: 8 de mayo de
2020]. Disponible en https://www.unaids.org/en/resources/documents/2019/2019-UNAIDS-data
18. World Health Organization (WHO)
[Internet]. HIV testing and care continuum (2018). [Acceso: 8 de mayo
de
2020]. Disponible en https://www.who.int/hiv/data/2018_hiv-continuum-care.png.
19. Farmer K. AIDS as human suffering
Daedalus Living
with AIDS. 1989; 118(2): (Spring) 135-160.
20. Treichler PA. AIDS, homophobia
and biomedical discourse: An epidemic of signification. Cultural
Studies
1987; 1(3): 263-305.
21. Stein C, Cooter R. Visual Objects
and Universal Meanings: AIDS Posters and the Politics of Globalisation
and
History. Medical History. 2011; 55: 85-108.
22. CDC. Current Trends Acquired
Immune Deficiency Syndrome (AIDS): Precautions for Clinical and
Laboratory
Staffs MMWR. 1982; 31(43): 577-80.
23. CDC. Current Trends Prevention of
Acquired Immune
Deficiency Syndrome (AIDS): Report of Inter-Agency
Recommendations MMWR. 1983; 32(8): 101-3.
24. CDC. Antibodies to a Retrovirus
Etiologically Associated
with Acquired Immunodeficiency Syndrome (AIDS) in
Populations with Increased Incidences of the Syndrome.
MMWR. 1984; 33(27): 377-9.
25. CDC. Perspectives in Disease
Prevention and Health
Promotion Public Health Service Guidelines for Counseling and Antibody
Testing to Prevent HIV Infection and
AIDS. MMWR. 1987; 36(31): 509-515.
26. Parekh BS, Ou CY, Fonjungo PN, et
al. Diagnosis of
Human Immunodeficiency Virus Infection. Clin Microbiol
Rev. 2018; 32(1): e00064-18. Published 2018 Nov 28.
27. Current Trends Recommendations
for Assisting in
the Prevention of Perinatal Transmission of Human TLymphotropic Virus
Type III/Lymphadenopathy-Associated Virus and Acquired Immunodeficiency
Syndrome
MMWR. 1985, December 6; 34(48): 721-6,731-2.
28. Connor EM, Sperling RS, Gelber R,
et al. Reduction of
maternal-infant transmission of human immunodeficiency virus type 1
with zidovudine treatment. Pediatric AIDS
Clinical Trials Group Protocol 076 Study Group. N Engl
J Med. 1994; 331(18): 1173-1180.
29. Fowler MG, Lampe MA, Jamieson DJ,
Kourtis AP, Rogers MF. Reducing the risk of mother-to-child human
immunodeficiency virus transmission: past successes,
current progress and challenges, and future directions.
Am J Obstet Gynecol. 2007; 197(3 Suppl): S3-S9.
30. CDC. Recommendations for
prevention of HIV transmission in health-care settings. MMWR Suppl.
1987; 36(2):
1S-18S.
31. U.S. Public Health Service.
Updated U.S. Public Health
Service Guidelines for the Management of Occupational
Exposures to HBV, HCV, and HIV and Recommendations for Postexposure
Prophylaxis. MMWR Recomm
Rep. 2001; 50(RR-11): 1-52.
32. CDC. Recommendations for
Preventing Transmission of
Human Immunodeficiency Virus and Hepatitis B Virus
to Patients during Exposure-Prone Invasive Procedures
MMWR. 1991; 40(RR08): 1-9.
33. Ogunremi T, Defalco K, Johnston
BL, et al. Preventing
transmission of bloodborne viruses from infected healthcare workers to
patients: Summary of a new Canadian
Guideline. Can Commun Dis Rep. 2019; 45(12): 317-
322.
34. CDC. Guidelines for Effective
School Health Education
to Prevent the Spread of AIDS MMWR. 1988; 37(S-2): 1.
35. Eisinger RW, Fauci AS. Ending the
HIV/AIDS Pandemic
Emerg Infect Dis. 2018 Mar; 24(3): 413–416.
36. Fauci AS, Marston HD. Ending the
HIV-AIDS Pandemic-
-Follow the Science. N Engl J Med. 2015; 373(23): 2197-
2199.
37. Li J. Advances toward a cure for
HIV: getting beyond
n=2. Top Antivir Med. 2020; 27(4): 91-95.
38. Eisinger RW, Fauci AS. Ending the
HIV/AIDS Pandemic1. Emerg Infect Dis. 2018; 24(3): 413-416.
Doi:10.3201/eid2403.171797
39. Watts JM, Dang KK, Gorelick RJ,
et al. Architecture and
secondary structure of an entire HIV-1 RNA genome.
Nature. 2009; 460(7256): 711-716.
40. Robinson HL. HIV/AIDS Vaccines:
2018. Clin Pharmacol
Ther. 2018; 104(6): 1062-1073. Doi:10.1002/cpt.1208
41. Trovato M, D’Apice L, Prisco A,
De Berardinis P. HIV Vaccination: A Roadmap among Advancements and
Concerns. Int J Mol Sci. 2018; 19(4): 1241.
42. Rerks-Ngarm S, Pitisuttithum P,
Nitayaphan S, et al.
Vaccination with ALVAC and AIDSVAX to prevent HIV1 infection in
Thailand. N Engl J Med. 2009; 361(23):
2209-2220.
43. Bekker LG, Tatoud R, Dabis F, et
al. The complex challenges of HIV vaccine development require renewed
and expanded global commitment. Lancet. 2020;
395(10221): 384-388.
44. Fajardo-Ortiz D, López-Cervantes
M, Durán L, et al. The
emergence and evolution of the research fronts in HIV/
AIDS research. PLoS One. 2017; 12(5): e0178293.
Recibido: : 5 de Junio de
2020
Aceptado: 20 de Junio de 2020
Correspondencia:
Ángela María Ruiz Sternberg
angela.ruiz@urosario.edu.co
Aceptado: 20 de Junio de 2020
Correspondencia:
Ángela María Ruiz Sternberg
angela.ruiz@urosario.edu.co