USO CONTROLADO DE ANTIBIÓTICOS AYUDA EN LA DISMINUCIÓN DE LA RESISTENCIA BACTERIANA EN UNA INSTITUCIÓN DE CUARTO NIVEL DE COMPLEJIDAD (2004-2012)
Rubén Darío Camargo R.1, Gisela Olivares2, Nidia Fonseca3, Iván Zuloaga3. Ella Guardo4, Adriana Marín5
RESUMEN
El uso excesivo o indiscriminado de antibióticos va de la mano con la aparición de resistencia bacte- riana. Objetivo: Confirmar si el control de la prescripción diaria de antibióticos contribuye a disminuir la resistencia bacteriana. Métodos: Estudio descriptivo, trasversal, del control de la prescripción diaria de antibióticos. Durante los años 2004 a 2007 (primer periodo) y 2008 a 2011 (segundo perio- do). Diariamente se evaluó la prescripción de antibióticos de control institucional y se compararon semestralmente cada año sus resultados, con el reporte de resistencia en bacterias bajo vigilancia epidemiológica. Resultados: Los resultados obtenidos con el control diario de las prescripciones de antibióticos durante el estudio evidencian que controlar antibióticos ayuda a disminuir la resistencia bacteriana, en el periodo 2004-2007. La falta de adherencia a las políticas institucionales de control de las prescripciones de antibióticos, evidenció en el estudio aumento de la resistencia bacteriana, en el periodo 2008-2010. Comentario: Controlar institucionalmente antibióticos contribuye a disminuir la resistencia bacteriana o aumentarla sino se controlan.
Palabras clave: Control de antibióticos, resistencia bacteriana, prescripción antibiótica
1 MD. Internista-Intensivista. Director Científico de la UCI, Clínica General del Norte, Barranquilla.
2 Jefe de Vigilancia Epidemiológica, Clínica General del Norte, Barranquilla.
3 MD. Esp Infectología Adultos, Clínica General del Norte, Barranquilla.
4 MD, Esp Infectología Pediátrica, Clínica General del Norte, Barranquilla.
5 BSc. Microbiología, Clínica General del Norte, Barranquilla.
CONTROLLED USE OF ANTIBIOTICS HELPS IN REDUCING ANTIMICROBIAL RESISTANCE IN AN INSTITUTION OF FOUR LEVEL OF COMPLEXITY (2004-2012)
Objective: Excessive or indiscriminate use of antibiotics goes hand in hand with the emergence of bacterial resistance. This study aims at checking whether the daily control of antibiotic prescription helps in reducing bacterial resistance. Methods: This is a descriptive, crossed study. During years
2004 to 2007 (first period) and 2008-2011 (second period), daily antibiotic prescribing institutional control was evaluated; yearly comparison of bi-annual semester results with the report of resistance to bacteriae under epidemiologic surveillance was done. Results: The results obtained with daily monitoring of antibiotic prescriptions during the study showed that antibiotics control helped to reduce bacterial resistance (period 2004-2007). Lack of adherence to institutional policies for the control of antibiotic prescriptions evidenced increased bacterial resistance (2008-2010). Comments: Contro- lling daily institutionally prescribed antibiotics help to reduce bacterial resistance, but loosening the strategy reverses that trend.
Key words: Antibiotic control, antimicrobial resistance, antibiotic prescriptions
INTRODUCCIÓN
La aparición y uso de los antibióticos va de la mano con la aparición de resistencia bacteriana. Cada vez que ingresa a una institución un nuevo antibiótico y pasa el tiempo, se observa que los porcentajes de resistencia empiezan a aumentar (1). Por eso lo primero en el control de antibióticos y monitoreo de la resistencia bacteriana es definir la antibióticoterapia la cual puede ser utilizada en forma empírica, cuando se desconoce el agente causal, o etiológico. Cuando el agente ya ha sido identificado la antibioticoterapia será dirigida (2, 3). Sin embargo, antes de iniciar el tratamiento se debe obtener material, tanto para el examen microscópico que facilite la definición del tratamiento o su desescalamiento (4), evitando así la resistencia bacteriana mediante el control de la prescripción de antibióticos.
En los hospitales, la resistencia a los antimi- crobianos es determinada por problemas de falta de higiene de manos, limpieza y desinfección de áreas y por la presión selectiva creada por el uso excesivo e irracional de los antibióticos.
MARCO REFERENCIAL
Estudios muestran que más de 50% de las prescripciones de antimicrobianos en el medio hospitalario son inapropiadas y no obedecen a criterios microbiológicos, y que hasta 29% de las prescripciones de antibióticos de amplio espectro (carbapénicos y cefalosporinas) no están justifi- cadas debidamente, es decir, no se fundamentan en la flora local y perfil de resistencia institucional. El uso irracional e inadecuado de antimicrobianos tiene consecuencias a cuatro niveles: el paciente, el ecosistema hospitalario, la selección de cepas resistentes y los costos (5).
Para controlar antibióticos en las instituciones se plantean diferentes formas, las cuales no han mostrado ser mejores unas que otras. Describimos las formas más conocidas y utilizadas y reconocidas para el control de antibióticos.
1. Política Restrictiva, siendo la mayor de las estrategias para el uso racional de antibióti- cos (ATBs). Es la autorización del infectólogo para el uso de ciertos antimicrobianos en la institución.
2. Libertad de prescripción o no restrictiva. En la literatura mundial son pocas las comunicaciones sobre experiencias exitosas de programas de control de ATB (6). Jasovich y su grupo han reportado una experiencia de 10 años en 6 hospitales, logrando reducir el consumo y los costos con políticas de formulación libre de ATBs, con acompañamiento educativo perma- nente al médico con guías y protocolos claros y definidos (7, 8).
3. Desintensificación (deescalating) del tratamien- to ATB, que consiste en utilizar en pacientes graves la cobertura ATB empírica máxima hasta obtener resultados microbiológicos que permitan reducir el espectro de los antibacte- rianos utilizados (9).
4. Ciclado de antibióticos, que consiste en se- leccionar un ATB en particular (o un grupo de ellos) y no utilizarlo por un período de tiempo determinado, durante el cual es sustituido por otro ATB aprobado para las mismas indicacio- nes. Habitualmente los períodos de ciclado van de un mes a 2 años (10).
5. Control diario de prescripciones de antibióticos, no usual en las instituciones de salud. Es una opción, siempre y cuando se cuente con un grupo multidisciplinario o grupo de control de antibióticos que se encarga de controlar las prescripciones de antibióticos día a día en forma activa, analizando su pertinencia, relación con microbiología, con la norma institucional, su racionalidad, e interactuando con los diferentes servicios en donde se emite la prescripción (11).
6. Stewardship antimicrobial control, o gerencia- miento en el control de antibioticos (12, 13) es una forma actual de gerenciar institucionalmente el uso de antibióticos de forma multidisciplinaria centrado no solamente en la resistencia bac- teriana, sino en las variables que intervienen a aumentarla cuando la prescripción no es la adecuada, en relación a dosis, frecuencia, vía de administración. Controla la dosis diaria definida (DDD) el uso diario de antibióticos y los costos, siendo la ecuación directamente proporcional. La Resolución WHA 51.17 del 18 de Mayo de 1998 de la Asamblea Mundial de la Salud insta a los países miembros a adoptar medidas encamina- das a promover el uso de los antimicrobianos de manera apropiada y eficaz (14).
En Colombia, se encuentran liderando estas iniciativas de control de la resistencia bacteriana, instituciones como el INS (Instituto Nacional de Salud) y Secretarías Departamentales de Salud, a través de la red creada dentro del plan estratégico 2010 – 2014 para la contención de la resistencia bacteriana y el control de la IAAS, que se ha denominado: “Red Nacional para la Prevención, Vigilancia y Control de Infecciones Asociadas a la Atención en Salud (IAAS) y Resistencia a los Anti- microbianos” (15), la cual gradualmente se tendrá que implementar en cada institución y regional nacional. Actualmente se considera la infección un evento adverso evitable a IAAS y más si ésta se relaciona con un germen multirresistente.
En este estudio se muestra la experiencia ins- titucional de control de antibióticos, en la estrategia “Control diario de la prescripción de antibióticos” desde el 2004 fecha que se implementó hasta 2012 corte.
OBJETIVO
Controlar la prescripción diaria de antibióticos contribuye a disminuir la resistencia bacteriana.
OBJETIVOS ESPECÍFICOS
• Determinar el uso de tratamiento empírico y de tratamiento dirigido.
• Monitorizar la resistencia bacteriana.
METODOLOGÍA
Estudio descriptivo, transversal, del control de la prescripción diaria de antibióticos en el periodo comprendido entre el año 2004 a 2012. Durante este periodo se integró a las actividades del Comité de Vigilancia y Control de Infecciones, la actividad de controlar antibióticos diariamente. Se utilizó como herramienta de control diario, una hoja previamente diseñada por el comité y aceptada por el Comité de Bioética en investigación Institucional (hoja de prescripción antibiótica), que debían diligenciar diariamente los médicos cuando requerían prescribir antibióticos. En esta herramienta se verificaba el tipo de tratamiento: empírico o dirigido, y los anti- bióticos llamados de control institucional (ACI) por ser generadores de presión selectiva en bacterias denominadas de vigilancia epidemiológica (BVE).
El Comité de Vigilancia y Control de Infecciones estableció desde el inicio las definiciones aceptadas universalmente en control de antibióticos para los ítems que debían de llenar los médicos en la he- rramienta (hoja de prescripción antibiótica):
Bacterias de vigilancia epidemiológica (BVE): Son los microorganismos Pseudomona aeruginosa, Acinetobacter baumanii, Klebsiella pneumoniae, Es- cherichia Coli, por ser patógenos con alta resistencia a carbapenem y cefalosporinas de tercera generación.
Antibióticos de control institucional (ACI): Son aquellos que por su presión y mal uso son gene- radores de resistencia bacteriana: carbapenem y cefalosporinas de tercera generación.
Tratamiento empírico: Es el que se inicia ante la sospecha de infección por BVE, sin germen microbiológico determinado. Se solicita cultivo y se evalúa en 48 horas.
Tratamiento dirigido: Es llevado a cabo so- lamente con fundamento a la evidencia bacterio- lógica por cultivos positivos a BVE y sensibilidad demostrada a ACI.
Resistencia bacteriana: Son cambios en la plataforma genética de la bacteria secundaria a uso de antibióticos, alterando membrana, porinas, bombas de eflujo y producción de betalactamasas. Es evidenciada a través de cambios fenotípicos en la bacteria, informados en el antibiograma.
Se monitorizó la resistencia bacteriana a través de registros suministrados semestralmente por el Departamento de Microbiología de la Institución. Se comparaban semestralmente cada año el uso de antibióticos ACI y las llamadas BVE. Labor hecha por el equipo de vigilancia y control de Antibióticos conformado por: Infectólogo de adultos, Infectólogo Pediatra, Microbiólogo, Químico farmaceuta, jefe de vigilancia de IAAS (Infecciones Asociadas a la Atención en Salud), Jefe de control de ISO (Infec- ción de Sitio Operatorio) y la Dirección Científica de la Institución.
Se tomó para el monitoreo y el análisis de la resistencia bacteriana la unidad de cuidados inten- sivos, por ser el lugar en una institución de salud con mayor consumo de antibióticos denominados de control institucional (ACI) y en donde se repor- tan drogo resistencia o pan resistencia a bacterias denominadas de vigilancia epidemiológica (BVE).
Durante los años 2004 a 2007 (primer periodo) y 2008 a 2011 (segundo periodo), diariamente se evaluó la prescripción de antibióticos de control institucional (ACI) y se compararon semestral- mente cada año sus resultados, con el reporte de la resistencia bacteriana de la unidad de cuidado intensivo a BVE.
Para el mes de Junio del 2011se diseñó y desarrolló una herramienta por parte del depar- tamento de sistemas (Software de Microbiología) para mejorar la calidad del dato, el análisis y la intervención, haciendo más eficiente la captura del dato, generando cambios en la dinámica del trabajo del control diario de la prescripción de antibióticos. Pues como producto del Estudio se incorporó el gerenciamiento de antibióticos (Stewardship) como política Institucional en el control de antibióticos.
RESULTADOS
En el primer año 2004 en que se inició el control de antibióticos diario. A través de la herramienta se obtuvieron y analizaron 573 prescripciones, en el segundo año 2.192 prescripciones, al tercer año
3.093 prescripciones, y al cuarto año 2.622 pres- cripciones. El total de prescripciones de antibióticos revisado durante los cuatro años fue de 8.480, con
un promedio de 2.120 (DE+/-: 1.095) prescripciones.
El mantener un promedio por semestre de 2.120 (DE+/- : 1.095) prescripciones de antibió- ticos realizadas, permitía observar la adherencia del personal médico a las recomendaciones del Comité de Vigilancia Epidemiológica, con relación al control de antibióticos y el diligenciamiento de la herramienta (hoja de prescripción antibiótica).
El porcentaje de los tratamientos empíricos con ACI al inicio de las medidas de control de antibióticos fue de 14,1%, mostrando a través del tiempo una disminución significativa (Chi2: 62,98; p: 0,0000) hasta valores de 7,3% en 2007, lo que denota la racionalidad y comprensión de lo que significa un tratamiento empírico y la necesidad de tener en cuenta la microbiología para el ajuste del tratamiento y pasar a dirigirlo.
Los tratamientos dirigidos con ACI también presentaron porcentajes altos de uso, al inicio del análisis, de 19,5%, mostrando en el tiempo dismi- nución significativa a 3,4% en 2007 (Chi2: 351,81; p: 0,0000), debido a racionalidad de uso de ACI después de contar con reporte microbiológico que permite y asegura el tratamiento como dirigido (Figura 1).
Tabla 1. Prescripciones de antibióticos de control institucional (ACI) en tratamientos Empíricos y Dirigidos 2004 -2007.
Primer Semestre Año |
Prescripciones por Semestre |
Tratamiento empírico ACI semestre |
% de tratamientos empíricos por prescripciones |
Tatamiento dirigido ACI semestre |
% ACI dirigido sobre total de prescripciones por semestre |
2004 |
573 |
81 |
14,1% |
112 |
19,5% |
2005 |
2192 |
141 |
6,4% |
260 |
11,9% |
2006 |
3093 |
160 |
5,2% |
101 |
3,3% |
2007 |
2622 |
192 |
7,3% |
89 |
3,4% |
Total |
8480 |
574 |
6,7% |
562 |
6,6% |
Fuente: Comité de Vigilancia Epidemiológica 2008.
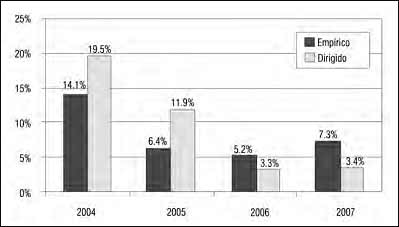 |
Fuente: Comité de Vigilancia Epidemiológica 2008.
Figura 1. Prescripciones de antibióticos de control institucional (ACI) en tratamientos Empíricos y Dirigidos. 2004-2007.
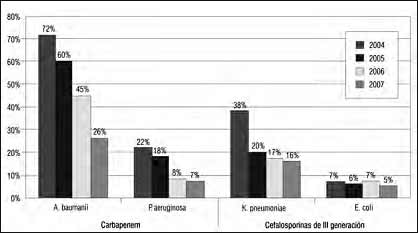 |
Fuente: Comité de Vigilancia Epidemiológica, Clínica General del Norte 2008.
Figura 2. Correlación entre porcentaje de ACI y resistencia bacteriana a BVE. 2004-2007
Se observó en el análisis de los ACI y las BVE una relación directamente proporcional del control de ACI en los tratamientos, tanto empíricos como dirigidos, en la institución. Con la disminución de la resistencia a BVE, en ese mismo periodo 2004- 2007 en Cuidados Intensivos (Figura 2), con coeficientes de correlación entre el porcentaje de ACI dirigido y la resistencia de A. Baumannii, P. Aeruginosa, K. pneumoniae, de 0,90, 0,98, 0,92, respectivamente; para E. Coli, el coeficiente de correlación fue bajo, mostrando una asociación igualmente baja entre las dos variables empírica y dirigida de 0,44.
Al correlacionar el control de antibióticos con el reporte microbiológico de la resistencia bacteriana del primer semestre de cada año, de 2004 a 2007, se encontró que en P.Aeruginosa la resistencia en UCI en 2004 fue de 22% a carbapenem, disminuyendo significativamente la resistencia bacteriana a 7% en 2007. Para A. Baumannii la resistencia en UCI a carbapenem registrada para el año 2004 fue de 72%, teniendo una disminución de la resistencia a carbapenem de 26% para 2007.
En K. pneumoniae la resistencia a cefalospo- rinas de tercera generación (ceftriaxona) al inicio de control de antibióticos institucional a través del Comité de Vigilancia Epidemiológica era de 38%, al corte de 2007 se encontró en 16%.
Para Coli la resistencia a cefalosporinas de tercera generación al inicio del control de antibióticos fue de 7%, al corte de 2007 fue de 5%.
Esta correlación observada entre ACI y BVE puede corresponder directamente a control de antibióticos. Hay que tener en cuenta que no sola- mente para disminuir la resistencia bacteriana se cuenta con esta estrategia. También está la limpieza y desinfección, higiene de manos, aislamiento, control de brotes.
El control de las prescripciones diarias de antibióticos se continuaron controlando (Figura
3) por el mismo equipo durante los años 2008 a
2011 ( segundo corte) notando gradualmente, poca adherencia al llenado de la herramienta (hoja de prescripción de antibióticos) reflejándose en varia- ciones importantes en la Resistencia Bacteriana durante ese periodo, aumentando la resistencia a P. Aeruginosa de 9.5% a 30.5% , Con el A. Baumannii se encontró 68% La E. Coli y la K. Pneumoniae, tuvieron también cambios importantes con incre- mento de la Resistencia , de 5% y 16% a 52% y
25% respectivamente para el 2010.
Estos cambios observados en la resistencia bacteriana, estuvieron acompañados durante este periodo de falta de diligenciamiento adecuado de la herramienta, poca adherencia a las políticas de antibióticos y rotación de personal.
Si tomamos en cuenta la relación directamente proporcional entre control de antibióticos y dismi- nución de resistencia bacteriana, se podría decir que no controlar antibióticos es variable influyente en aumentar la resistencia, como lo observamos en el segundo corte 2008-2010.
Esto llevó al equipo en el año 2011 a replantear el trabajo diario. Se detectó que la recolección de la información diaria, por el tamaño de la Institu- ción (360 camas), no facilitaba la recolección de la prescripción en la herramienta utilizada hasta ese momento, además de la rotación del personal, falta de adherencia a las guías recomendadas y divulgación por parte del comité de las políticas de control de antibióticos.
Después del análisis causal y detectado las debilidades del proceso, como plan de mejora se diseñó y desarrolló una herramienta (sistematiza- da) por parte el departamento de sistemas de la institución, para mejorar la calidad del dato y el análisis y la intervención (Figura 4).
Esta herramienta de sistema nos permitió inicialmente comparar la información de la pres- cripción diaria de antibióticos de Febrero a Mayo (forma manual) 428 prescripciones. Con la forma sistematizada (software Perfil Microbiológico y Terapéutico) de Junio-Septiembre, 3.208 pres- cripciones, mejorando así la fuente de registro de información, el dato y mejorando el control diario de la prescripción de antibióticos.
Al finalizar el año 2011 (Figura 5) con la imple mentación de la nueva herramienta sistematizada
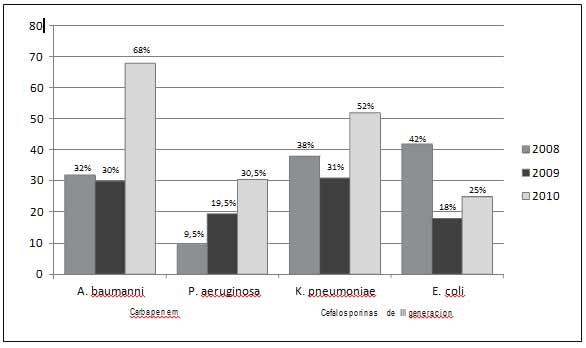 |
Fuente: Comité de Vigilancia Epidemiológica, Clínica General del Norte 2011.
Figura 3: Correlación entre porcentaje de ACI y resistencia bacteriana a BVE. 2008-2010.
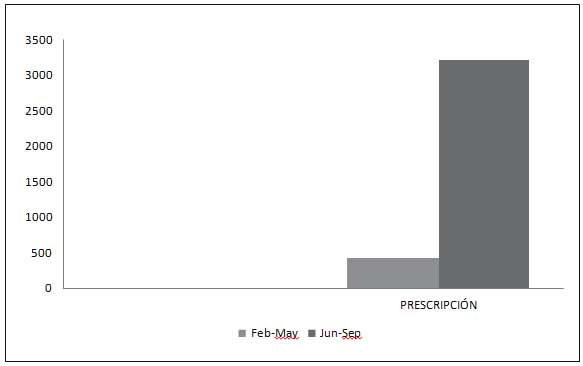 |
Fuente: Comité de Vigilancia Epidemiológica, Clínica General del Norte 2011.
Figura 4. Número de prescripciones, antes y después de una nueva herramienta Sistematizada. 2011.
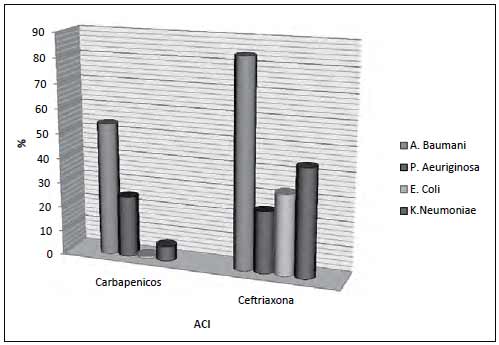 |
Fuente: Comité de Vigilancia Epidemiológica, Clínica General del Norte 2011.
Figura 5. Resistencia Bacteriana a Carbapénicos y Cefalosporinas de Tercera Generación 2011
se muestran disminución de las resistencias a A. Baumanii y P.Aeruginosa de 54% y 25% respecti- vamente, en relación a porcentajes de resistencia obtenidos en el 2010 de 68% para A. Baumanii y 30.5 para P.Aeruginosa. En relación a los carbapénicos. Las cefalosporinas de tercera generación mantienen resistencias altas a E. Coli y K. Pneumoniae (16).
Notando la tendencia de controlar antibióticos ACI, contribuye a disminuir la resistencia bacteriana a BVE o lo contrario. Como en el caso E. Coli y K. Pneumoniae en relación a cefalosporinas que aumenta.
A partir de la experiencia adquirida con el control diario de la prescripción de antibióticos desde el
2004 y la nueva herramienta sistematizada desde el 2011, la institución asume como compromiso y proyecto institucional la metodología de control de antibióticos “Antimicrobial stewardship programs” a partir del año 2012, conformando un grupo de gerenciamiento de antibióticos, está integrado por:
a) Comité de farmacia y terapéutica. Enfermera epidemióloga clínica, infectólogo, Microbióloga. B) Comité de vigilancia y control de infecciones. Este trabaja en: Dosis diaria definida (DDD), uso de antibióticos (ACI), tipo de tratamiento empírico o dirigido, dosis, frecuencia, costos, auditoria con- currente y resistencia bacteriana.
DISCUSIÓN
En las instituciones de salud usualmente no existen grupos de profesionales dedicados al control de la prescripción de antibióticos. Posiblemente se trabaja en la higiene de manos, en los métodos de barrera en las medidas de aislamiento, pero poco en el control de antibióticos.
Los resultados obtenidos con el control diario de las prescripciones de antibióticos durante el estudio evidencian que controlar antibióticos ayuda a disminuir la resistencia bacteriana, en el periodo 2004-2007. La falta de adherencia a las políticas Institucionales de control de las prescripciones de antibióticos, evidenció en el estudio aumento de la resistencia bacteriana, en el periodo 2008-2010.
Siendo el control de antibióticos una medida a tener en cuenta en toda institución, como medi- da contributiva a la disminución o aumento de la resistencia bacteriana.
La implementación de programas sistema- tizados para el control de antibióticos, mejora la calidad del dato, la intervención y proporciona una herramienta para monitoreo de la resistencia bacteriana controlando antibióticos.
Stewardship antimicrobial control, desde el 2012 es el programa institucional adaptado con base a la experiencia de control diaria de la prescripción de antibióticos, es el plan de mejora integral para el control de antibióticos y resistencia bacteriana (17).
REFERENCIAS
1. Shlaes DM, Gerding DN, John JF Jr, Craig WA, Bornstein DL, Duncan RA, et al. Society for Healthcare Epidemiology of America and Infectious Diseases Society of America Joint Committee on the Preven- tion of Antimicrobial Resistance: guidelines for the prevention of antimicrobial resistance in hospitals. Clin Infect Dis 1997; 25(3): 584-99.
2. Apisarnthanarak A, Danchaivijitr S, Khawcharoen- porn T, Limsrivilai J, Warachan B, Bailey TC, et al. Effectiveness of education and an antibiotic-control program in a tertiary care hospital in Thailand. Clin Infect Dis 2006; 42(6): 768-75.
3. Nathwani D. How do you measure the impact of an an-
tibiotic policy? J Hosp Infect 1999; 43 (Suppl): S265-8.
4. Villegas MV, HartsteinAl.Acinetobacter outbreaks 1977-
2000. Infect Control and Hosp Epi 2003; 24(4): 284-295.
5. Paterson DL. The role of antimicrobial management programs in optimizing antibiotic prescribing within hospitals. Clin Infect Dis 2006; 42 (Suppl 2): S90-S95.
6. Crowe H M, Quintiliani R. Antibiotic Formulary Selec- tion. In: Cunha B, Guest Editor The Medical Clinics of North America, Antimicrobial Therapy I, W.B. Saunders Company May 1995: 79 (3); 463-76.
7. Jasovich A, Curcio D, Prieto S et al. Is it feasible to reduce consumption and cost of antibiotics with freedom of prescription? A 10-year experience in 6 hospitals. Abstract of the III Panamerican Congress of Infection Control and Hospital Epidemiology. Belo Horizonte, Brazil, Nov 2000.
8. López-Medrano F, San JR, Serrano O, Chaves F, Lumbreras C, Lizasoain M, et al. [Impact of a non- compulsory antibiotic control program (PACTA): cost reductions and decreases in some nosocomial infections]. Enferm Infecc Microbiol Clin 2005; 23(4):
186-90
9. Höffken G, Niederman M S. Nosocomial pneumo- nia: The importance of a Deescalating strategy for antibiotic treatment of pneumonia in the ICU. Chest
2002; 122 (6): 2183-96.
10. Martin C, Ofotokun I, Rapp R, Empey K, Armitstead J, Pomeroy C, et al. Results of an antimicrobial control program at a university hospital. Am J Health Syst Pharm 2005; 62(7): 732-
11. Bantar C, Franco D, Heft C, Vesco E, Arango C, Izaguirre M, et al. Alternative indicators for monitor- ing the quality of a continuous intervention program on antibiotic prescribing during changing healthcare conditions. J Chemother 2005; 17(3):277-82
12. Pestotnik SL. Expert clinical decision support systems to enhance antimicrobial stewardship programs: insights from the society of infectious diseases pharmacists. Pharmacotherapy 2005; 25(8): 1116-25.
13. Organización Mundial de la Salud.http://apps.who.
14. Instituto Nacional de Salud. www.ins.org.co
15. Owens RC, Jr., Fraser GL, Stogsdill P. Antimicrobial stewardship programs as a means to optimize anti- microbial use. Insights from the Society of Infectious Diseases Pharmacists. Pharmacotherapy 2004;
24(7): 896-908.
16. Villegas MV, Correa A, Perez F, Zuluaga T, Radice M, Gutkind G, et al. Detection of CTX-M 12 from K. pneumoniae in Colombia. Antimicrob Agents Che- mother 2004; 48: 629
17. MacDougall C, Polk RE. Antimicrobial stewardship programs in health care systems. Clin Microbiol Rev
2005; 18(4):638-56.
Recibido: Febrero 7, 2014
Aprobado: Mayo 10, 2014
Correspondencia: Dr. Rubén Darío Camargo R. MD dcientifica@clinicageneraldelnorte.com